| 氟硅酸一步法制备氟化钠 |
b. 江西理工大学,冶金与化学工程学院, 江西 赣州 341000
b. Faculty of Metallurgy and Chemical Engineering, Jiangxi University of Science and Technology, Ganzhou 341000, China
磷肥是农作物的重要肥料,我国是磷肥(普通过磷酸钙)生产和消费大国.2010年我国磷肥产量超过1400万t,通常每生产1 t普钙(100 %P2O5)大约副产0.06 t氟硅酸(100 %H2SiF6)[1], 以此计算,全国磷肥行业副产大量氟硅酸.目前磷肥厂副产的低浓度氟硅酸(H2SiF6),实际回收利用量不足三分之一,多数不回收,直接用水冲稀排放.既污染了环境,又浪费了宝贵的氟资源.磷肥厂回收的氟硅酸可用来制备氟硅酸钠、氟化铝、冰晶石、氟化钠、氟化钾等.目前回收氟硅酸的大多厂家用于制备氟硅酸钠(Na2SiF6),但容易产生二次污染——盐酸废水.部分厂家用氟硅酸制氟化铝(A1F3),因成本过高生产受到限制[2-5].因此氟硅酸的再利用将成为制约磷肥企业生产的“瓶颈”问题,探索新的处理磷肥副产氟硅酸的途径,充分利用磷矿资源,实现氟资源再利用已十分紧迫[6].
NaF是一种重要氟化物产品,广泛用于木材防腐剂、酿酒杀菌剂、电解铝调整剂、牙齿氟化剂等领域.目前,生产NaF的工艺主要有熔浸法、中和法、氟硅酸钠纯碱法、纯碱法等.本工艺采用磷肥工业副产氟硅酸为原料,与纯碱液一步法进行反应,分离后得氟化钠和二氧化硅,产品均符合国家标准[7].
1 实验部分 1.1 反应原理传统的两步法生产氟化钠工艺[8]:
第1步,用NH4HCO3和H2SiF6反应生成NH4F溶液和SiO2沉淀.反应式如下:
H2SiF6 + 6NH4HCO3→SiO2+ 6NH4F+6CO2↑+ H2O
第2步,用Na2CO3与NH4F溶液反应制备NaF反应式如下:
2NH4F+Na2CO3→2NaF + (NH4)2CO3
本实验采用纯碱一步法进行反应,总化学反应方程式为:
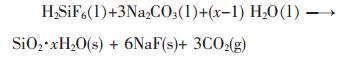
|
该反应为气液固三相反应,反应中不断有CO2气泡逸出和SiO2沉淀生成,同时不断有NaF晶体析出.该反应由以下步骤组成:中和反应:H2SiF6+ Na2CO3=Na2SiF6+CO2↑+H2O;复分解反应:2Na2CO3+ Na2SiF6=6NaF+SiO2+2CO2↑
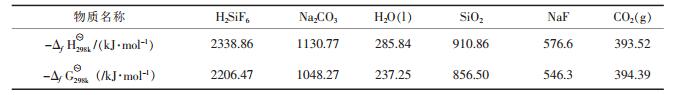
表 1为总方程式中各物质的标准摩尔生成焓和标准摩尔自由焓[9],由表 1可得方程式的标准反应热为: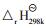
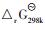
| 表1 各物质的标准摩尔生成焓和标准摩尔自由焓 |
 |
| 点击放大 |
1.2 主要仪器设备及试剂原料
仪器设备:玻璃烧杯、三口烧瓶、电子恒速搅拌器、分液漏斗、恒温水浴锅、真空泵和恒温水槽、硅胶分离器、真空蒸发装置、恒温鼓风干燥箱等.
原料:氟硅酸(23.1 wt%,磷肥副产品),碳酸钠(工业级,96.8 %),硫酸(工业级,98.0 %).
原料和产品质量按国家标准规定分析检测.
1.3 实验流程由氟硅酸生产氟化钠的工艺流程图如图 1所示.
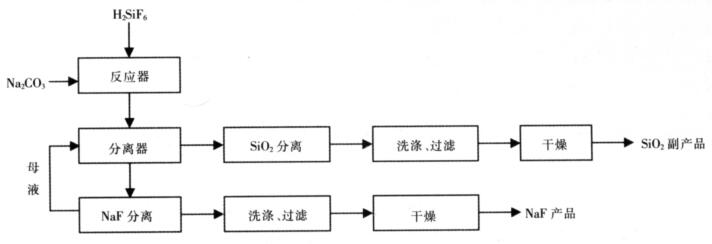 |
| 图 1 由氟硅酸生产氟化钠工艺流程图 |
2 实验结果与讨论 2.1 反应条件的选定
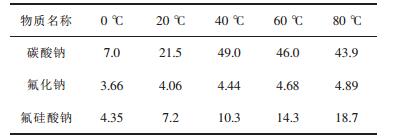
(1) 原料配比对反应的影响.此反应为多相反应,为使H2SiF6反应完全,全部以硅胶的形式析出,纯碱需过量.由于硅胶和NaF密度的差异,藉助重力作用使之分离,应注意NaF表面附着未反应完的Na2SiF6和硅胶,尽可能避免产生“包晶”现象[3].表 2给出了Na2CO3、NaF在水中的溶解度数据[8].从表 2中可知,40 ℃时Na2CO3溶解度最大,配料时先将Na2CO3在40 ℃下溶解.NaF的溶解度在4 %左右,故在反应得到NaF结晶时,大约4 %的NaF留在Na2CO3溶液中.因溶液中存在Na2CO3,盐析效应会使NaF溶解度<4 %.
| 表2 碳酸钠、氟化钠和氟硅酸钠在水中不同温度时的溶解度/% |
 |
| 点击放大 |
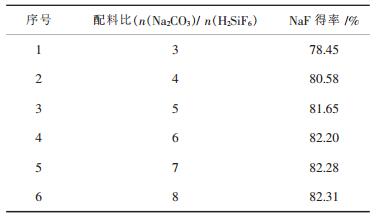
在其他反应条件相同下,实验考察碳酸钠和氟硅酸配料比(摩尔比)对氟化钠得率的影响,结果如表 3.由表 3可知,碳酸钠和氟硅酸配料比越高,NaF得率增大.配料比为3时,反应按化学计量比进行,氟化钠得率略低.但配料比大于化学计量比时,氟化钠得率增加.但是当配料比达6后,氟化钠得率增加不明显.因此,选定反应中配料比n(Na2CO3)/n(H2SiF6)= 6.0,且所得NaF纯度和得率均达标准.
| 表3 配料比对氟化钠得率的影响 |
 |
| 点击放大 |
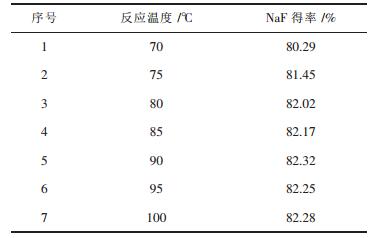
(2) 反应温度对氟化钠得率的影响.反应为吸热反应,则温度升高有利于反应的进行.实验考察不同反应温度下氟化钠的得率情况,结果如表 4.从表 4的实验结果可以看出,随着温度升高,氟化钠得率有所增大.实验选择反应温度为90~95 ℃.
| 表4 反应温度对氟化钠得率的影响 |
 |
| 点击放大 |
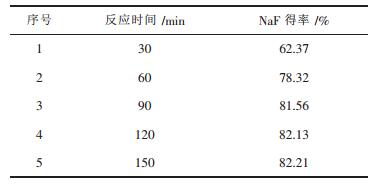
(3) 反应时间对氟化钠得率的影响.在配料比n(Na2CO3)/n(H2SiF6) =6.0,反应温度为90 ℃条件下,实验考察反应温度对氟化钠得率的影响.结果如表 5.反应时间较短时,氟化钠的得率偏低,随着反应时间的增加,氟化钠得率提高,当反应时间达到120 min后,氟化钠得率增大的程度较小.综合考虑,确定反应时间为90~120 min.
| 表5 反应时间对氟化钠得率的影响 |
 |
| 点击放大 |
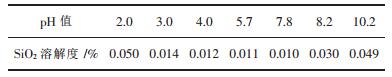
(4) 溶液pH值的影响.25 ℃时SiO2溶解度与pH值的关系如表 6.由表 6可知,pH值超过8.0时,SiO2的溶解度急剧增加.因此进行SiO2分离时选定pH值在7.8以下.综合实验结果,选定pH值为5.0~5.5.
| 表6 25 ℃时SiO2溶解度与pH值的关系 |
 |
| 点击放大 |
2.2 氟化钠生产工艺条件
配料比:n(Na2CO3)/n(H2SiF6)=6.0~6.3;
应温度:90~95 ℃;
反应时间:90~120 min;
pH值: 5.0~5.5.
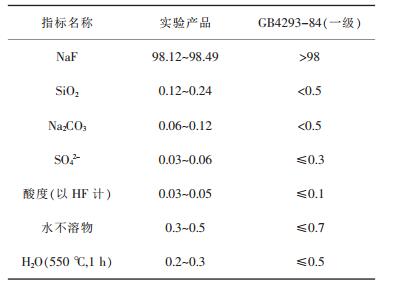
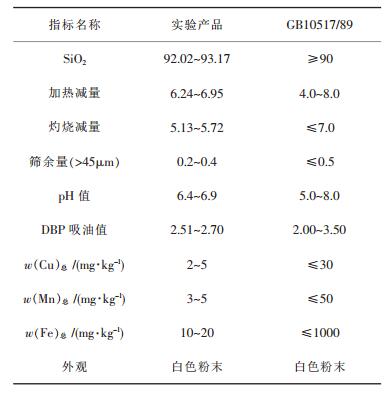
2.3 产品质量实验所得产品及相关产品质量及有关国家标准规定的技术指标见表 7和表 8.氟化钠产品符合国标GB4293-84一级品的质量要求;副产品SiO2符合国标GB10517/89的产品质量要求.
| 表7 氟化钠产品质量/wt% |
 |
| 点击放大 |
| 表8 副产SiO2质量/wt% |
 |
| 点击放大 |
3 结论
(1) 利用磷肥行业副产氟硅酸,采用纯碱法一步制备氟化钠, 原料费用低、工艺简单、易操作, 所得氟化钠产品符合国标GB4293-84一级品的质量要求;副产品SiO2符合国标GB10517/89的产品质量要求.为氟硅酸生产氟化钠工业化提供一个切实可行的新工艺.
(2) 具体工艺为:反应原料纯碱和氟硅酸摩尔比为n(Na2CO3)/n(H2SiF6)=6.0,反应温度为90~95 ℃,反应时间为90~120 min,溶液pH为5.0~5.5.
| [1] | 杨先. 磷肥行业副产氟硅酸的综合利用研究[D]. 昆明: 昆明理工大学, 2005. http://cdmd.cnki.com.cn/Article/CDMD-10674-2005130529.htm |
| [2] | 王贺云. 由磷肥副产氟硅酸制取冰晶石的过程研究[D]. 南昌: 南昌大学, 2006. http://cdmd.cnki.com.cn/Article/CDMD-11902-2006121693.htm |
| [3] | 唐忠诚, 唐文斌, 刘璇, 等. 纯碱处理氟硅酸溶液一步法生产氟化钠[J]. 磷肥与复肥, 2004(3): 56. |
| [4] | 魏琴. 利用磷肥副产物氟硅酸(钠)生产冰晶石工艺浅析[J]. 硫磷设计与粉体工程, 2010(2): 40. |
| [5] | 刘晓萍, 刘晓红. 氟硅酸制氟化钠和白炭黑[J]. 化学工业与工程, 2005(2): 154. |
| [6] | 郭伟杰. 由磷肥企业副产氟硅酸制备氟化钠的研究[J]. 中国资源综合利用, 2007(7): 4. |
| [7] | 周秀梅. 磷肥副产物生产氟化钠联产水玻璃工艺技术[J]. 磷肥与复肥, 2010(4): 60. |
| [8] | 卢芳仪, 卢爱军. 由氟硅酸制氟化钠新工艺研究[J]. 硫酸工业, 2004(2): 25. |
| [9] | Dean J A. 兰氏化学手册(第2版)[M]. 魏俊发, 译. 北京: 科学出版社出版, 2003. |
 2011, Vol. 2
2011, Vol. 2

