| Ru-La2O3/Al2O3催化剂上CO选择氧化本征反应动力学 |
b. 江西理工大学, 工程研究院, 江西 赣州 341000
b. Engineering Research Institute, Jiangxi University of Science and Technology, Ganzhou 341000, China
燃料电池是解决能源危机和环境污染最有发展前景的动力源之一, 所用氢燃料主要来自天然气(甲烷)或甲醇重整, 重整气经变换后所含的浓度1%的CO会使燃料电池阳极铂电极中毒, 因而必须将CO的浓度控制到0.01%以下[1].CO选择催化氧化反应是将富氢气中CO含量减少到10-6级最有效的方法[2], 常用的催化剂包括金、铂、钌、钯贵金属及铜、钴等非贵金属.其中铂、钌催化剂具有良好的CO选择氧化性能.稀土元素La由于其独特的4f电子层结构, 在合成氨、制氢等催化反应中表现出良好的助催化性能[3-4].前期研究发现, Ru-La2O3/ Al2O3催化剂有较好的CO选择氧化活性[5-6].
催化剂上本征动力学的研究, 对研究CO催化剂床层温度及浓度分布、反应器优化设计具有重要的意义.对CO氧化反应动力学的研究也多集中在金、铂催化剂上.目前关于Ru/Al2O3基催化剂上反应动力学的基础数据十分匮乏, 为了研究富氢气体中CO选择氧化本征动力学, 探讨其氧化反应机理, 实验在固定床微分反应器进行Ru-La2O3/ Al2O3催化剂上CO选择氧化数据收集, 并进行计算拟合, 得出反应级数及活化能.
1 实验部分 1.1 催化剂的制备、装填催化剂的制备采用浸渍法, 具体方法见文献[6].
催化剂的装填分3步骤:即反应床层分为3层.首先在反应器中装填1mL的石英砂, 然后再装填用石英砂稀释过的催化剂, 最后在催化剂上层装填1.5mL的石英砂.反应床层上下两端用石英棉填充.
1.2 动力学实验本征动力学实验在消除内外扩散及内部温度热效应后进行.反应器模型是活塞流微分反应器, 该反应器催化剂用量少, 反应转化率较低, 可以假定在其转化率范围内, 反应速度基本保持不变, 取微元反应层作物料衡算有:-rco=(Fco/Wcat)×(XAa-XA1)=Fa×Xco×Yco/Wcat式中:Fa为反应原料混合气的体积流量; Xco为氧化碳转化率; Yco为原料气中CO的体积分率; Wcat为催化剂用量.
本研究中原料气空速为40, 000h-1, 催化剂用量为0.01g, 换算得CO氧化速率计算式为:
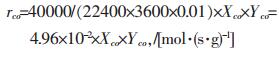
|
(1) |
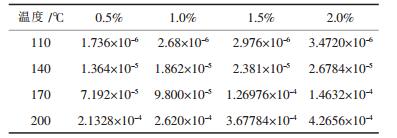
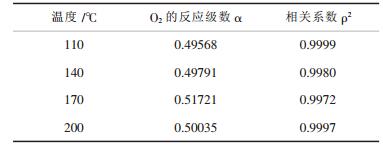
实验考察不同温度点O2分压对其自身选择氧化反应速率的影响, 根据测得的反应转化率, 由式(1)得CO的氧化速率如表 1所示.以表 1中O2浓度的常用对数ln(YO2)为横坐标, CO选择氧化反应速率的常用对数ln(Rco)为纵坐标, 作图 1.对图 1数据通过线性拟合, 可以得到各温度点下反应中氧的反应级数, 如表 2所示.各温度条件下, 相关系数为ρ2>0.9, 可以认为氧气的反应级数为0.5.
| 表 1 O2浓度(体积分数)对CO选择氧化反应速率rco的影响/[mol·(g·s)-1] |
 |
| 点击放大 |
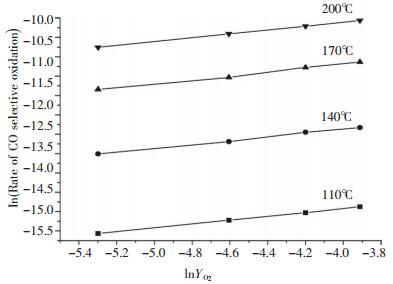 |
| 图 1 氧气浓度对CO选择氧化速率的影响 |
| 表 2 各温度点氧反应级数和相关系数 |
 |
| 点击放大 |
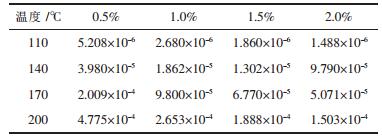
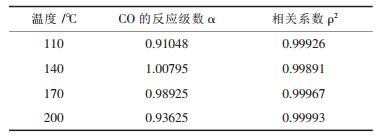
考察各温度点下CO分压对其选择氧化反应速率的影响, 结果如表 3所示.以表 3中CO浓度的常用对数ln(Yco)为横坐标, CO选择氧化反应速率的常用对数ln(Rco)为纵坐标, 得到图 2.对图 2中数据通过线性拟合, 可以得到反应中CO的反应级数, 如表 4所示.各温度条件下, 相关系数为ρ2>0.9, 可以认为CO的反应级数为一级.
| 表 3 CO浓度(体积分数)对CO选择氧化反应速率rco的影响/[mol·(g·s)-1] |
 |
| 点击放大 |
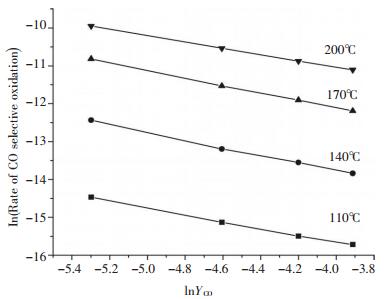 |
| 图 2 CO浓度对CO选择氧化速率的影响 |
| 表 4 各温度点CO反应级数和相关系数 |
 |
| 点击放大 |
为求反应活化能, 以温度的倒数1/T为横坐标, 以CO氧化速率的常用对数ln(Rco)为纵坐标, 通过曲线拟合(如图 3), 得到CO氧化反应的活化能Ea为76.24kJ/mol, 指前因子K0为7.28×104, 相关系数ρ2为0.998.
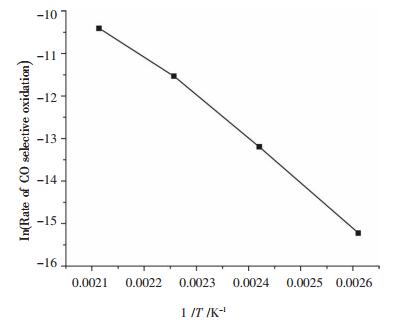 |
| 图 3 温度对富氢气体CO选择氧化反应速率的影响 |
对于CO氧化反应CO+1/2O2→CO2, 假设其遵循的模型:Langmuir-Hishelwood双活性非竞争吸附模型, 则CO选择氧化反应动力学表达式为: 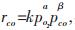
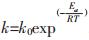
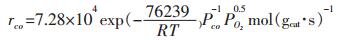
|
(2) |
初步推测CO的选择氧化反应是解离吸附态氧分别与吸附态CO和吸附态氢与发生的竞争反应, 反应体系反应机理为:

|
(3) |

|
(4) |
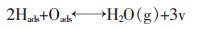
|
(5) |

|
(6) |

|
(7) |
根据上述反应机理, 在Langmuir理想吸附模型基础上进行CO选择氧化动力学方程式的推导, 各速率决定步骤相应的动力学方程式推导结果如下:
(1) 假设氧的解离吸附步骤(不可逆)(式3)为速率控制步骤:
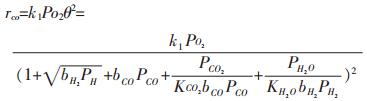
|
(8) |
其中k1为反应速率常数, KCO2, KH2O为相应物质反应平衡常数, bCO等为相应物质吸附平衡常数.
(2) 假设不可逆CO的吸附步骤(式6)为速率控制步骤:
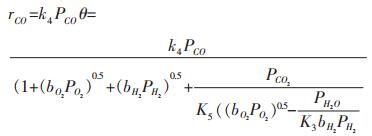
|
(9) |
(3) 假设解离吸附态CO和解离吸附态氧的表面反应(不可逆)步骤(式7)为速率控制步骤
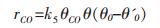
|
(10) |
式中θ0为吸附态氧分率, θ'0为参与氢的氧化反应的吸附态氧的分率, 根据Langmuir吸附等温方程, 可以得到:
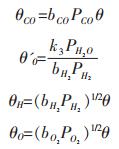
|
再由θco+θO+θH+θ=1得到:
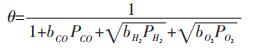
|
将上述结果代入式(10), 得到:
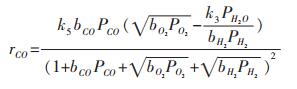
|
(11) |
因为实验条件下氢气的含量>65%, 在反应过程中PH2几乎不变, 可认为H2的反应级数为零, 又因为bCO很大, 且氢的吸附较弱, 所以有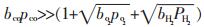
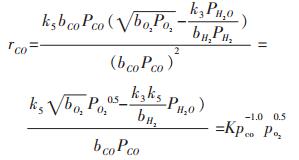
|
(12) |
将上述历程中的各速率控制步骤动力学方程形式与各个温度下动力学实验结果比较, 确定CO选择氧化反应速率控制步骤为催化剂表面吸附态CO与解离吸附态氧之间的反应.因而CO选择氧化速率方程式可以采用式(12)的表达式.
将动力学实验所得反应速率rco与其相应的气体分压PCO和PO2代入式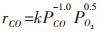
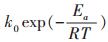
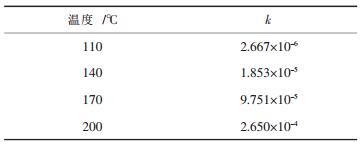
| 表 5 不同温度下反应速率常数 |
 |
| 点击放大 |
3 结论
采用浸渍法制备了Ru-La2O3/ Al2O3催化剂, 研究了富氢气体中CO在催化剂床层上的催化反应本征动力学.实验结果表明, 在消除内外扩散影响及内部温度热效应的前提下, Ru-La2O3/ Al2O3催化剂上CO的选择性氧化遵循非竞争性Langmuir Hinshelwood反应机理.催化剂的本征动力学方程是r CO =7.28 × 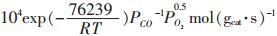
| [1] |
Park Eun Duck, Doohwan Lee b, Hyun Chul Lee. Recent Progress in Selective CO Removal in a H2 -rich Stream[J].
Catalysis Today, 2009, 139: 280–290. DOI: 10.1016/j.cattod.2008.06.027. |
| [2] |
Shuailin Zhou, Zhongshan Yuan, Shudong Wang. Selective CO Oxidation with Real Methanol Reformate over Monolithic Pt Group Catalysts: PEMFC Applications[J].
International Journal of Hydrogen Energy, 2006(6): 924–933. |
| [3] |
陈喜蓉, 董新法, 邹汉波, 等. 车载燃料电池富氢气体中CO选择氧化去除催化剂研究进展[J].
天然气化工, 2007, 32: 59–62.
|
| [4] |
Tiziano Montini, Rakesh Singh, Piyali Das. Renewable H2 from Glycerol Steam Reforming: Effect of La2O3 and CeO2 Addition to Pt/Al2O3 Catalysts[J].
Chem Sus Chem, 2010, 3: 619–628. DOI: 10.1002/cssc.v3:5. |
| [5] |
Xirong Chen, Hanbo Zou, Shengzhou Chen, et al. Selective Oxidation of CO in Excess H2 over Ru/Al2O3 Catalysts Modified with Metal Oxide[J].
Journal of Natural Gas Chemistry, 2007(12): 409–414. |
| [6] |
陈喜蓉, 董新法, 邹汉波, 等. Ru1La xOδ/ γ-Al2O3催化剂上CO选择性氧化去除性能及焙烧温度的影响[J].
现代化工, 2008, 3: 40–43.
|
| [7] |
朱炳辰.
化学反应工程(第3版)[M]. 北京: 化学工业出版社, 2001.
|
| [8] |
Han Y F, Kahlich M J, Kinne M, et al. CO Removal from Realistic Methanol Reformate Via Preferential Oxidation -performance of a Rh/MgO Catalyst and Comparison to Ru/γ-Al2O3 and Pt/γ-Al2O3[J].
Applied Catalysis B:Envirenmental, 2004, 14(5): 209–218. |
| [9] |
Dong Hyun Kim, Mee Sook Lim. Kinetics of Selective CO Oxidation in Hydrogen -rich Mixtures on Pt/alumina Catalysts[J].
Applied Catalysis A: General, 2002, 224: 27–38. DOI: 10.1016/S0926-860X(01)00739-6. |
 2011, Vol. 2
2011, Vol. 2
