| 钨制品中磷的测定 |
钨制品中微量磷的测定方法比较普及的是用正丁醇及氯仿萃取,利用萃取分离干扰组分,但操作烦琐,既费时又费力。且氯仿有毒,长期接触可能引起中毒。现改用氯化亚锡甘油溶液还原磷钼酸盐,生成亮蓝色配合物[1]。根据颜色的深浅比色测定。在水相中直接测定微量磷。本文研究了适宜的反应条件和共存离子的影响,己用于合成试样的分析。
1 实验部分 1.1 仪器与试剂仪器:721型分光光度计。
钼酸铵溶液:称取2.5g钼酸铵溶于少量水,以H2SO4定容至/0012。
氯化亚锡甘油溶液:称取2.5g氯化亚锡溶于100mL甘油中,溶解后储于瓶中。
氨水氯化铵洗液:取氯化铵1g溶于5%氨水中。磷标准溶液:
甲:称取0.4392g磷酸二氢钾溶解于100mL水中,移入一升容量瓶中,以水稀释至刻度,摇匀,此液1mL为100μg憐。
乙:取上液(甲)2mL于200mL容量瓶中,以水稀释至刻度,摇匀,此液每毫升为1μg磷。
1.2 实验方法 1.2.1 样品处理称取试样1~2g(钨制品均转化为WO3)于250mL烧杯中,加20mL10%氢氧化钾溶液,于低温电炉上分解完全,取下,用水吹洗表面皿及烧杯内壁至40mL体积,加氯酸钾0.5~1g,加热煮沸至冒大气泡取下,加10mL3%双氧水,搅拌1-2min,加4mL的2%EDTA溶液,搅匀,加一滴对硝基酚(0.1%),用盐酸(1 + 1)调至无色,然后用氨水调至溶液呈黄色,并过量16mL,以热水稀释至体积100mL,加10mL2%硫酸被溶液,边加边搅拌使沉淀完全,微沸1min,取下,静置30min,用快速定量滤纸过滤,以氨水洗液洗潘烧杯、沉淀各5~6次,甩去水柱,用1.2mol/L硫酸将沉淀溶解于100mL容量瓶中,并用此液稀至刻度,摇匀。
1.2.2 样品分析吸取样液5~10mL于50mL比色管中,加20mL水,2.0mL钼酸铵溶液,0.25mL氯化亚锡甘油溶液, 然后用水稀释至刻度,混匀。10min后用分光光度计690nm波长处,5cm比色皿,以水作参比,测定其吸光度,与试样同时做试剂空白试验。从工作曲线上求得相应磷的含量。
1.2.3 工作曲线移取质量浓度为1μg/mL的P(V)标准溶液0mL、0.5mL、1.0mL、1.5mL、2.0mL、2.5mL于一系列50mL比色管中,以下同样品分析。绘制工作曲线,利用工作曲线测定磷量。
2 结果讨论 2.1 检测波长的选择二氯化锡与磷钼酸盐形成稳定的配合物,按照试验方法绘制其吸收曲线证明该配合物的最大吸收峰在685nm~693nm处。本试验选定波长为690nm.
2.2 显色液的稳定时间试验试验表明,配合物经过10min达到稳定, 稳定时间在30min以内。
2.3 精密度和线性回归方程结果表明本方法形成的配合物在0μg~2.5μg P/ 50mL范围内服从朗伯-比尔定律,P的质量浓度在0~2.5μg/50mL与吸光度呈良好的线性关系。回归方程为y=0.021+0.075p(mg/L), 相关系数r为0.9908。对1.5μg P/50mL的标准溶液测定11次, RSD2.6%。
2.4 共存离子的影响在氨性溶液中,磷经氢氧化铍为载体生成磷酸盐沉淀, 与主体钨分离。因此钨不干扰磷的测定。
以15μg (1gWO3中)P为例,当吸光度相对误差≤±5%时,测得常见共存离子的允许限量(μg)为:Al(Ⅲ)600、Mg(Ⅱ)600、Cd(Ⅱ)500、Mn(Ⅱ)500、Pb (Ⅱ)500、Zn(Ⅱ)500、Cu(Ⅱ)250、Fe(Ⅲ)250、Ni(Ⅱ) 250、Co(Ⅱ)150、Sb(Ⅲ)150、Si(Ⅳ)150、As(V)6、Cr(Ⅵ)125。
2.5 甘油用量的影响添加适量的甘油,可以显著提高检测灵敏度。试验表明,随着甘油用量比例増加或减少,会导致体系配合物的吸光度不稳[2]甘油溶液的最佳体积比为0.125%.
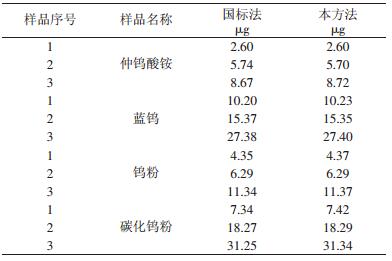
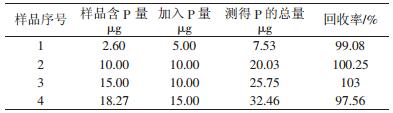
3 分析方法评定将此法用于合成试样中P的测定。分别取钨制品中仲钨酸铵、蓝钨、钨粉、碳化钨粉样品进行定量分析,并与国标方法作了对比,结果如表 1所示。可见本方法在钨制品磷的测定中,测得结果与国标法测得的结果基本一致。回收实验结果如表 2所示,回收率在97%~103 %之间,表明本方法具有较高的回收率。
| 表 1 钨制品中磷含量的测定 |
 |
| 点击放大 |
| 表 2 标准回收试验结果 |
 |
| 点击放大 |
以上测试结果表明,本方法数据稳定,准确度高,适用于钨制品中磷含量范围在0%~0.0030%的测定。
| [1] |
华东化工学院分析化学教研组.
分析化学[M]. 北京: 高等教育出版杜, 1989: 327-373.
|
| [2] |
黄传坤, 赵国君, 毛显林.
食品化学分析[M]. 上海: 上海科学技术出版杜, 1979: 97-101.
|
 2005, Vol. 19
2005, Vol. 19
