| 盐类矿物浮选中矿物的溶解及转化 |
盐类矿物在水中具有微溶性。在盐类矿物的共存体系中, 一种矿物溶出的构成离子在其他矿物表面的吸附以至发生反应, 将导致矿物表面性质的变化, 造成浮选分离的困难。本文以典型的盐类矿物萤石和方解石为对象, 研究了矿物的溶解对浮选分离的影响, 提出了矿物表面的相互转化是盐类矿物浮选分离的一个重要问题, 进一步揭示了复杂盐类矿物共存体系的浮选规律。
1 矿物共存对浮选的影响图 1和图 2分别为萤石和方解石在单独体系及共存体系中浮游率与捕收剂用量的关系, 所谓单独体系,即单一矿物在其饱和水溶液中的浮选; 所谓共存体系, 即在萤石-方解石的饱和水溶液中的浮选。捕收剂分别采用油酸钠(NaOl)及十二烷基硫酸钠(SDS), pH调整剂采用KOH。由两组图看出:萤石在共存体系中的浮游率明显低于其单独体系中的浮游率; 方解石在共存体系中, NaOl的浮游率与单独体系几乎完全一致, SDS的浮游率略低于单独体系。可见, 方解石的共存对萤石的浮选有显著的影响, 而萤石的共存对方解石的浮选影响甚小以至无影响。
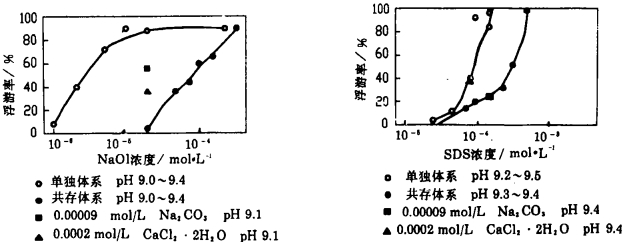 |
| 图 1 萤石在单独体系及共存体系中浮游率与捕收剂用量的关系 |
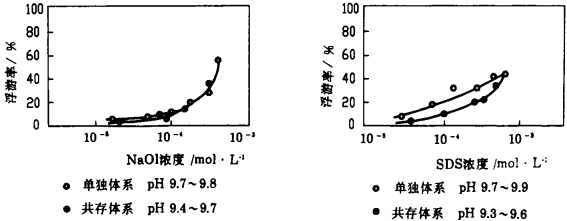 |
| 图 2 方解石在单独体系及共存体系中浮游率与捕收剂用量的关系 |
为了探讨方解石的共存对萤石浮选影响的原因, 人为地在萤石的单独体系浮选中加入Na2CO3以考察方解石溶出的CO32-离子的影响, 加入CaCl2以考察方解石溶出的Ca2+离子的影响。其加入的Na2CO3和CaCl2的量是根据计算方解石溶解平衡时溶出的CO32-和Ca2+离子的量来确定的。试验结果分别如图 1中的黑体四方形和黑体三角形所示。结果表明:在NaOl的浮选中, Na2CO3和CaCl2的加入均使萤石的浮游率显著下降; 在SDS的浮选中, 加入Na2CO3的影响与方解石共存的影响一致, 而加入CaCl2对萤石的浮选无影响。可认为:方解石溶出之Ca2+离子的影响, 是由于Ca2+离子与油酸离子生成油酸钙所致; 而溶出之CO32-离子则是方解石的共存对萤石浮选影响的主要因素。
CO32-离子的影响, 还可通过分别采用NaOH和Na2CO3调节pH, 萤石的NaOl浮选试验来证实, 其结果如图 3所示。当NaOl浓度为20mg/L时,用Na2CO3调节pH, 萤石的浮游率从pH值为8.5左右起便开始明显地下降, 而水溶液中的CO32-离子浓度也是从pH值为8.5左右起随pH的升高而急骤增大的; 采用NaOH调节pH的浮游率, 从pH12左右起急骤下降, 此现象可解释为OH-离子与油酸离子竞争吸附的结果[1]。
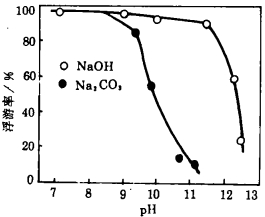 |
| 图 3 萤石的浮游率与pH的关系 |
2 矿物的溶解及矿物表面的相互转化 2.1 萤石在水中的溶解平衡
在萤石的饱和水溶液中存在下列平衡[2]:
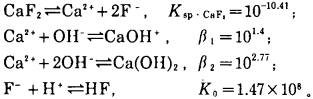
|
设F-的加质子反应系数、Ca2+的羟化反应系数及萤石的溶解度分别为aF-、aCa2+和Sm。
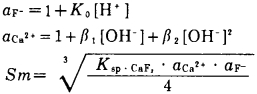
|
由于aF-、aCa2+都是溶液pH的函数,因此Sm也是pH的函数。绘pSm-pH关系曲线, 见图 4。
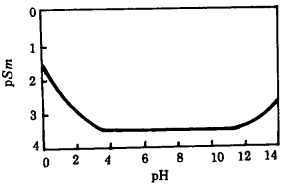 |
| 图 4 萤石pSm-pH图 |
由图 4看出, 在pH=4~12区间, pH对萤石的溶解度无影响, 在强酸和强碱中萤石的溶解度显著增大。这是在强碱中Ca2+的羟化反应和强酸中F-的加质子反应所致。
2.2 方解石在水中的溶解平衡在方解石饱和溶液中存在下列平衡:
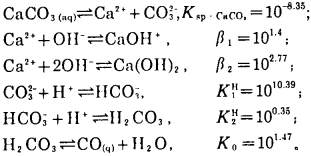
|
设CO32-的加质子反应系数、Ca2+的羟化反应系数和方解石的溶解度分别为aCO32-、aCa2+和Sm。
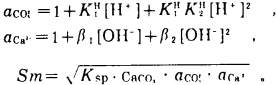
|
aCO32-、aCa2+都是溶液pH的函数, 绘pSm-PH关系曲线, 见图 5。
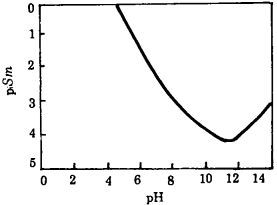 |
| 图 5 方解石pSm-PH图 |
由图 5看出, 方解石的溶解度受溶液pH的影响非常大。这主要是由CO32-的加质子反应造成的。H2CO3是弱酸, CO32-的加质子倾向非常强烈。CO32-在酸性介质中主要以HCO3-和H2CO3形式存在, 降低了CO32-的活度, 推动了方解石的溶解。
2.3 共存体系中矿物表面的相互转化图 6为分别对萤石、CaCO3及在Na2CO3溶液中的萤石进行红外线光谱分析的结果。在波数1420~1400cm-1处, Na2CO3溶液中的萤石出现与CaCO3相同的吸收谷。表明, 在萤石表面上生成了CaCO3。由此可推论, 在萤石-方解石的共存体系中, 矿物表面发生了转化。方解石溶出的CO32-离子在萤石表面吸附, 与萤石溶出的Ca2+离子生成了方解石。
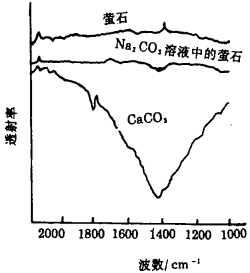 |
| 图 6 萤石、CaCO3及Na2CO3溶液中的萤石红外线光谱分析结果 |
矿物相互转化平衡关系可用下式表示:
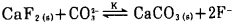
|
(1) |
反应标准自由能变化:
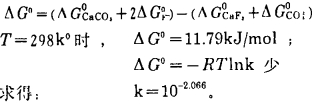
|
反应进行的方向与限度, 由共存体系中的F-离子和CO32-离子的活度大小决定。
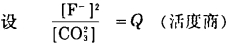
|
则当Q < k时, 反应朝正方向进行(萤石表面生成CaCO3); 当Q>k时, 反应朝反方向进行(方解石表面生成CaF2)。
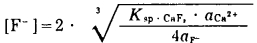
|
(2) |
开放体系中:
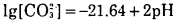
|
(3) |
计算各pH值下的lgQ值, 绘lgQ-pH曲线见图 7。曲线与lgk值(-2.066)交点处pH值为8.5。则当pH < 8.5时, Q>k, 方解石表面向萤石转化;pH>8.5时, Q < k, 萤石表面向方解石转化。
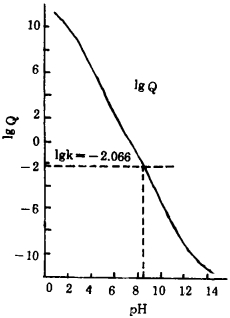 |
| 图 7 lgQ-pH关系图 |
用共存体系中矿物表面相互转化的观点可以较好地解释前述试验现象。图 1和图 3中, 在碱性范围, 人为地添加Na2CO3或有方解石共存的情况下, 萤石浮游率下降, 可认为在萤石表面有CaCO3生成所致; 图 2中, 方解石的浮游率不受萤石共存的影响, 可认为在碱性范围不存在方解石表面向萤石的转化。
根据以上的热力学分析, 对于萤石-方解石的浮选分离, 应在弱碱性矿浆中进行。在此条件下, 只存在萤石的表面向方解石的转化。虽然萤石的浮游将受一定的影响, 但有利于减少方解石在萤石精矿中的混杂。
3 结论以萤石-方解石共存体系为研究对象, 通过共存条件下的试验以及人为地向浮选体系中添加相应的矿物构成离子成分, 证实了矿物的溶解对共存体系浮选的影响及矿物表面相互转化的客观存在。
通过对矿物表面相互转化的热力学分析, 得出了矿物表面相互转化的热力学条件。用矿物表面相互转化的观点较好地解释了实验现象。表明, 矿物表面的相互转化是影响复杂盐类矿物共存体系浮选分离的重要因素, 进一步揭示了盐类矿物的浮选规律。
| [1] |
恒川昌美. 高森隆胜. 关于难处理盐类矿物优先浮选基础的问题. 札幌: 日本资源、素材学术会议分科研究会. 1988. 25~26
|
| [2] |
张治元, 王博. 共存体系中矿物表面的相互转化[J].
西部探矿工程, 1994, 6(6): 9–11.
|
 1997, Vol. 11
1997, Vol. 11
