| 选择性螯合滴定法测定铅含量 |
铅的螯合滴定法, 一般应用直接滴定法和返滴定法[1, 2]。奇怪的是用释放螯合滴定法测定铅, 报道很少[3, 4], 用H2SO4-BaCl2为释放剂, 螯合滴定法测定铅, 选择性大为提高[4]。为此提出用EDTA螯合铅(Ⅱ)和其他金属离子, 然后用氨荒丙酸铵(Ammonium dithiocarbamino-propoonate简称ADTCPA)作释放剂, 置换、释放Pb2+-EDTA螯合物中的EDTA(与Pb2+等摩尔数), 用XO(二甲酚橙)、MTB(甲基百里酚蓝)和CPB(阳离子表面活性剂溴化十六烷基吡啶)为混合指示剂, 锌标准溶液滴定释放析出的EDTA, 从而间接计算出铅的含量, 几乎所有金属离子均不干扰。利用此混合指示剂, 三者互相配合、协调、互补的颜色, 使滴定终点更加敏锐、清晰。用于测定铅基合金镀层、Pb-Sn-Cu合金镀层和电镀液中的铅, 结果准确、精密度高和操作方便。
为了操作上的简便, 笔者用氟化物、MSA(巯基丁二酸)[5]、ADTCPA, 分别作Sn4+、Cu2+和Pb2+的EDTA螯合物的释放剂, 分别定量释放出EDTA, 间接计算出锡、铜和铅的含量。从而实现了在同一份试液中, 同一pH值、缓冲溶液、指示剂和锌标准溶液, 连续释放螯合滴定法测定试样中的锡、铜和铅, 并在实际应用中获得了准确的结果。
1 实验部分 1.1 仪器与主要试剂UP-2型超精电动加液滴定仪。
铅标准溶液, 称取3.200g硝酸铅[Pb(NO3)2], 溶于50mL水中, 加入2mLHNO3, 然后稀释至1000mL容量瓶中, 摇匀, 2.00mgPb2+/mL, 需标定。
KF, 20%水溶液; MSA, 10%巯基丁二酸水溶液; 2, 4-二硝基酚溶液, 0.2%乙醇溶液(1+1)。
ADTCPA, 5%水溶液。
缓冲溶液, 30%六次甲基四胺水溶液。
EDTA, 0.025mol/L乙二胺四乙酸二钠溶液。
XO-MTB指示剂, 100mL二甲酚橙溶液(0.4%)中,加入0.05g甲基百里酚蓝(MTB)。
CPB, 3%溴化十六烷基吡啶水溶液。
锌标准溶液, 0.025mol/L乙酸锌溶液。
锡、铜标准溶液, 均为2.00mg/L。
1.2 实验方法 1.2.1 铅的单独滴定法吸取10.00mL铅标准溶液, 置于300mL锥形瓶中, 加入5mL KF(20%)、5mL MSA(10%)溶液、20mL EDTA(0.025mol/L), 滴加2滴2, 4-二硝基酚(0.2%), 滴加六次甲基四胺溶液由红变黄色、再加10mL六次甲基四胺溶液, 摇匀放置2min, 滴加4滴XO-MTB指示剂、3mL CPB(3%), 用锌标准溶液滴定至由黄色恰变为紫红色(不计读数)。加入5mLADTCPA溶液, 摇动1min(立即返黄色), 再用锌标准溶液滴定至由黄色恰变紫红色为终点, 记下消耗锌标准溶液的mL数为V。计算含铅量。
1.2.2 锡、铜和铅的连续螯合滴定法吸取锡、铜和铅标准溶液(均为2.00mg/mL)各5.00mL, 分别置于同一300mL锥形瓶中, 加入25mL EDTA(0.025mol/L), 滴加2滴2, 4-二硝基酚溶液, 滴加6次甲基四胺溶液(30%)至出现黄色、再加入10mL, 滴加4滴XO-MTB指示剂和3mLCPB(3%), 用锌标准溶液滴定至由黄色恰变紫红色(不计读数)。加入5mL KF(20%), 摇动(出现黄色), 放置3min, 用锌标准溶液滴定至由黄色恰变紫红色为终点(记下mL数为V1, 锡量); 加入5mL MSA(10%), 摇动返黄色并加热至60~75℃左右, 再用锌标准溶液滴定至由黄色恰变紫红色为终点(记下mL数V2, 铜量); 加入5mL ADTCPA(5%), 摇动0.5min, 又用锌标准溶液滴定至恰呈紫红色为终点(记下mL数为V3, 铅量), 分别计算锡、铜和铅的含量。
2 结果与讨论 2.1 释放剂的用量用氟化物[6]、MSA[7]作释放剂, 螯合滴定法测定锡和铜, 已作了论述。例如铜的释放螯合滴定的机理[5]:
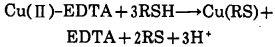
|
在酸性溶液中MSA具有还原作用和螯合作用, 将铜(Ⅱ)还原为铜(Ⅰ), 并与铜(Ⅰ)生成更稳定的螯合物[Cu(Ⅰ)-MSA], RSH代表MSA, Cu(RS)为一价铜的螯合物。MSA是Sn4+、Sn2+、Cu2+、Cu+、Hg2+、Bi3+等的最佳掩蔽剂, 也是它们的释放剂[8, 9]。5mL MSA(10%)能掩蔽50mg的Sn4+、Cu2+、Hg2+、Bi3+、Zr4+和Pd2+等[10, 11]。
ADTCPA能掩蔽Fe3+、Fe2+、Co2+、Cu2+、Ni2+、Ag+、Cd2+、Hg2+、Sn4+、Sn2+、Pb2+、Bi3+等[12], 在KF存在下, ADTCPA只能释放Pb2+、Cd2+、Cu2+、Hg+、Bi3+的EDTA螯合物中的EDTA[12, 13], 但不能释放其他金属离子的EDTA螯合物中的EDTA[13]。实验结果表明, 3~15mL KF(20%)、2~10mL MSA(10%)、3~12mL ADTCPA(5%), 均能定量释放Sn4+Cu2+和Pb2+的EDTAF螯合物中的EDTA, 实验均选用5mL。
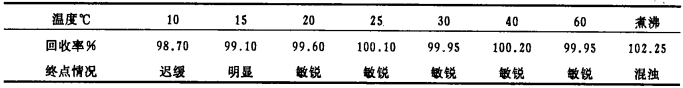
2.2 释放反应与温度、时间的影响实验表明, 在室温(15~35℃)或60℃条件下, 摇动0.5min, 即可定量释放出Pb-EDTA螯合物中的EDTA, 即使摇动5min, 也是如此.实验结果见表 1。
| 表 1 释放反应与温度 10mgPb2+ |
 |
| 点击放大 |
氟化物、MSA释放Sn4+、Cu2+的EDTA螯合物中的EDTA, 在15~35℃条件下, 放置0.5min以上, 均能定量释放完全。不过加入MSA后, 加热60~75℃左右, 终点颜色变化更加敏锐、清晰。
2.3 缓冲溶液的用量用2, 4-二甲基酚为指示剂, 滴加六次甲基四胺(30%)来控制pH值, 再加入10mL六次甲基四胺(30%), 在操作上容易掌握, 终点颜色变化十分敏锐、清晰。
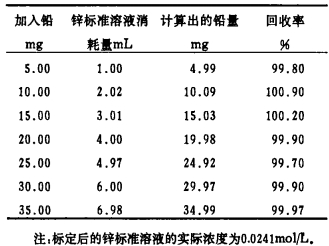
2.4 铅量与锌标准溶液消耗量的线性关系实验表明, 铅量与锌标准溶液消耗量呈良好的线性关系, 并且与理论计算结果完全一致。结果见表 2。按公式计算铅量:

|
| 表 2 铅量与锌标准溶液消耗量的关系 |
 |
| 点击放大 |
回收率为100%。
2.5 指示剂的选择与用量Krishna等在“用EDTA直接滴定Cd2+的指示剂颜色变化”中[14], 利用PAR[4-(2-吡啶基偶氮)-间苯二酚]和MTB混合指示剂, 终点敏锐[14]。实验表明, 利用XO、MTB和CPB混合指示剂、锌标准溶液滴定(在pH5~6), 终点颜色变化比用PAR和MTB混合指示剂, 更加敏锐、清晰[11]。从实践证明, 3~6滴XO-MTB指示剂, 效果最佳, 选用4滴; 2~5mLCPB(3%)则使终点颜色变化额外敏锐, 清晰, 当小于2mL时则变色不明显, 大于5mL则泡沫太多, 影响终点颜色变化的观察, 实验选用3mLCPB(3%)。
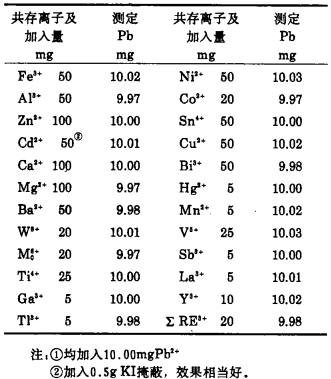
2.6 干扰离子及消除巧妙的用氟化物、MSA和KI等掩蔽Sn4+、Al3+、Cu2+、Bi3+、Hg2+、Cd2+等离子的干扰, 几乎所有阳离子都不干扰, 比文献[8]更先进。在弱酸介质(pH5~6)中, ADTCPA能释放Pb2+、Cd2+、Cu2+、Bi3+、Hg2+与EDTA螯合物中的EDTA[12, 13], 但是不能释放Fe3+、Fe2+、Ni2+、Co2+、Al3+、Zn2+、Sn4+的EDTA螯合物中的EDTA[13]。在pH5~6时,ADTCPA与Ca2+、Mg2+、Ba2+、Th4+、Ca3+、Mn2+、Gr3+、Mo6+、W6+、Ti4+、Zn2+、In4+、V5+、RE3+、碱金属、和碱土金属等无反应[12, 13]。在实际实验中Cu2+、Sn4+、Bi3+、Hg2+等用MSA掩蔽[8], 完全可靠。但是Cd2+是唯一干扰元素, 严重干扰测定铅含量, 可加入KI掩蔽之。实验选用了KF、MSA和KI作联合掩蔽剂, 应用ADTCPA为释放剂, 选择性的测定铅含量, 几乎所有金属离子, 均不干扰, 这是本方法的最大特点之一。实验还表明, 大量Cl-、F-、ClO4-、NO3-、SiO32-、C2H2O2-、PO43-、SO42-、P2O74-、硫脲、抗坏血酸、氟硼酸、间苯二酚、4, 4'-二氨基二苯甲烷和乳化剂OP、P2O74-等, 均不干扰锡、铜和铅的测定。对共存离子的影响, 结果见表 3。
| 表 3 共存离子的影响① |
 |
| 点击放大 |
3 实际应用与测定结果 3.1 铅基合金镀层及Pb-Sn-Cu合金镀层中铅含量的测定
称取0.2000g试样, 置于250mL高型烧杯中, 加入10mL酒石酸溶液(20%)及10mL浓硫酸摇匀后温热溶解试样, 加5mL硝酸, 加热煮沸驱除黄烟, 冷却后, 稀释至200mL容量瓶中, 摇匀。吸取50.0mL试液, 置于300mL锥形瓶中, 加入5mL KF(20%), 以下按1.2.1实验方法, 进行操作并按下式计算:
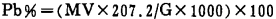
|
式中:M——锌标准溶液的浓度(mol/L);
V——为加入ADTCPA后所消耗锌标准溶液的mL数; 207.2——铅的原子量; G——相当试样重量, (0.200/200)×50=0.05(g)。
锡、铜和铅的连续测定:同上, 吸取50.00mL试液, 置于300mL锥形瓶中, 加入5mL H2O2(30%), 加热煮沸1min, 冷却, 加入35mL EDTA溶液, 以下1.2.2实验方法测定, 按下式计算:

|
式中, V1、V2分别为加入释放剂后所消耗的锌标准溶液mL数; 其他同Pb%的计算式。
3.2 电镀液中锡、铜和铅的测定吸取2.00mL电镀液, 置于300mL锥形瓶中; 加入5mL H2O3(30%), 加热至微沸并冷却, 加2mL硼酸(20%), 35mL EDTA溶液, 按上述方法测定并计算其含量。
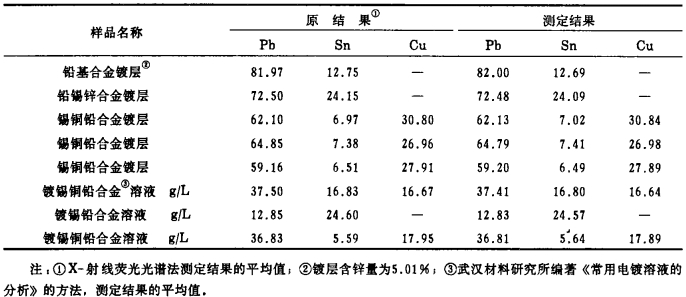
3.3 测定结果与准确度铅的单独滴定法和铅的连续螯合滴定法, 测定结果完全相同。用本方法测定了8种样品, 结果见表 4。对每种试样均测定7次, 将测定的数据, 进行数理统计处理, 变异系数CV=1.2%~4.6%, 其精密度和准确度, 均较高, 是目前较好的方法之一, 很有实用价值。
| 表 4 试样分析结果对比 % |
 |
| 点击放大 |
4 结论
本法巧妙地运用了氟化物、巯基丁二酸和碘化钾等联合掩蔽剂, 以氨荒丙酸为释放剂, 选择性的螯合滴定法测定试样中铅含量, 几乎所有金属离子都不干扰铅的测定。用XO-MTB-CPB为混合指示剂, 用锌标准溶液滴定, 终点颜色变化额外敏锐、清晰。本方法操作简便, 结果准确, 精密度高。
| [1] |
陈永兆.
络合滴定[M]. 北京: 科学出版社, 1986: 256.
|
| [2] |
陈焕光, 吴见新, 黄航星, 等. 以硫代苹果酸为掩蔽剂络合滴定法测定铅基合金中的铅[J].
冶金分析, 1994, 14(6): 17.
|
| [3] |
章道昆. 间接络合滴定法(综述)[J].
冶金分析, 1994, 14(4): 39.
|
| [4] |
Wang Xian-Ke. Seleetive ComPlexometric Titration of Lead in the Presence of Large Aomunts of Interfering lons[J].
The Analyst (London), 1990, 115(12): 1611. DOI: 10.1039/an9901501611. |
| [5] |
王献科, 李玉萍. 选择性螯合滴定法测定电镀液中的铜[J].
电镀与精饰, 1993, 15(6): 35.
|
| [6] |
张树成. 滴定分析(综述)[J].
分析试验室, 1991, 10(4): 90.
|
| [7] |
王献科. 锡的螯合滴定[J].
岩矿测试, 1991, 10(1): 64.
|
| [8] |
王献科, 李玉萍. 选择性螯合滴定法测定电镀液中的锡铜铅[J].
电镀与涂饰, 1994, 13(1): 43.
|
| [9] |
王献科, 李玉萍. 用MSA作释放剂选择性螯合滴定法测定锆[J].
耐火材料, 1995, 29(1): 48.
|
| [10] |
王献科. 大量干扰离子存在下铋的螯合滴定[J].
分析试验室, 1988, 7(3): 31.
|
| [11] |
王献科, 赵广翰. 长春首届分析化学国际学术会议论文选编. 长春: 吉林大学出版社(英文版), 1990. 462~474
|
| [12] |
姚守拙. 关于分析试剂α-氨荒丙酸铵[J].
湖南大学学报(自然科学版), 1981, 8(2): 31.
|
| [13] |
王献科. EDTA络量释放法测定锡青铜中的铜锡铅锌[J].
甘肃有色金属, 1989(3): 51–56.
|
| [14] |
M.M.K Krishna, G.Scarano. Complexometric Determination of Cadmium and the Colour change of end-point.Anal[J].
Chim.Acta, 1992, 364(1): 197–140. |
 1996, Vol. 10
1996, Vol. 10
