| 赣南荡坪复合硫化矿的三氯化铁直接浸出试验研究 |
试验原料来自赣南荡坪钨矿产出的硫化矿,其化学成分列于表 1。从中可知,试料中除了铜外,尚含较高品位的铅锌含量。试料中的铜主要以难浸出的黄铜矿存在。
| 表 1 复合硫化铜精矿的化学成分 % |
 |
| 点击放大 |
1.2 试验目的
本试验旨在探索试料中的铜、铅、锌等金属浸出率高,硫能利用,无污染,工艺技术简单,对设备要求不高,适合中小型企业的硫化矿直接浸出的工艺条件。
1.3 试验方案的选择国内外硫化铜精矿湿法冶金成熟的工艺是焙烧-浸出-电积流程。其优点是技术及设备简单,缺点是会产生废电解液过剩的问题,此外还需庞大的焙烧、收尘、制酸等设备,不宜于小型企业所采用。
高压酸浸、氨浸等直接浸出方法从设备、技术及经济上考虑仅适用于大规模处理含镍、钴高的复合硫化铜矿。至于氯化铜或硫酸高铁浸出法,无论是从文献报道或用本试料的初步探索性试验的情况都表明,铜的浸出速度慢且不完全。
综上考虑,试验选择三氯化铁直接浸出法,不但设备、技术简单,而且硫富集于浸出渣中,既可从中提取元素硫,亦可根据小型企业的实际情况直接将浸出渣以硫精矿的形态出售给制酸企业。此法用于处理铜铅锌复合硫化矿的报道尚不多见[1],本文主要探讨浸出工艺条件对浸出指标的影响。
2 三氯化铁直接浸出硫化矿的原理硫化物酸浸的平衡反应如下:

|
从热力学上看,除了反应平衡pH值较大的FeS、NiS、CoS外可用盐酸浸出,其他如CuS等平衡pH值很小的硫化物难于酸溶。而FeCl3为强氧化剂,E0(Fe3+/Fe2+)为0.77V, 高于除Ag2S外其余MeS的E0值,可将H2S进一步氧化为元素硫,使浸出反应平衡往右移动。不过实际浸出过程中,由于络合物的形成及动力学等原因,不但Ag2S也能被部分浸出,其他硫化物浸出的难易程度也与表 2中E0的顺序不完全一致。
| 表 2 各种硫化物的E0值 |
 |
| 点击放大 |
黄铜矿与磁黄铁矿被FeCl3浸出的平衡反应如下:
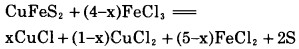
|
(1) |
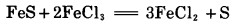
|
(2) |
PbS、ZnS的浸出有类似的反应。以上反应中的x值在0与1之间。FeCl3还可能将原料中少量硫进一步氧化为S042-:
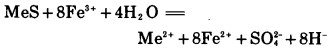
|
浸出后的铜可用废铁置换为海绵铜回收或还原、冷却结晶得氧化亚铜产品,还可直接或萃取后电积得电解铜。浸出的铅可加入硫酸或加铁屑、锌粉使之沉淀分离。至于锌则可在提铜铅后用叔胺萃取,碳酸钠反萃得到氢氧化锌,再将其干燥后以氧化锌形态出售。浸出液中的FeCl2可用空气氧化为FeCl3循环使用[2]。
3 浸出试验及结果分析 3.1 基本正交试验黄铜矿由于具有面心四面体晶格的结构,实际上是铜铅锌硫化矿物中最难浸出的,故先考虑铜浸出的情况。按反应(1)化学计量,FeCl3(mol):CuFeS2(mol)为3:1至4:1之间,换算成重量比则为3.5和2.7。取试验条件FeCl3(wt)/CuFeS2(wt)分别为3.5、2.7和2.1。
从热力学分析以及初步探索性试验表明,HCl浓度对Cu的浸出率影响不大。每次试验添加4mlHCl调整溶液的酸度,以避免铜离子的水解沉淀。其他试验条件的选择见表 3。
| 表 3 基本正交试验结果 |
 |
| 点击放大 |
将试料球磨8小时至-320目的占97.5%。每次试验试料量为50克。试验结果列于表 3。
若不考虑交互作用,用直观综合比较法似乎在试验条件范围内的最优条件组合是90℃、60分钟,液固比为4:1及FeCl3/CuFeS2为3.5。而根据最优回归子集法[3],用计算机将试验数据处理筛选出最优回归数学模型为:

|
按此数模预测,液固比对铜浸出率无明显影响,最优组合条件则是105℃、180分钟及FeCl3/CuFeS2为3.5。
3.2 最优组合条件验证试验将上述两种组合条件各作两次验证试验,其结果列于表 4。
| 表 4 最优组合条件验证试验结果 |
 |
| 点击放大 |
进一步将13组试验数据回归分析得出最优回归数学模型为:
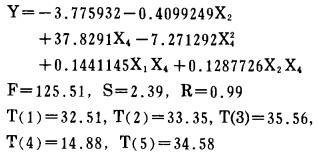
|
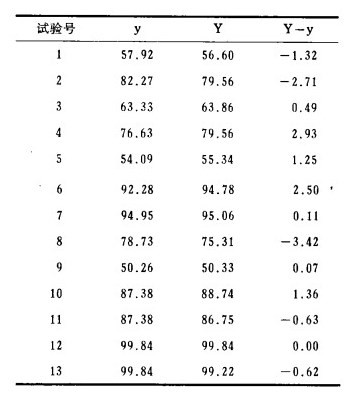
预报值y与实际铜浸出率Y的比较列于表 5, 可见回归数模预报值可信度较大。
| 表 5 铜浸出率预报值y与实际值Y的比较 |
 |
| 点击放大 |
3.3 数学模型解析
基于上述数模,用计算机作模拟计算的结果如附图所示。模拟结果表明:
 |
| 附图 Fe3+浓度、温度及时间对铜浸出率 的影响 |
(1) Fe3+浓度是影响铜浸出率最重要的因素。由于试料中的铜主要以黄铜矿形态存在,且含较高铅锌的特性,FeCl3/CuFeS2高达3.5(即Fe3+/Cu=3.5,或当液固比为4:1时Fe3+浓度为192g/l)方能取得满意的铜浸出率,如低于3.18时,延长浸出时间反而有可能引起铜浸出率呈下降的趋势。
(2) Fe3+浓度与温度和时间之间有交互影响。Fe3+浓度和温度高时,浸出速率更大,浸出时间可相对缩短。
(3) 液固比对铜浸出率影响不大。这可能是液固比增大虽降低了高铁离子浓度,但也降低了矿浆的粘度,改善了扩散条件之故。
3.4 高Fe3+浸出试验| 表 6 高Fe3+浸出试验 结果 |
 |
| 点击放大 |
由表可见在高Fe3+浓度浸出条件下,在更短的浸出时间和稍低的浸出温度时仍然能取得较高的铜浸出率,但是此时浸出液澄清过滤较困难,且铁离子过剩给后一步处理带来诸多不便。
3.5 添加CuCl2对铜浸出率的影响固定浸出条件为105℃、60分钟、FeCl3/CuFeS2=2.1、液固比=5:1,添加CuCl2的浸出试验结果列于表 7。从中可知,添加氯化铜略可提高铜的浸出率,但效果并不显著。
| 表 7 添加CuCl2对铜浸出率的影响 |
 |
| 点击放大 |
3.6 铜、铅、锌、硫等元素在浸出液与浸出渣中的分布
在取得铜浸出率最优的组合条件下,考察了铅、锌、硫、铁等元素的浸出情况(表 8)。结果表明此条件下,铅、锌均达满意的浸出率;原料中的硫氧化为SO42-的量低于4%,即96%以上的硫以元素硫或黄铁矿形态富集于渣中,有利于硫的回收。
| 表 8 原料中铜、铅、锌、硫等元素在浸出液与浸出渣中的分布情况 |
 |
| 点击放大 |
4 结论
(1) 采用三氯化铁直接浸出铜铅锌复合硫化矿的工艺技术是可行的。
(2) 在试验条件范围内,温度(X1)、时间(X2)和FeCl3/CuFeS2(X1)对铜浸出率(Y)的影响可用下面的回归数模来描述:
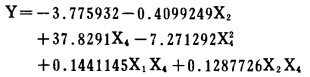
|
搅拌速度、固液比、HCl浓度、加入NaCl或CuCl2等对铜浸出率均无显著影响。
(3) 由于试料中的铜主要以黄铜矿形态存在,且含较高铅锌的特性,应采用较高的Fe3+浓度方能取得满意的金属浸出率;此时相应宜采用偏高的液固比有利于固液的澄清分离。最佳浸出条件为:液固比4:1, Fe3+浓度192g/l, 温度105℃, 时间3小时。此条件下,铜、铅、锌的浸出率分别高达99.5%、98.6%、99.6%; 96%的硫富集于渣中。
(4) 有待于进一步考察贵金属的行为和研究完善全工艺流程。
| [1] |
Ngoc N V. Oxidative Leaching of an Offgrade/Complex Copper Concentrate in Chloride Lixiviants[J].
Metallurgical Transactions B, 1990(4): 611–620. |
| [2] |
马荣俊.
湿法炼铜新技术[M]. 长沙: 湖南科学技术出版社, 1985: 77-109.
|
| [3] |
方开泰, 等.
实用回归分析[M]. 北京: 科学出版社, 1988: 233-273.
|
 1995, Vol. 9
1995, Vol. 9
