| 宜春锂云母采用硫酸盐法制取碳酸锉工艺净化除杂试验 |
宜春锂云母采用硫酸盐法制取碳酸锂工艺流程主要分三个部分。第一部分是原料处理,第二部分是净化沉锂,第三部分是母液回收。净化效果的好坏对产品碳酸锂有决定性的影响。同时净化措施是否合理对锂的收率有较大的影响。本文列出浸出液中的主要杂质φ-pH关系,并将φ-pH关系绘于图上。根据φ-pH图,我们可分析杂质在浸出液中的行为状态。寻找出一条合理的净化除杂途径,并通过实验验证,验证拟定的净化除杂流程是合理的。
1 浸出液中主要杂质φ-pH关系浸出液中除了主成份Li+,还有杂质Fe+3、A1+3、Si+4、Ca+2、Mg+2、Mn2+、F-等。设除杂后溶液中杂质浓度:Fe+3= 10-6mol·l-1. Al+3=10-5mol·l-1、Ca+2=10-3mol·l-1、Mg+2= 10-4mol·l-11、F-=10-3mol·l-1。因缺乏有关SiO2标准电位的数据,未能列出有关SiO2反应φ-pH关系。主要杂质少φ-pH关系如表 1、图 1所示。
| 表 1 浸出液中主要杂质φ-pH关系 |
 |
| 点击放大 |
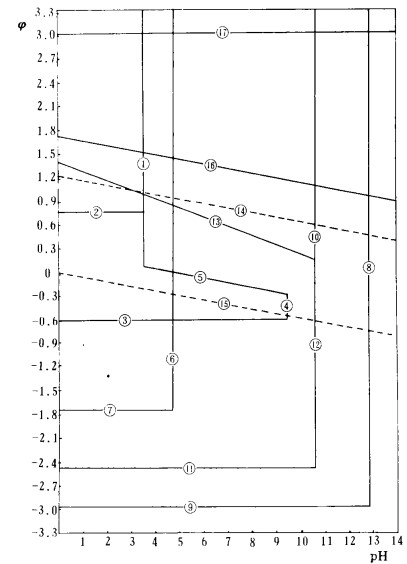 |
| 图 1 杂质-H2O系电位-PH图 |
讨论:a. 分析图 1可知,在浸出液pH = 6.0时,浸出液中杂质Fe+3、Al+3能以氢氧化物沉淀形式被去除。而Fe+2、Mg+2、Ca+2、Mn+2、F-不能被去除。要将Fe+2、Mg+2、Ca+2、Mn+2、以氢氧化物沉淀形式除去需将溶液的pH值升高到一定值。从⑰线知F-不可能用调pH法使其形成氢氧化物沉淀被去除。b.如果将Fe+2氧化成Fe+3、Mn+2氧化成MnO2,那么在pH=6.0条件下,Fe+3形成氢氧化物沉淀而被去除,Mn+2形成MnO2沉淀而被去除。C.从⑯线、⑬线、②线知道ClO-能够将Fe+2氧化成Fe+2, Mn+2氧化成MnO2。
2 净化除杂流程根据φ-pH图并结合实际,拟定浸出液的净化除杂综合流程,见图 2。
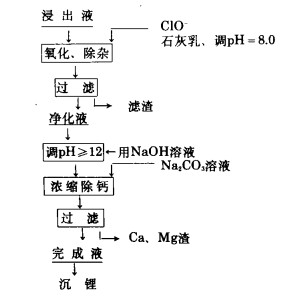 |
| 图 2 浸出液净化除杂综合流程 |
按照上述流程将浸出液进行净化除杂,最后沉锂。碳酸锂产品经化验分析,产品均是零级品。试验结果说明净化除杂流程是可行的。
3 结论宜春锂云母采用硫酸盐法制取碳酸锂工艺净化除杂过程中一次性净化不可能将所有杂质去除;净化除杂必须分步进行,首先除去Fe+3、Al+3、Mn+2、F-、Si+4而后除去Ca+2、Mg+2。按照拟定的流程,可将浸出液中大部份杂质去除,使沉锂产品质量达到零级品的要求。
 1995, Vol. 9
1995, Vol. 9
