| 从磷灰石精矿提纯混合氧化稀土 |
本技术方法把初加工原料和非稀土元素的分离进行结合处理以制取混合氧化稀土。原料的性质、元素性质及相组分不同确定了使用的工艺方法。
其实,从磷灰石生产稀土是用硝酸浸取磷灰石。从硫酸加工磷灰石的废产品制取稀土元素的方法虽有过报道,但目前少用,这就是为何不系统地研究该方法对所获精矿(具有一定的特点)作深加工的原因。
自从保加利亚进行了某些精矿实验性生产以来,作者研究了各种沉淀方法的效果(从中可能选择一种处理其原料的方法)。以便从精矿中除去非稀土元素。其目的是建立一套生产混合氧化稀土的流程。研究工作限于探求精矿在HCl和HN03中溶解。
提纯稀土精矿的几种方法已作过综述。为了从稀土精矿的硝酸溶液中分离钙,一种以冷却结晶Ca(N03)•4H2O为基础的方法已见报道。直接处理磷灰石矿,通过用NaOH进行团矿并取稀HNO3洗涤矿饼提取稀土元素。Ca、Ba、Si和某些金属的分离靠添加对苯二酸盐沉淀稀土来完成。由于稀土氢氧化物与碱土金属氢氧化物沉淀所需的pH值不同,通过水解沉淀可以提纯稀土,提纯的效率可由后面加柠檬酸盐沉淀稀土来提髙。
为了分离Sr,(它以难溶的SrSO4沉淀)必须附加额外的提炼过程把沉淀的稀土元素分离。
混合氧化稀土中含的硅,使以后提取单个稀土元素时极为困难。按Parkhomenko报告,试样中的F和Si能以Na2SiF6分离。酸溶液中的Si以胶体形态存在,可用煮沸30分钟除去。这是以减少约20%产生悬浮的液相体积来实现的。
有许多处理稀土精矿的方法,其中包括草酸沉淀稀土元素工艺,确保了与某些过渡金属,Cl和P分离。
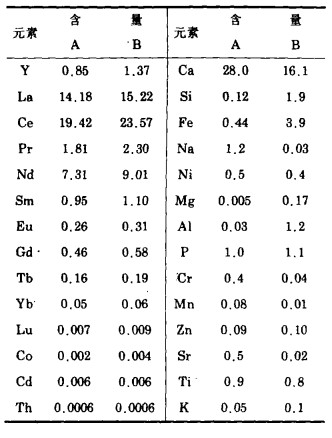
1 实验 1.1 原料研究工作用的精矿取自EoRedmet的试验组合物,并以含有杂质磷的氢氧化物产品或(比较少)以草酸制品交付使用,草酸物质应在其溶解前灼烧,以保证转变为氧化物。表 1示出两种精矿在800~850℃加热3小时的成份。产品A是处理磷石膏得到,产物B由加工磷酸获得。
| 表 1 火焰燃烧的矿物成分 |
 |
| 点击放大 |
1.2 分析
稀土与硅含量用偶感应离子发射光谱分析仪测定;其它的元素用原子吸收分析仪测定。
1.3 溶解氢氧化物在稀酸中溶解并不十分困难。
氧化矿在HNO3中溶解时加入H2O2(6%的体积浓度)是为了使介质减少并让Ce溶解。
1.4 不完全水解沉淀氢氧化物不完全沉淀按如下方法进行:
a 把10%的NH4OH加入到搅拌着的酸液中,直到达到要求的pH值为止。1小时后,沉淀物过滤,并用水洗涤。
b 空气-稀氨气泡(1:10氨:空气体积比)在未达到要求的pH值前于室温下缓慢通过溶液(Tromble法[12])。用该法制备的水解产物具有良好的吸附性质。
1.5 完全水解沉淀母液含135克/升稀土(氧化物)和90克/升NH4N03。把溶液加热至沸点以下,边搅拌边极缓慢地加入12%NH4OH, 直至达到所需的pH值。把悬浮物冷却(连续搅拌)3小时再分离。用本方法得到的沉淀物作离心分离,而该类沉淀物相当容易洗涤。
1.6 草酸沉淀硝酸盐母液HN03相对含量为2M, 沉淀过程在60℃进行,边搅拌边加入饱和H2C2O4溶液,一直加到超过化学计量式要求量的5%为止。沉淀物至少陈化6小时后过滤。并用1%的稀草酸洗涤,但第二次洗涤用热水。
2 结果及讨论 2.1 溶解溶解进度由酸浓度与酸量、温度与处理时间确定。过剩的酸量必须中和,在按步深加工过程中,选择工艺参数特别重要。据此选定了示于图 1的参数。固相与100%酸的质量比为:HNO31:3;对HNO3+H2O2为1:3.5;HCl为1:4。在这些条件下,确保了溶解达98%以上。
留下的不溶部分(原矿质量的1~5%)可作各种用途如冶金添加剂。
2.2 碱金属及碱土元素提纯研究了水解沉淀的效率,以便从碱金属和碱土金属中分离稀土元素。
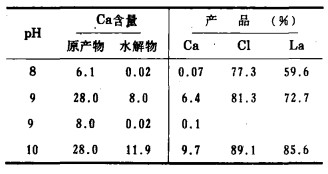
实质上的问题之一是沉淀的最佳pH值。它是稀土生产要求的上限值与非稀土成份共沉淀的下限值之间取折衷值。表 2给出满足生产要求的pH≥9.5。母液中Ca含量高,得到的水解沉淀物不能含高Ca量。现在是从磷石膏中进行制取稀土精矿的情况,在这种情况下,必须把氢氧化物溶解于HCl或HNO3后进行二次水解沉淀。
| 表 2 水解沉淀稀土 |
 |
| 点击放大 |
可以预计,水解沉淀使Na、K、Mg及Ba除去(在pH9.4以Mg(OH)2态沉淀)。
草酸沉淀也有利于这些元素的提纯作用,因为草酸生成溶解性介质,并使草酸钙和镁在酸性介质中溶解度增大。洗涤氢氧化物和草酸沉淀很有必要.因为它将减少Ca和Mg的含量。
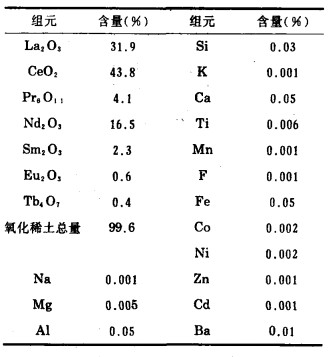
在混合稀土矿中得到的碱金属和碱土元素示于表 3。
| 表 3 混合氧化稀土最后成份 |
 |
| 点击放大 |
从某些过渡元渡(Cl元素)提纯
草酸沉淀稀土是脱除某些过渡元素的有效方法,虽然草酸沉淀用得广泛,但特别引人注目的是实验包括的细节。
本试验结果证明,超量的H2C2O4对除Cr(Ⅲ)和Fe(Ⅲ)以及Zr、Al、Nb、Ta、和U022有利,形成可溶性的草酸络合物。同时,增加酸度,草酸Mn、Cu、Pb、Ni、Zn、Co和Cd的溶解度增加,有利于除去这些元素。
然而, 酸性太强和H2C2O4过剩多能引起Lu2(C2O4)3下降;这又与可溶性草酸络合物的生成有关,按此考虑,我们采用了在实验部分所述的沉淀加工的参数并示于图 1。
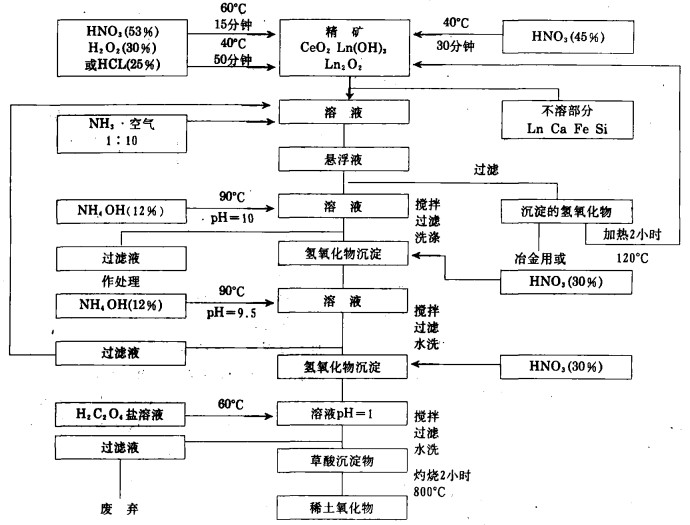 |
| 图 1 工艺流程 |
可以增加氧化介质中进行的沉淀过程(保证Fe的高氧化程度),升高温度并把沉淀物陈化6小时以上,上面两点对较简易的离心和更有效地洗涤沉淀物是重要的。
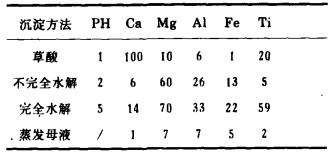
表 4示出,溶液中一些杂质转化为草酸沉淀物的百分比,其稀土产物为98%。
| 表 4 从溶液沉淀的杂质量 |
 |
| 点击放大 |
稀土氢氧化物完全沉淀以前, 不完全水解沉淀的颗粒还含有脱除的Fe、Cr、Th、Al、Ti和一定量Cd、Co, Mn、Ni和Zn。
不完全水解沉淀后得到的沉淀物含稀土母液中5~10%的稀土(与pH有关)。该沉淀物含67%稀土、10%以上Fe、2.2%Si及大约0.8%其它非稀土元素。本方法的成功性可由示于表 4的数据加以证明。
用NH3和空气沉淀取得了较好的结果,这就是把该沉淀法用于工艺流程的原因。
稀土元素的完全水解沉淀关系到除Mg和Co, 因其形成可溶性络合物。
液相蒸发,拌有25%的体积减少.使沉k物的组成含约2~3%的稀土元素和杂质。
正如表 4所示,本工艺对分离碱土金属和元素并非十分凑效。
除Si
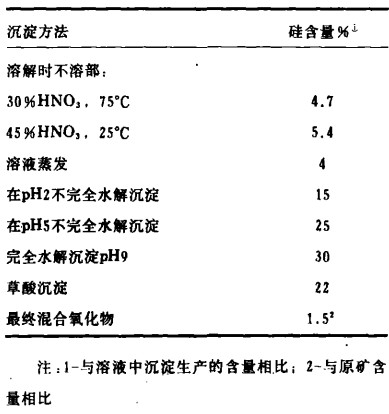
表 5包括了除硅研究的有关数据,用以研究除Si工艺的功效。很明显,蒸发母液不会带去大量的硅,这就说明把脱硅工序引入常规流程制取稀土是合理的(应该想到在某种情况下,含Si沉淀物也是由留在母液中的精矿,放8~10小时不加热生成的)。
| 表 5 用各种工艺方法共沉淀的硅 |
 |
| 点击放大 |
不完全水解沉淀是较好的脱Si方法。严格按上述工艺对于以最少的稀土元素损失获取最大的提取效果极为重要。得到的沉淀物能用在某些用途,也能把其加入原料中在处理加工时再次回收。在此情况下,沉淀物应在120℃以上先加热烘干。这会引起脱水和少量硅在其后的酸溶时溶解。
本论证研究提出了一套生产流程,由硫酸处理磷灰石副产品中获取的精矿生产混合稀土(如图 1所示)。从产物B得到的混合稀土氧物的成份见表 3。产品可直接生产铈稀土合金,或通过后续处理制取纯稀土元素。
 1992, Vol. 6
1992, Vol. 6
