| 铜矿石中微量镓的测定 |
随着科技进步,镓的用途越来越广泛,尤其是高技术领域中更加显得重要。如电子计算机磁泡储存器,光电倍增管,大功率激光器,微波通讯,红外技术,太阳能电池等。镓的分析方法也日渐增多,但铜矿石中微量镓的测定却很少报导。
1 主要试剂a 镓标准液。称取优级纯三氧化二镓0.0269g于200ml烧杯中,加6M盐酸15ml,于水浴上溶解完全,取下冷却用6MHCL移入200ml容量并中并稀至刻度。此液1ml含0.1mg镓,取上述(甲)标液10ml于1000ml容量并中,用6MHCL稀至刻度摇匀,此液1ml含1μg镓。
b 0.5%罗丹明B溶液。称2.5g罗丹明B试剂溶于6MHCL,滤入500ml容量并中,用6MHCL稀至刻度摇匀。
c 分析纯乙醚。市面上出售的乙醚,一般含有少量过氧化物对罗丹明B有破坏,需经如下处理:于125ml分液漏斗中,加6M盐酸25ml,加0.6g无水亚硫酸钠,加乙醚65ml振荡萃取1分钟,将乙醚贮于棕色玻璃瓶。
d 苯(分析纯)。经如下处理备用:于500ml分液漏斗中加200ml分析纯苯再加2.5N H2SO4(内含2%KI,1%硫脲)100ml,萃取1分钟,弃水相再用蒸馏水洗苯三次,弃水相贮存。
e 15%三氯化铁(1:1盐酸)液,分析纯。
2 主要试验a 镓-罗丹明B络合物吸收曲线:取1ml含1ug镓的标准液0、1ml、2ml,于25ml比色管中,用1:1Hcl稀至15ml加15%三氯化钛2ml,0.5%罗丹明B2ml摇匀再加10ml苯-乙醚(3:1)混匀萃取剂摇动1分钟萃取,静置分层后,取有机相于1cm比色皿中72型光度计上,于不同波长下测吸光度,有如下吸收曲线。
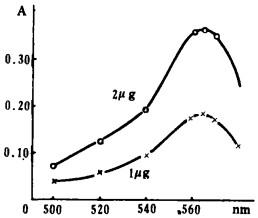 |
| 图 1 吸收曲线 |
由图可知,镓-罗丹明B络合物在564nm处有最大吸收峰,故选用波长564nm。
b 显色酸度通过试验,发现有如下曲线。
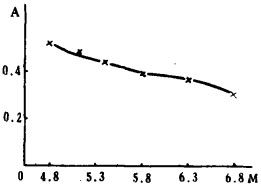 |
| 图 2 显色酸度对络合物吸光度影响 |
由图可知:溶液酸度在5.4~6.3M范围内吸光度曲线平缓,变化较小,故以6.0M盐酸酸度为宜。
c 镓-罗丹明B络合物稳定性试验;
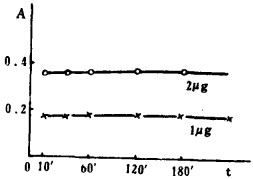 |
| 图 3 稳定性曲线 |
试验发现此络合物较稳定,显色后四小时内吸光度变化很小,为测定带来了方便。
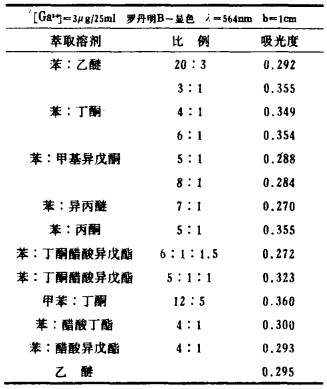
d 萃取溶剂的选择:按照镓-罗丹明B络合物吸收曲线绘制步骤显色后,用不同的溶剂萃取,测其吸光度,试验数据如下:
上述数据都是各萃取溶剂的最好结果,从上可看出:在不考虑干扰元素影响的情况下,苯-乙醚、苯-丙酮、甲苯-丁酮等混合溶剂对镓-罗丹明B络合物萃取较为有利,根据我们的实际情况,我们选用苯-乙醚为萃取溶剂。
| 表 1 萃取效果 |
 |
| 点击放大 |
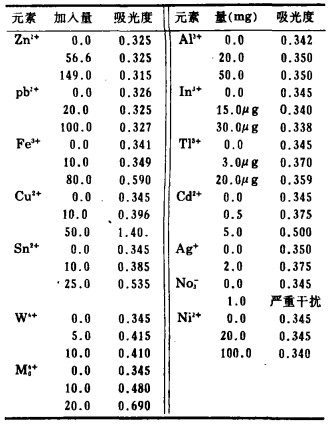
e 其他元素的干扰。据光谱分析,铜矿石中主要含有Cu、Fe、Zn、iS、Al及少量Pb、Bi、As等。笔者认为,凡在盐酸溶剂中能形成阴离子或络阴离子的元素都能生成离子缔合物或者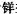
f 标准曲线 取镓标准液0、1.0、2.0、3.0、4.0、5.0、6.0、8.0、10.0μg于125ml分液漏斗中,用6m的盐酸释至30ml,滴加TiCl3呈紫红色并过量2ml,加30ml乙醚萃取一分钟,分层后,水相放入另一分液漏斗中,再加30ml乙醚萃取一分钟,两次乙醚合并,用6m盐酸(乙醚饱和过)10ml两次洗醚层,乙醚加入100ml干烧杯中于水浴上驱除乙醚,取下加硝酸1ml硫酸(1:1)1ml于电热板上蒸至冒硫酸烟尽,取下,加6m盐酸溶解,冷却后用6m盐酸移入25ml比色管中,用6m盐酸稀至10ml,加TiCl32ml,0.5%罗丹明B2ml,加苯-乙醚(3:1)萃取溶剂10ml萃取一分钟,静置分层后,取有机相于72型分光光度上,564nm波长,1cm比色皿测吸光度。
| 表 2 其它元素干扰 |
 |
| 点击放大 |
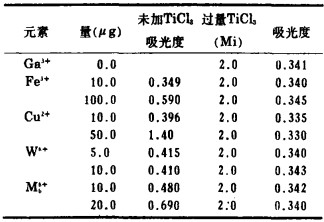
| 表 3 过量TiCl3消除干扰情况 |
 |
| 点击放大 |
0~8ugGa/25ml符合比耳定律。
3 分析步骤及结果称样0.5000g于予先放有4gNaOH的镍坩锅中,加4g过氧化纳,在喷灯上焙坍至熔液出现亮红色过半分钟取下,稍冷,放入300 ml烧杯中,用50ml热水浸取,洗净坩埚,加20ml浓盐酸酸化,加1:1硫酸5ml在电热板上蒸至冒烟尽,冷却,加入6m盐酸15ml溶解其盐类,并用6m盐酸移入125ml分液漏斗中控制体积30ml,加TiCl3还原至呈紫红色并过量2ml,加30ml乙醚萃取一分钟(以下同标准曲线绘制的步骤。)
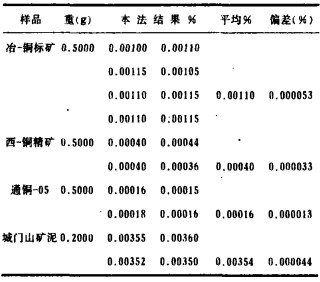
笔者多年来采用此方法进行了大量样品的分析、并承担了部分外单位委托任务,结果较为满意。
| 表 4 分析结果 |
 |
| 点击放大 |
| [1] |
秦中骏, 周剑林. [J].
岩石矿物及测试, 1984, 3(4): 367.
|
| [2] |
陈玉绶, 等. [J].
福州大学学报, 1984(2): 119.
|
| [3] |
傅瑞祥. [J].
冶金分析与测试, 1985, 5(2): 28.
|
| [4] |
吴润身. [J].
分析化学, 1985, 13(8): 611.
|
| [5] |
黄运英. [J].
冶金分析, 1986, 6(4): 67.
|
 1991, Vol. 5
1991, Vol. 5
