| 硫化铅还原硫酸浸出锌电解阳极泥中二氧化锰的试验研究 |
2. 株洲市湘麒资源综合利用研究所, 湖南 株州 412005
2. Xiangqi Research Institute for Comprehensive Utilization of Mineral Resources, Zhuzhou 412005, China
锌电解阳极泥的主要成分是二氧化锰.湿法炼锌厂一般都是将以二氧化锰为主要成分的锌电解阳极泥返回到锌浸出工序,其目的之一是使其中的氧化锰起到氧化剂的作用,有利于提高焙砂中部分难浸硫化锌矿物的浸出率[1], 目的之二是有利于除掉浸出液中过多的铁, 提高电锌质量[2], 目的之三是使固态的氧化锰还原为液态的硫酸锰并进入到电解工序后,对铅银合金阳极板起到保护作用,减缓阳极板的腐蚀溶解速度,延长阳极板的使用寿命[3].株洲冶炼厂的电解锌阳极泥中含有较高的铅和银.如果将以二氧化锰为主要成分的锌阳极泥返回到锌浸出工序,锌阳极泥中的铅和银将随之进入到锌浸出渣中.株冶对锌浸出渣设有浮选银的工序,只可回收到一部份银[4-6].再对浸出渣通过进行转窑还原焙烧,铅主要进入到次氧化锌产品中,在对次氧化锌进行再加工的同时可附产铅渣,再返回铅冶炼系统回收铅.但银主要残留在窑渣中.进入到窑渣中的银只有一部分可随着铁被选为铁精矿,作为添加剂加入到火法炼铅炉中而得到回收,大部分银无法回收.随着有色金属和贵金属的价值不断提高,铅和银含量较高的电解锌阳极泥中铅和银的高效回收问题已引起了人们的高度重视,将锌阳极泥在返回浸出工序之前分离回收其中铅和银,以实现铅和银的早收, 避免铅和银损失在浸出渣中,是一条提高铅银综合回收率的重要技术路线.
当前国内对铜、铅、锡等电解阳极泥的综合利用开展了大量的研究工作,但对锌阳极泥开展的研究文献报道较少.国内文献只有3篇是锌阳极泥利用方面的文章,均是采用硫酸还原浸出MnO2的工艺,其中之一是王淼生等人采用褐煤还原焙烧[7],之二是廖云军等人采用ZnS精矿做还原剂[8],另一篇是沈慧庭等人采用玉米秆的硫酸水解液做还原剂[9].浸取锰后的铅银渣配入硫化铅精矿进行火法熔炼回收铅银.而关于MnO2的直接还原浸出方面的文献报道较多,采用硫酸浸出的还原剂有海绵铁[10], 黄铁矿[11-12]、闪锌矿[13-14]、SO2[15-16]、有机物[17-20]等,采用方铅矿做还原剂的文献均是采用稀HCl[21-22]或稀HNO3[23]浸出工艺.本研究采用方铅矿做还原剂在稀硫酸溶液中还原浸出二氧化锰的技术路线,实现锌电解阳极泥中的二氧化锰与硫酸铅和银的分离.含锰离子的浸出液可以返回电锌生产系统,也可用来生产硫酸锰、碳酸锰等锰制品,含铅银的浸出渣可以配入硫化铅精矿入炉冶炼,使浸出渣中的铅银得到综合利用.
1 实验 1.1 试验物料试验用的锌电解阳极泥取自株冶电解锌车间.化学分析和原子吸收分析结果表明,该物料含有34.60%锰,16.10%左右的铅,1250g/t银;3.73% H2SO4, 1.83%水溶锌,0.87%水溶锰.XRD的衍射分析(图 1)表明,锰主要以KMn8O16形式存在,铅主要以PbSO4形式存在.
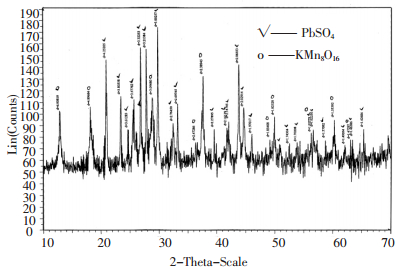 |
| 图 1 锌阳极泥综合样XRD衍射图谱 |
用0.149mm筛对以上锌阳极泥样进行控制筛分干式研磨,让全部通过0.149mm筛,做浸出试验原料.条件试验用还原剂PbS采用纯方铅矿样,取自水口山铅锌矿,化验含Pb 79.26%,S 12.68 %,Zn 0.46%,Fe 0.33%,Ag 1290g/t.研磨并用各种规格的标准套筛控制PbS样的粒度.
200g锌阳极泥样的扩大验证试验采用硫化铅浮选精矿样做还原剂.试验采用了3种铅和锌品位不同浮选铅精矿样,化验结果分别是:
1号:Pb 55.8%,锌6.48%,Fe 6.06 %,Ag 979g/t,S 13.69%;
2号:Pb 50.2%,锌11.14%,Fe 2.23 %,Ag 235g/t,S 15.57%;
3号:Pb 35.8%,锌27.97%,Fe 3.10 %,Ag 160g/t,S 20.26%.
1.2 试验方法浸出条件试验每次称取20 g-0.149mm电解锌阳极泥样,在恒温水浴中的300 mL高型烧杯中开展浸出试验,对PbS的细度、PbS的用量(PbS:MnO2摩尔比)、硫酸用量(H2SO4:MnO2摩尔比)、反应温度和反应时间等对二氧化锰浸出的影响开展了详细的条件试验.浸出试验结束后通过抽滤进行固液分离,对得到的滤液计量体积,化验滤液中Mn2+的含量(g/L), 对得到的滤渣烘干后称重,制样化验Mn的含量(%).按照下式计算锰的浸出率η:

|
(1) |
按照条件试验得到的最佳工艺条件,对200g -0.149mm锌阳极泥样在恒温水浴中的3000ml烧杯中开展4组扩大验证试验,使用的PbS还原剂在试验A、B、C中分别采用1号、2号和3号浮选铅精矿,在试验D中采用0.037~0.074mm纯方铅矿.浸出试验结束后通过抽滤进行固液分离,对滤液计量体积并取样化验滤液中的Mn2+含量,对滤渣计量干矿重量,并取样化验Mn、Pb和Ag的含量,再按照式(1)计算锰浸出率.
2 试验结果与讨论 2.1 PbS的细度和用量对锰浸出率的影响图 2给出了不同细度的PbS颗粒在不同的PbS: MnO2摩尔比条件下得到的锰浸出率的变化曲线.从图 2可得到如下两个重要结论:
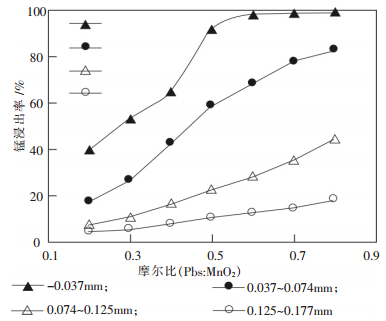 |
| 图 2 PbS的细度和PbS:MnO2摩尔比对锰浸出率的影响 |
(1) PbS的颗粒越细,锰的浸出率越高.对0.125~ 0.177mm的粗粒级来说,锰的最大浸出率低于20%,而对于-0.037mm细粒级来说,锰的最大浸出率已超过了90%.这是因为硫化铅还原二氧化锰的化学反应速度与PbS颗粒的总表面积有关,PbS颗粒越细,PbS颗粒的总表面积就会越大,反应速度就会越快.
(2) 随着PbS:MnO2摩尔比从0.2增加到0.8,锰的浸出率由低变高.对于-0.037mm细粒级来说,当PbS:MnO2摩尔比为0.5左右时,锰的浸出率已超过了90%;对于0.037~0.074mm粒级来说,当PbS:MnO2摩尔比达到0.8时,锰的浸出率已超过了80%.因此,后续试验均采用0.037~0.074mm粒级纯PbS样.
2.2 硫酸用量对锰浸出率的影响图 3给出了选用0.037~0.074mm方铅矿样在PbS:MnO2摩尔比0.8,90℃反应2h的条件下开展的硫酸用量对锰浸出率的影响试验结果.当硫酸:二氧化锰摩尔比0.5时,锰浸出率只有35%,当硫酸:二氧化锰摩尔比为1时,锰浸出率升高到65%左右;再继续增加硫酸用量,锰浸出率缓慢升高,当硫酸:二氧化锰摩尔比为3左右时,锰浸出率到达最高值.
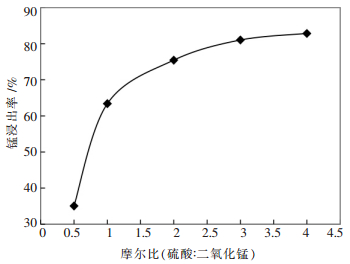 |
| 图 3 硫酸用量对锰浸出率的影响 |
2.3 反应时间和反应温度对锰浸出率的影响
图 4给出了选用0.037~0.074mm方铅矿样在PbS:MnO2摩尔比0.8,H2SO4:MnO2摩尔比3的条件下浸出反应时间和温度对锰浸出率的影响.显然,在反应时间相同时,反应温度越高,锰的浸出率越高;在反应温度相同时,随着反应时间的延长,锰浸出率逐渐升高.在保持2h浸出时间条件下,达到90℃温度后再增加反应温度,锰浸出率增加幅度不大,在保持浸出温度90℃条件下,反应2h后再增加浸出时间,锰浸出率增加幅度同样不大.因此,最佳浸出条件为90℃下浸出2h.
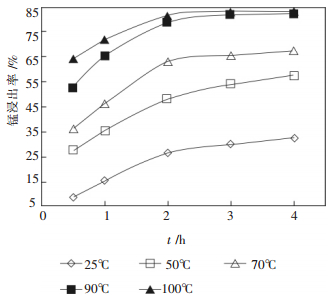 |
| 图 4 浸出反应时间和反应温度对锰浸出的影响 |
2.4 200g锌阳极泥样的放大验证试验
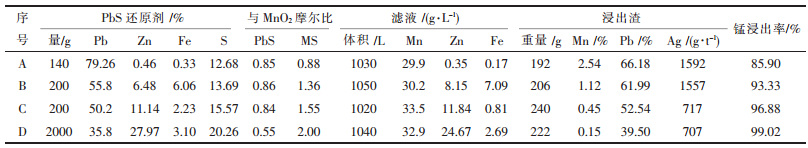
表 1为200g-0.149mm锌阳极泥样用0.037~0. 074mm纯方铅矿样和3个品位不同的硫化铅浮选精矿样在以上条件试验得到的最佳条件(PbS:MnO2摩尔比>0.5,H2SO4:MnO2摩尔比3,在90℃反应2h)的条件下开展的放大验证试验结果.
| 表 1 200g锌阳极泥样PbS精矿还原硫酸浸出试验结果 |
 |
| 点击放大 |
表 1结果表明,采用相同重量的硫化铅浮选精矿,当PbS精矿样含铅较低时,其锌和铁含量就会较高,获得的锰浸出率较高,但获得的浸出渣含铅较低, 浸出液中含Zn2+、Fe2+等杂质也较多.因此,如果要使浸出液含锌铁等杂较少,以更利于生产高纯锰产品,同时又要使浸出渣的含铅品位也较高,有利于返回参与硫化铅入炉料配矿,宜采用高品位铅精矿做还原剂.
从表 1结果还可见,试验A、试验B、试验C计算的PbS:MnO2摩尔比均为0.85%左右,但三者按样品中S含量计的MS:MnO2摩尔比差别较大,试验A的MS:MnO2摩尔比值最小(为0.88),试验A的锰浸出率值最低,为85.90%,而试验C的MS:MnO2摩尔比值最高(为1.55),该试验的锰浸出率值最高,为96.88%.这说明了硫化铅以外的其它硫化矿物在起协同浸出作用.试验D进一步说明了硫化铅以外的硫化矿物的协同浸出作用,因为在该试验中虽然采用的PbS:MnO2摩尔比为几个对比试验的最低值(0.55),但MS:MnO2摩尔比值为4个试验中的最高值(2.0),因而该试验获得的锰的浸出率最高,达到了99.02%.
3 硫化矿协同浸出过程机理探讨锰的浸出率记为a, 在50℃、70℃和90℃ 3个温度条件下, 以1-(2/3)a-(1-a)2/3对时间t作图,得图 5.
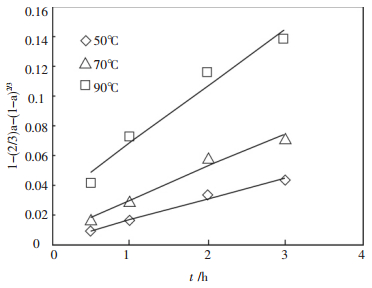 |
| 图 5 不同温度下1-(2/3)a-(1-a)2/3与时间t的关系 |
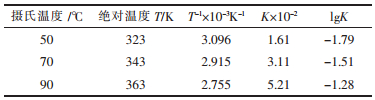
由图 5可见,在不同温度下1-(2/3)a-(1-a)2/3对时间t大致成线性关系,各直线的线性回归斜率k代表该直线温度下的表观速率常数,并计算出不同温度T下的lgK值,见表 2.
| 表 2 不同温度T下的K与lgK值 |
 |
| 点击放大 |
将不同温度下的lgK对1/T作图,得到图 6.由图 6可见,lgK对1/T呈线性关系,线性回归直线斜率f=-1.4967.由此求得试验条件下浸出表观活化能E 表(方铅矿)= -2.303Rf =28.63 kJ /mol.而文献中方铅矿与软锰矿在稀硝酸溶液中反应的表观活化能值为13.14 kJ /mol[23],造成本试验中方铅矿与软锰矿反应的表观活化能较大的原因可能是因为在本试验中产生的硫酸铅沉淀附着在方铅矿表面上,在一定程度上阻碍了电子的传递,影响了反应的进程.
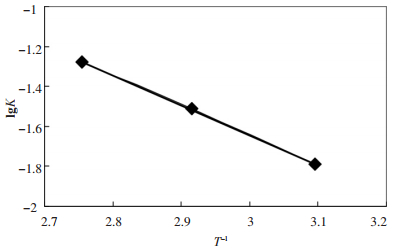 |
| 图 6 lgK与T-1 的关系 |
李军旗研究得到闪锌矿与软锰矿在硫酸溶液中同时浸出机理的表观活化能E 表(闪锌矿)=83.40 kJ /mol[14],与本研究得到的E 表(方铅矿)=28.63 kJ /mol相比,方铅矿的表观活化能低,其与二氧化锰的反应速度要比闪锌矿与二氧化锰的反应速度快,并优先进行.王少芬研究[24]各硫化矿与FeCl3体系发电浸出过程得到各硫化矿的发电浸出表观活化能分别为:E 表(PbS)=18.26kJ/mol、E 表(方铅矿)=14.96kJ/mol/、E 表(ZnS)=21.22kJ/mol、E 表(闪锌矿)= 25.66kJ/mol, 在该体系得到的结果与本研究中的软锰矿硫酸浸出体系相似,方铅矿(或PbS)的表观活化能也低于闪锌矿(或ZnS), 也说明方铅矿发生氧化的反应速度快于闪锌矿,方铅矿的反应为优势化学反应.
李军旗的研究[14]还指出,黄铁矿与闪锌矿共存时,由于形成了“迦伐尼”电偶的缘故,黄铁矿受到阴极保护,闪锌矿优先参与反应,但黄铁矿的存在对闪锌矿和软锰矿的同时浸出过程有催化作用.因此,当方铅矿、闪锌矿和黄铁矿共存时,PbS会优先参与反应,当PbS反应到一定程度,因其表面吸附覆盖反应产物PbSO4沉淀阻止内部PbS继续反应时,ZnS就会又优先于FeS2出来参与反应,最后才是FeS2的反应.但ZnS和FeS2的存在对PbS与二氧化锰的氧化还原反应有催化作用,或协同促进浸矿作用.
4 结论本研究采用硫化铅做还原剂在硫酸溶液还原浸出锌电解阳极泥中二氧化锰,实现了锰与铅银的分离.通过试验得到以下基本结论:
(1) 采用的还原剂PbS样的细度、PbS:MnO2摩尔比、H2SO4:MnO2摩尔比、浸出反应时间和温度等都对二氧化锰的还原浸出效率有很大的影响.采用的PbS样品颗粒越细,比表面积越大, 与二氧化锰接触的表面积就会越多,反应速度就会越快;试验获得较佳的条件为PbS:MnO2摩尔比>0.5,H2SO4:MnO2摩尔比>3, 浸出反应温度>90℃,时间>2h.在较佳条件下用0.037~0.074mm纯方铅矿样做还原剂可获得锰浸出率85%以上的试验指标.
(2) 实际浮选PbS精矿样比纯方铅矿样含有较多的硫化锌和硫化铁等硫化矿物,由于这些硫化矿物的协同还原浸出作用,使得使用实际浮选PbS精矿样做还原剂时锰的浸出效果优于使用纯方铅矿样.用实际硫化铅浮选精矿样做还原剂, 温度90℃, 时间2h, 可获得锰浸出率93%~99%以上的试验指标.
(3) 采用的PbS精矿样含铅越低,含锌越高,获得的锰浸出率越高,但获得的浸出渣含铅较低,浸出液含锌铁等杂质金属也较多.因此,宜采用高品位铅精矿做还原剂,此时,浸出液含杂较少,有利于生产高纯锰产品,浸出渣的含铅品位也较高,有利于返回参与硫化铅入炉料配矿.
| [1] |
赵永, 蒋开喜, 王德全, 等. 添加锌电解阳极泥对ZnS浸出过程的影响[J].
东北大学学报:自然科学版, 2006, 27(1): 61–64.
|
| [2] |
关亚君. 锌阳极泥过量对电锌酸浸影响的理论探讨与改进实践[J].
湖南有色金属, 2006, 22(3): 25–27.
|
| [3] |
彭小苏. 锌电解阳极电积MnO2的研究[J].
有色金属(冶炼部分), 2001, 3: 2–4.
|
| [4] |
黄开国, 王秋风. 从锌浸出渣中浮选回收银[J].
中南工业大学学报:自然科学版, 1997, 6: 530–532.
|
| [5] |
张万生. 锌浸出渣浮选银生产实践[J].
湖南有色金属, 2000(S1): 86–90.
|
| [6] |
倪恒发, 张小虎, 张全胜. 从锌浸出渣中浮选回收银的实践[J].
资源再生, 2008(2): 28–29.
|
| [7] |
王淼生, 郑团, 周继刚. 锌阳极泥制取碳酸锰的研究[J].
广东有色金属学报, 1997, 7: 125–130.
|
| [8] |
廖云军, 梅光贵, 刘荣义. 锌电解过程中减少锰离子贫化及对阳极泥返回利用的研究[J].
中国锰业, 1999, 19(1): 33–36.
|
| [9] |
沈慧庭, 覃华, 黄晓毅, 等. 某含锰冶金渣中锰和铅的综合回收研究[J].
金属矿山, 2009(6): 171–175.
|
| [10] |
Bafghi M S, Zakeri A, Ghasemi Z, Adeli M. Reductive Dissolution of Manganese Ore in Sulfuric Acid in the Presence of Iron Metal[J].
Hydrometallurgy, 2008, 90(2-4): 207–212. DOI: 10.1016/j.hydromet.2007.07.003. |
| [11] |
袁明亮, 邱冠周. 软锰矿直接还原浸出的研究[J].
矿产综合利用, 2000, 5: 4–7.
|
| [12] |
黄佩芳, 马集成, 滕英才. 硫铁矿和锰矿浓硫酸熟化法生产硫酸锰[J].
广西大学学报:自然科学版, 2002, 27(1): 39–41.
|
| [13] |
Pande A M, Gupta K N, Altekar V A. Single Cell Extraction of Zinc and Manganese Dioxide from Zinc Sulphide Concentrate and Manganese ores[J].
Hydrometallurgy, 1982, 9(1): 57–68. DOI: 10.1016/0304-386X(82)90053-6. |
| [14] |
李军旗. 硫化锌精矿和软锰矿同时浸出机理[J].
有色金属, 1996, 48(2): 90–93.
|
| [15] |
Kanungo S B, DAS R P. Extraction of Metals from Manganese Nodules of the Indian Ocean by Leaching in Aqueous Solution of Sulphur Dioxide[J].
Hydrometallurgy, 1988, 20: 135–146. DOI: 10.1016/0304-386X(88)90047-3. |
| [16] |
Abbruzzese C. Percolation Leaching of Manganese Ore by Aqueous Sulfur Dioxide[J].
Hydrometallurgy, 1990, 25(1): 85–97. DOI: 10.1016/0304-386X(90)90066-B. |
| [17] |
Veglio F, Toro L. Fractional Factorial Experiments in the Development of Manganese Dioxide Leaching by Sucrose in Sulphuric Acid Solutions[J].
Hydrometallurgy, 1994, 36(2): 215–230. DOI: 10.1016/0304-386X(94)90007-8. |
| [18] |
Momade F W Y, Momade Zs G. Reductive Leaching of Manganese Oxide Ore in Aqueous Methanol Sulphuric Acid Medium[J].
Hy -drometallurgy, 1999, 51(1): 103–113. |
| [19] |
Sahoo R N, Naik P K, Das S C. Leaching of Manganese from Lowgrade Manganese Ore using Oxalic Acid as Reductant in Sulphuric Acid Solution[J].
Hydrometallurgy, 2001, 62(3): 157–163. DOI: 10.1016/S0304-386X(01)00196-7. |
| [20] |
Ismail A A, Ali E A, Abrahim I A, Ahmed M S. A Comparative Study on Acid Leaching of Low Grade Manganese Ore Using Some Industrial Wastes as Reductants[J].
The Canadian Journal of Chemical Engineering, 2008, 82(6): 1296–1300. DOI: 10.1002/cjce.5450820618. |
| [21] |
徐本军, 覃文庆, 邱冠周. 方铅矿和软锰矿两矿法浸出工艺的研究[J].
矿产保护与利用, 2005(3): 29–33.
|
| [22] |
唐尚文. 用闪锌矿(方铅矿)精矿催化还原软锰矿(大洋锰结核矿)制取硫酸锰[J].
无机盐工业, 2005, 37(6): 46–49.
|
| [23] |
胡全红, 刘坚, 屈芸. 方铅矿的两矿法浸出动力学研究[J].
矿冶工程, 2007, 27(4): 61–63.
|
| [24] |
 2010, Vol. 24
2010, Vol. 24
