2. 潍坊市市政工程设计研究院有限公司, 山东 潍坊 261061;
3. 临沂市阳光热力有限公司, 山东 临沂 273411
2. Weifang Municipal Engineering Design Research Institute Co. Ltd., Weifang, Shandong 261061, China;
3. Linyi Yangguang Heating Power Ltd., Linyi, Shandong 273411, China
蒸汽热采是开采稠油行之有效的方法之一,通过向油藏中注入高温蒸汽加热原油,降低原油黏度,增强原油流动性,达到开采的目的[1-2]。同时会促使原油、地层水以及地层矿物之间发生一系列复杂的化学反应,进而产生CO
H
Manzano等提出,在TSR过程中参与反应的有机物类型有链烷烃、环烷烃、芳香烃等,并通过分析研究发现,3类物质中最容易进行TSR反应的是链烷烃,其次是环烷烃、芳香烃[9]。Zhang等通过模型化合物参与TSR的实验探究有机化合物的类型对TSR的影响,发现参与TSR程度大小为:辛烯>辛醇>辛酮>辛烷>辛酸>正辛基苯>二甲苯[10]。
Orr实验研究表明,由于甲烷的分子结构,其化学性质最稳定,参与TSR反应的可能性极低[11],但岳长涛等通过实验研究证明甲烷与硫酸钙可以发生TSR,并指出反应过程的表观活化能为154.623 kJ/mol[12]。Krouse等通过调研及理论分析发现,有两个方面会影响H
戴金星探究了高温高压条件下烃类和硫酸盐TSR反应生成H
张水昌等通过实验探究了离子浓度以及盐类型对TSR反应的影响,结果表明离子浓度对TSR反应具有较大影响,提高离子浓度有利于TSR反应进行;结果还表明反应体系中盐的类型对TSR反应亦有较大影响[18]。朱光有等以辽河稠油为研究对象探究了H
Hoffmann等研究了稠油热采生成H
从文献调研来看,TSR主要是针对天然气田的H
实验所用主要仪器设备如表 1所示。通过岩芯元素分析得到岩芯元素分布如表 2所示。可以看出,油藏矿物岩芯中元素O和Si的含量很高,此外,含有Al、K、Na、Mg、Fe等金属元素,同时,还检测到元素S。以上元素多以金属化合物的形式存在于油藏岩石中,而硫元素主要以金属硫酸盐和金属硫化物的形式存在。地层中硫酸盐的种类比较多,如石膏(CaSO
| 表1 主要实验仪器 Tab. 1 The main experimental instruments |
| 表2 油藏矿物岩芯XRF检测结果 Tab. 2 Detection results of reservoir core by XRF |
| 表3 实验药品试剂 Tab. 3 Experimental reagents |
稠油油样来自辽河油田洼1914井,其元素分析见表 4,其组分分析如表 5所示。
| 表4 洼1914井原油基本组成元素的检测结果 Tab. 4 Detection results of crude oil(Well Wa1914) element detection and sulfur content |
| 表5 洼1914井原油族组分检测结果 Tab. 5 Detection results of crude oil(Well Wa1914) component |
实验系统如图 1所示。实验步骤如下。
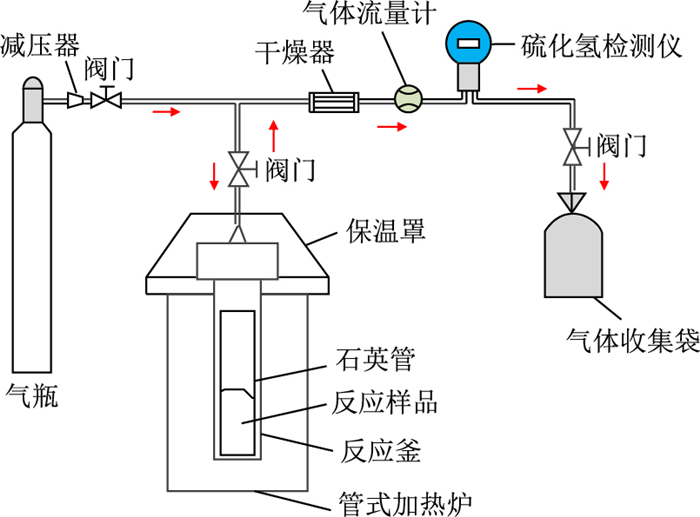 |
| 图1 实验装置图 Fig. 1 Experimental chart |
(1) 将样品分别按照设定好的比例称取,将配比好的样品放入石英管中,然后将石英管放入耐高温高压的哈氏合金钢反应釜中;向反应釜内反复充入1.0 MPa的高纯度氮气,目的是排除反应釜内的空气和维持反应所需要的高压条件;氮气充压完成后,检查反应釜的气密性,确定反应釜完全密封不漏气。
(2) 根据预定的实验温度,先将管式加热炉温度升至预设温度,然后将反应釜放入管式加热炉中进行恒温加热,通过热电偶实时监测温度。
(3) 反应完成后,关闭管式加热炉,取出反应釜,将反应釜放置在室温中10 min后,用水将反应釜迅速冷却至室温,使得反应釜内的蒸汽冷凝为水,减少气体中水的含量;将反应后釜内的气体通过H
(4) 将反应过后的固液油进行分离,分别检测其成分,判断TSR反应的产物。
2 实验结果及分析 2.1 气相检测对注汽锅炉冷凝水进行离子分析,结果发现Na
在进行TSR反应时,由于反应系统中存在水,因此需要考虑稠油热裂解和水热裂解对反应的影响,即空白实验为反应0,1和2。实验0可以看出,水与硫酸盐发生反应无H
|
表6 稠油与硫酸盐反应H |
将以上8组反应产生的气体通过气相色谱仪进行成分分析,具体结果如表 7所示。
| 表7 稠油与硫酸盐反应的气相色谱分析结果 Tab. 7 Analysis result of reaction between heavy oil and sulfates by GC |
从表 7可知,稠油进行热化学反应的气相组分以轻烃类气体为主,其中主要是甲烷。比较加入硫酸盐的反应气体产物可知,硫酸钠和硫酸钙的热模拟实验中,硫酸盐热化学还原序作用极低,其总烃生成量高于原油单独热裂解,但无机气体生成量低于原油热裂解,这是由于水的存在使得原油发生水热裂解反应,促进了原油成分裂解产生更多的气体,而CO
烃类气体和H
通过实验可知,硫酸盐热化学还原反应进行的程度越大,油相越呈现为焦性。即稠油中的饱和烃等低碳烃类参与硫酸盐热化学还原反应向焦性沥青转化,所以稠油参与TSR反应的产物有焦性沥青。通过红外光谱仪对干燥后固相物质进行检测,红外光谱图如图 2~图 5所示。
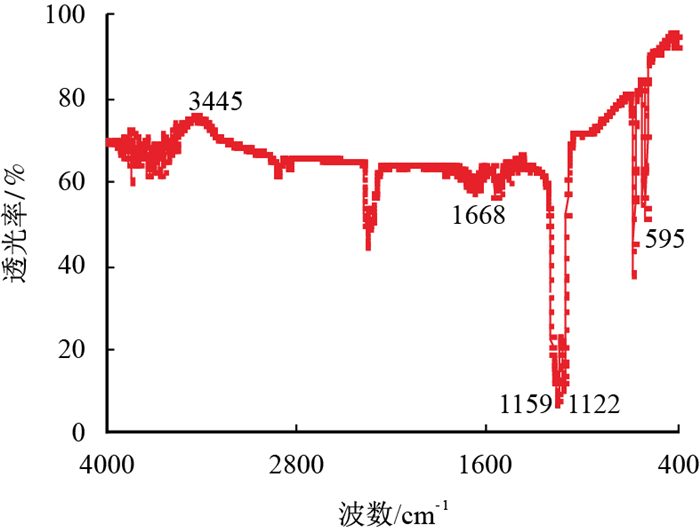 |
| 图2 稠油与硫酸钙反应后的固相产物红外光谱图 Fig. 2 FR-IR spectrogram of solidoid after the reaction the of heavy oil and calcium sulfate |
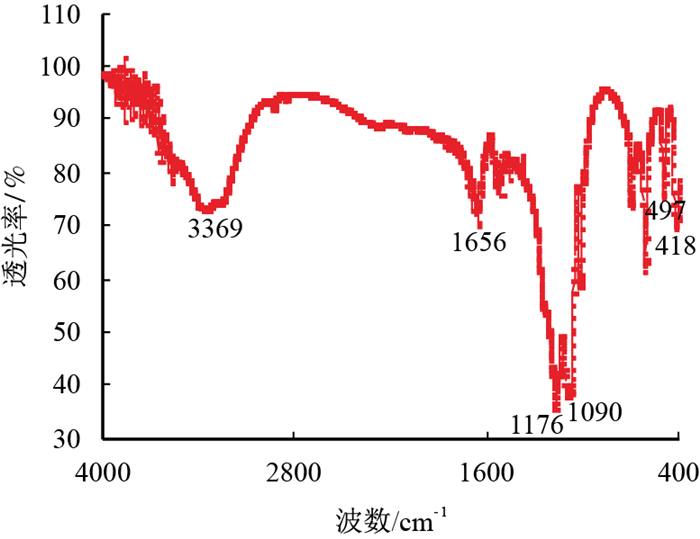 |
| 图3 稠油与硫酸镁反应后的固相产物红外光谱图 Fig. 3 FR-IR spectrogram of after of solidoid reaction of heavy oil and magnesium sulfate |
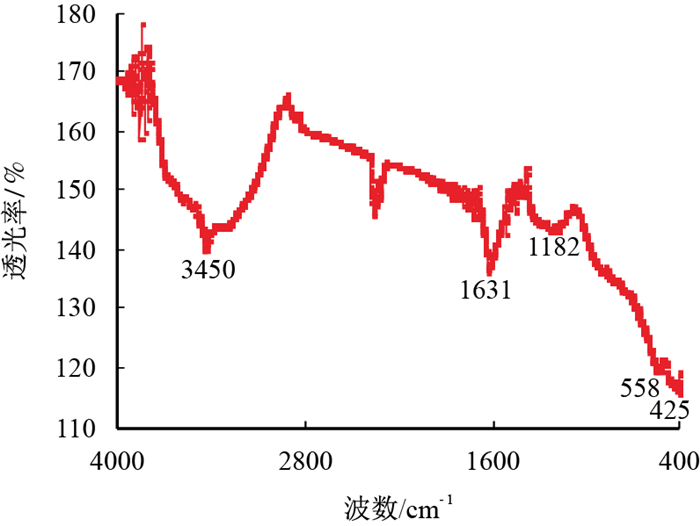 |
| 图4 稠油与硫酸铁反应后的固相产物红外光谱图 Fig. 4 FR-IR spectrogram of solidoid after the reaction of heavy oil and ferric sulfate |
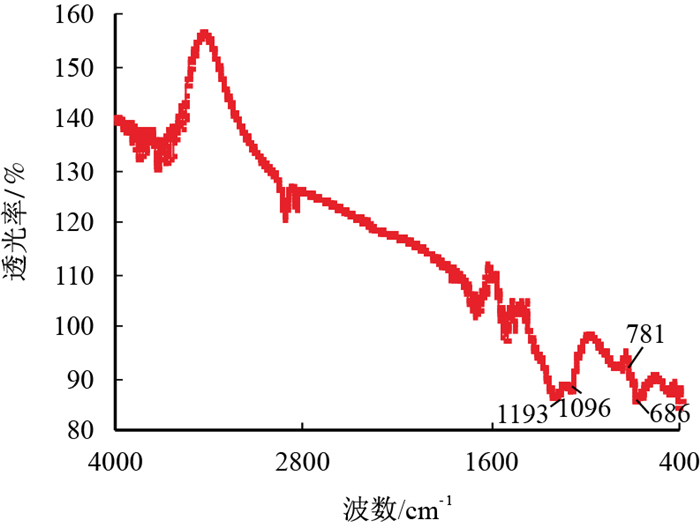 |
| 图5 稠油与硫酸铝反应后的固相产物外光谱图 Fig. 5 FR-IR spectrogram of solidoid after the reaction of heavy oil and aluminum sulfate |
由图 2可以看出,595 cm
综上可知,TSR反应生成的固相产物中有金属氧化物或者金属硫化物。普遍认为,金属氧化物的生成过程有两种:一种是氢氧化物的分解,另一种是碳酸盐的分解。但碳酸钙分解生成氧化钙的温度在900 ℃左右,碳酸镁的分解温度在500 ℃左右,而碳酸根与铝离子的双水解性质导致无法生成碳酸铝。根据实验条件可以判定氧化物的来源是其氢氧化物的分解。
结合硫酸铁与稠油的反应气体产物和固相产物可知,H
由于反应过程有水的参与,反应后冷却时油相产物会存在结合水,因此在检测油相产物时需要进行脱水处理,对处理后的油相产物进行含硫量分析,其结果如图 6所示。由表 4可知,反应前稠油硫含量为0.6%。
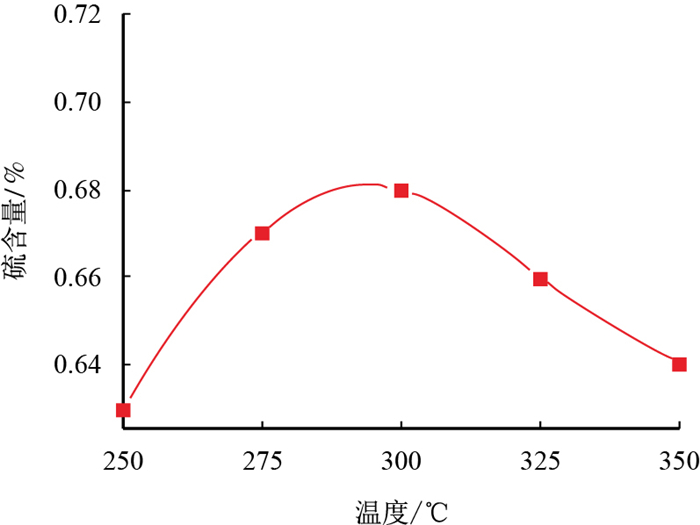 |
| 图6 TSR反应体系油相产物含硫量与温度的关系 Fig. 6 Content of sulfides in oil phase at different reaction temperatures |
从图 6可以看出,反应温度在350 ℃以下时,油相产物中硫含量都高于稠油的含硫量,这说明硫酸镁中的无机硫进入到油相中生成了有机硫。当温度低于300 ℃时,油相中硫含量随温度升高而增加,这是因为稠油中硫化物相对稳定,在低温时很难反应,而产生的H
(1) TSR的气体产物主要有H
(2) 反应后油相中硫含量高于反应前稠油中的硫含量,TSR反应将无机硫转化为有机硫,进而产生更多的H
| [1] |
王大为, 周耐强, 牟凯. 稠油热采技术现状及发展趋势[J]. 西部探矿工程, 2008, 20(12): 129-131. doi: 10.3969/j.issn.1004-5716.2008.12.045 |
| [2] |
刘喜林. 难动用储量开发稠油开采技术[M]. 北京: 石油工业出版社, 2005: 151-162. LIU Xilin. Hard to use reserves to develop heavy oil mining technology[M]. Beijing: Petroleum Industry Press, 2005: 151-162. |
| [3] |
IBATULLIN T, YANG T, PETERSEN E B, et al. Simulation of hydrogen sulfide and carbon dioxide production during thermal recovery of bitumen[C]. SPE 147934-MS, 2011. doi: 10.2118/147934-MS
|
| [4] |
THIMM H F. Aquathermolysis and sources of produced gases in SAGD[C]. SPE 170058, 2014. doi: 10.2118/170058-MS
|
| [5] |
张水昌, 帅燕华, 朱光有. TSR促进原油裂解成气:模拟实验证据[J]. 中国科学D辑:地球科学, 2008, 38(3): 307-311. |
| [6] |
戴金星, 胡见义, 贾承造, 等. 科学安全勘探开发高硫化氢天然气田的建议[J]. 石油勘探与开发, 2004, 31(2): 1-4. DAI Jinxing, HU Jianyi, JIA Chengzao, et al. Suggestions ofr scientifically and safely exploring and developing high H2S gas fields[J]. Petroleum Exploration and Development, 2004, 31(2): 1-4. doi: 10.3321/j.issn:1000-0747.2004.02.001 |
| [7] |
黄毅, 杨俊印, 吴拓, 等. 辽河油田稠油区块硫化氢分布特征及成因研究[J]. 天然气地球科学, 2008, 19(2): 255-260. HUANG Yi, YANG Junyin, WU Tuo, et al. Distribution and origin of hydrogen sulphide in heavy oil block, Liaohe Oilfield[J]. Natural Gas Geoscience, 2008, 19(2): 255-260. |
| [8] |
王潜. 辽河油田油井硫化氢产生机理及防治措施[J]. 石油勘探与开发, 2008, 35(3): 349-354. WANG Qian. Generation mechanism and control measures for H2S in oil wells, Liaohe Oilfield[J]. Petroleum Exploration and Development, 2008, 35(3): 349-354. doi: 10.3321/j.issn:1000-0747.2008.03.014 |
| [9] |
MANZANO B K, FOWLER M G, MACHEL H G. The influence of thermochemical sulphate reduction on hydrocarbon composition in Nisku reservoirs, Brazeau river area, Alberta, Canada[J]. Organic Geochemistry, 1997, 27(7-8): 507-521. doi: 10.1016/S0146-6380(97)00070-3 |
| [10] |
ZHANG Tongwei, ELLIS G S, WANG Kangshi, et al. Effect of hydrocarbon type on thermochemical sulfate reduction[J]. Organic Geochemistry, 2007, 38(6): 897-910. doi: 10.1016/j.orggeochem.2007.02.004 |
| [11] |
ORR W L. Rate and mechanism of non-microbial sulfate reduction: Thermochemical sulfate reduction[C]//Lecture notes of GRI workshop, 1990: 1-5.
|
| [12] |
岳长涛, 李术元, 丁康乐, 等. 硫酸盐热化学还原反应体系实验研究[J]. 科学技术与工程, 2004, 4(1): 44-45, 55. YUE Changtao, LI Shuyuan, DING Kangle, et al. Study of thermos-chemical sulfate reduction using simulation experients[J]. Science Technology and Engineering, 2004, 4(1): 44-45, 55. doi: 10.3969/j.issn.1671-1815.2004.01.013 |
| [13] |
KROUSE H R, VIAU C A, ELIUK L S, et al. Chemical and isotopic evidence of thermochemical sulphate reduction by light hydrocarbon gases in deep carbonate reservoirs[J]. Nature, 1988, 333(6172): 415-419. doi: 10.1038/333415a0 |
| [14] |
DIXON S A, SUMMERS D M, SURDAM R C. Diagenesis and preservation of porosity in Norphlet Formation (Upper Jurassic), Southern Alabama[J]. Aapg Bulletin American Association of Petroleum Geologists, 1989, 73(6): 707-728. |
| [15] |
戴金星. 我国天然气藏的分布特征[J]. 石油与天然气地质, 1982, 3(3): 270-276. DAI Jinxing. Distribution characteristics of gas pools in China[J]. Oil & Gas Geology, 1982, 3(3): 270-276. |
| [16] |
丁康乐, 李术元, 岳长涛, 等. 硫酸盐热化学还原反应基元步骤与反应机理初探[J]. 燃料化学学报, 2008, 36(6): 706-711. DING Kangle, LI Shuyuan, YUE Changtao, et al. Tentative study on elementary steps and reaction mechanism of thermo chemical sulfate reduction[J]. Journal of Fuel Chemistry and Technology, 2008, 36(6): 706-711. doi: 10.3969/j.issn.0253-2409.2008.06.012 |
| [17] |
MESHOULAM A, ELLIS G S, AHMAD W S, et al. Study of thermochemical sulfate reduction mechanism using compound specific sulfur isotope analysis[J]. Geochimica et Cosmo-chimica Acta, 2016, 188: 73-92. doi: 10.1016/j.gca.2016.05.026 |
| [18] |
张水昌, 帅燕华, 何坤, 等. 硫酸盐热化学还原作用的启动机制研究[J]. 岩石学报, 2012, 28(3): 739-748. ZHANG Shuichang, SHUAI Yanhua, HE Kun, et al. Research ion the initiation mechanism of thermochemical sulphate reduction[J]. Acta Petrologica Sinica, 2012, 28(3): 739-748. |
| [19] |
ZHU Guangyou, ZHANG Shuichang, HUANG Haiping, et al. Induced H2S formation during steam injection recovery process of heavy oil from the Liaohe Basin, NE China[J]. Journal of Petroleum Science and Engineering, 2010, 71(1-2): 30-36. doi: 10.1016/j.petrol.2010.01.002 |
| [20] |
HOFFMANN G G, STEINFATT I, STROHSCHEIN A. Thermal recovery processes and hydrogen sulfide formation[C]. SPE 29016, 1995. doi: 10.2118/29016-MS
|
| [21] |
HOFFMANN G G, DAVID T. Aquathermolysis of organic compounds in the presence of hydrogen sulfide and sulfate[J]. Abstracts of Papers of the American Chemical Society, 1997(3): 12. doi: 10.1016/S0140-6701(97)87663-1 |
| [22] |
刘永建, 范洪富, 钟立国, 等. 水热裂解开采稠油新技术初探[J]. 大庆石油学院学报, 2001, 25(3): 56-59. LIU Yongjian, FAN Hongfu, ZHONG Liguo, et al. Fundamental research on aquathermolysis for heavy oils recovery tehchnology[J]. Journal of Daqing Petroleum Institute, 2001, 25(3): 56-59. doi: 10.3969/j.issn.2095-4107.2001.03.013 |
| [23] |
彭文世, 刘高魁. 矿物红外光谱图集[M]. 北京: 科学出版社, 1982. PENG Wenshi, LIU Gaokui. The infrared spectra of minerals[M]. Beijing: Science Press, 1982. |
| [24] |
迪安. 兰氏化学手册[M]. 北京: 科学出版社, 1991. DI An. Langerhans chemical manual[M]. Beijing: Science Press, 1991. |
 2019, Vol. 41
2019, Vol. 41


