二氧化碳用于驱油已有许多年的历史[1-3],随着对于二氧化碳减排要求的日益提高,二氧化碳驱更为广泛地应用到了原油的开采中。由于二氧化碳气体的黏度低、密度低,极易在高渗层发生气窜及重力分异,因此在地层中的波及系数低[4-5]。针对这一问题,目前应用较为广泛的解决方法是使用表面活性剂溶液产生二氧化碳泡沫来控制二氧化碳流度[5-8]。但采用表面活性剂形成的二氧化碳泡沫存在一些不足,在油藏条件下接触到原油后容易消泡,并且用于产生泡沫的表面活性剂在高温条件下易发生分解[9]。二氧化碳在驱油方面较空气及氮气具有很多优势,但二氧化碳泡沫体系相对于氮气泡沫及空气泡沫稳定性较差,因此提高二氧化碳泡沫体系的稳定性具有重要的现实意义。
近年来,随着纳米技术的发展,对于使用纳米颗粒来稳定二氧化碳泡沫的研究逐渐得到了重视。本文结合国内外纳米颗粒稳定泡沫的理论与针对纳米二氧化碳泡沫的相关实验研究,探讨了纳米颗粒作为二氧化碳泡沫稳泡剂的优势、提高二氧化碳泡沫稳定性的机理、影响因素以及相关应用,并针对目前存在的问题提出了下一步的研究方向。
1 纳米颗粒稳定二氧化碳泡沫的优势经过改性后的纳米颗粒(如纳米二氧化硅颗粒)可作为稳泡剂,与表面活性剂相比,具有以下优势:(1)由于纳米颗粒具有一些固体颗粒的特点,因此在高温及高盐的条件下依然可以起到稳泡作用[10-13],这对二氧化碳泡沫在恶劣的地层条件下的应用具有重要意义。(2)地层对表面活性剂的吸附量大,而经过表面处理的纳米颗粒能够在地层孔隙中运移并且吸附量较少[14-15],减少了纳米颗粒的损失及对地层的伤害。(3) Dickson等研究发现,由于二氧化碳分子缺少永久偶极矩,并且范德华力弱,表面活性剂亲二氧化碳的一端在二氧化碳中的溶剂化作用通常较弱,使得表面活性剂更倾向于在液相中而非吸附在CO2/水界面上,因此导致表面活性剂稳定的二氧化碳泡沫稳定性较差[16];而被均匀改性过的纳米颗粒对二氧化碳和水均有亲和力,从而避开了二氧化碳分子对稳泡剂非极性端结合力较差的问题[17]。(4)二氧化碳相比于氮气在水中溶解度较高(比如饮料中,二氧化碳的溶解度比氮气大50倍[13]),因此造成泡沫破灭的歧化反应更加明显,这是二氧化碳泡沫稳定性较差的原因之一[4]。纳米颗粒吸附在CO2/水界面上后,由于纳米颗粒的尺寸与表面活性剂分子相比较大,减少了二氧化碳气体与液膜的接触面积,从而减弱了歧化反应。这说明纳米颗粒非常适合用于稳定二氧化碳泡沫。
2 纳米颗粒对二氧化碳泡沫的稳定机理由于泡沫具有较大的表面积和较高的表面自由能,因此泡沫为热力学不稳定体系。造成泡沫破灭的机理主要包括液膜的排液、气泡间的歧化反应以及气泡的聚并[13]。表面活性剂可吸附在气/液界面降低表面张力,从而对泡沫起到稳定作用。而Binks等研究发现,在由纳米颗粒稳定的泡沫体系中,纳米颗粒的加入并未改变表面张力的大小[17]。可见,纳米颗粒与表面活性剂对泡沫的稳定机理不同。目前对于纳米颗粒的稳泡机理主要有以下几种看法。
2.1 脱附能理论研究表明,纳米颗粒稳定泡沫的一个重要机理就是纳米颗粒可在气-液界面上形成吸附[18-21]。由于纳米颗粒具有一定的固体颗粒特征,相比于表面活性剂,纳米颗粒吸附形成的膜具有较高的机械强度,从而增强了泡沫的稳定性。Horozov借助于颗粒稳定乳状液的机理解释了颗粒对于泡沫的稳定作用。Horozov研究发现,吸附在液膜上并紧密排列的颗粒对液膜中水动力学流动具有阻力作用,从而减缓了液膜的排液。此外,由于纳米颗粒在液膜的致密排列,减少了气体与液体的接触面积,在一定程度上也抑制了泡沫的歧化作用[22-23]。
纳米颗粒与表面活性剂均可在界面吸附,但与表面活性剂不同的是,纳米颗粒在吸附界面上的脱附能要远大于表面活性剂。脱附能是指颗粒从界面上脱附所需要的能量,脱附能越大,表明颗粒与液膜的结合力越强,形成的液膜越稳定。颗粒的脱附能示意图见图 1,其值可通过式(1)计算得出[24]。
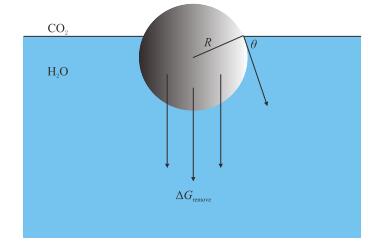 |
| 图1 颗粒脱附能示意图 Fig. 1 The detachment energy of the particle |
| $ \Delta {G_{{\rm{remove}}}} = \pi {R^2}{\gamma _{{\rm{OW}}}}{\left( {1-\left| {\cos \theta } \right|} \right)^2} $ | (1) |
式中:∆Gremove—脱附能,J;R—颗粒的半径,10-6 m;γOW—界面张力,mN/m;θ—颗粒与水相的接触角,(°)。
Binks通过计算得出,一般情况下,粒径为几百纳米的颗粒脱附能约为几千KBT(KB—玻尔兹曼常数,KB=1.380 650 5×10−23 J/K;T—绝对温度,K),而普通表面活性剂分子在油水界面上的脱附能仅为几个KBT。这进一步表明了表面活性剂分子在界面上的吸附为动态平衡过程,而颗粒的吸附则可以看作一种不可逆的过程,即颗粒一旦吸附在界面上便很难脱附,因此,固体颗粒比一般表面活性剂具有更强的稳泡作用。而当粒径较小时( < 5 nm),由式(1)计算出的脱附能虽然较小,但此时颗粒能够均匀地分散在体相中形成有序的结构,增加了体相的黏度,从而减缓了排液,增强了泡沫稳定性。
2.2 最大毛细压理论根据式(1)可以看出,当颗粒与水相接触角为90°时脱附能最大,泡沫体系最稳定,但研究发现,当泡沫体系最稳定时接触角在60°~80°[13, 23, 25]。很明显,单纯使用脱附能理论并不能完全解释颗粒对于泡沫的稳定机理。对此,许多研究者提出使用最大毛细压理论进行进一步的解释。与脱附能理论不同,毛细压考虑的并不是吸附在界面上的颗粒作用,而是考虑位于界面之间的颗粒的作用。位于界面之间的颗粒提供了一种毛细压力将相邻的气泡分开(图 2),而气泡的聚并就需要克服这种毛细压力,因此毛细压力也可以理解为一种类似分离压的作用力。
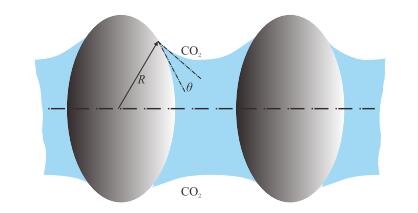 |
| 图2 最大毛细压示意图 Fig. 2 The maximum capillary pressure of coalescence |
最大毛细压可通过式(2)计算得出。
| $ p_{\rm{c}}^{{\rm{max}}} = \pm p\frac{{2{\gamma _{{\rm{AW/OW}}}}}}{R}\cos \theta $ | (2) |
式中:
pcmax—最大毛细压,mPa;±—对气泡和水包油体系取正值,对油包水体系取负值;p—理论堆积参数,无因次,表征了颗粒浓度和结构的影响;γAW/OW—气水或油水的界面张力,mN/m。
由式(2)可以看出,最大毛细压随着接触角的增大而减小,这与脱附能和接触角的关系相反,因此将以上两种理论结合可以较为合理地解释颗粒对泡沫的稳定作用。
2.3 颗粒间的相互作用脱附能理论与最大毛细压理论讨论的均是颗粒与液膜的相互作用,也有不少研究者提出,颗粒间的相互作用力也对泡沫的稳定性起到了重要作用[26-27]。界面颗粒间的相互作用力包括静电作用力(沉浸于水相部分)、范德华力、疏水作用力(沉浸于水相部分)、偶极静电作用力(浮于水面之上部分)、单极库伦作用力(浮于水面之上部分),以及由于界面颗粒周围弯液面引起的毛细引力[13]。
颗粒间在界面上的相互作用理论非常复杂,至今仍有许多无法解释的实验现象。但这些相互作用的宏观表现本质上是通过形成空间网络结构(图 3),从而对气泡起到一种屏障保护作用,这种保护作用可以通过气泡间聚并过程来理解。气泡间的聚并是由于液膜排液变薄造成的,在变薄的最后阶段,液膜会形成一个空洞,随着空洞的扩大,液膜逐渐破灭消失。当稳泡剂分子覆盖在液膜上时,在液膜中形成这样一个能够导致液膜破灭的有效空洞时就必须克服一个能量势垒。因此气泡聚并速度便与所需的能量势垒大小有关。根据脱附能理论,颗粒很难从液膜中脱附,因此在这一过程中颗粒更有可能随着液膜一起移动,而非离开液膜进入空洞中,因此由颗粒间的相互作用形成的网络结构大大增加了能量势垒,减弱了液膜排液作用,降低了气泡的聚并速度,从而对泡沫起到了重要的保护作用。
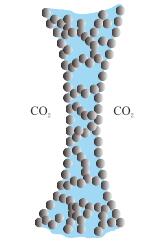 |
| 图3 颗粒形成的网络结构示意图 Fig. 3 The network structure of the nanoparticles inside the film |
目前利用纳米颗粒产生二氧化碳泡沫的方法主要是将纳米颗粒分散至液相中再与超临界状态下的二氧化碳进行混合,通过岩芯或者孔口的剪切作用产生泡沫。产生的二氧化碳泡沫性质主要受以下因素的影响。
3.1 纳米颗粒的疏水性应用于二氧化碳泡沫中的纳米颗粒的一个重要特性就是具有合适的疏水性能,即亲水/亲CO2平衡值(HCB)[28]。与HLB值(表面活性剂的亲水亲油平衡值)类似,HCB值表征了纳米颗粒在界面的吸附特性。式(3)为HCB的计算公式。
| $ \frac{1}{K} = \frac{{{A_{{\rm{AC}}}}-{A_{{\rm{AA}}}}-{A_{{\rm{CC}}}}}}{{{A_{{\rm{AW}}}}-{A_{{\rm{AA}}}} - {A_{{\rm{WW}}}}}} $ | (3) |
式中:A—相互作用能,J;K—HCB值;
下标:A—双亲分子,C—二氧化碳分子,W—水分子。
对于表面活性剂而言,非极性端主要对AAW有贡献,极性端主要对AAC有贡献。由于表面活性剂非极性端在二氧化碳中溶解较差(AAC值非常小),而极性端在水中溶解能力强(AAW值较大),最终使得表面活性剂更倾向于在水中而非吸附在CO2/水界面上。与表面活性剂不同,被均匀改性过的纳米颗粒没有非极性端和极性端的区分,而是对水相及二氧化碳均有亲和力[11],因此不存在非极性端在二氧化碳中溶解较差的问题,可以更好地吸附在界面上。
HCB值影响产生的CO2/水体系的性质。例如,Adkins利用疏水性较强的三乙氧基硅烷对纳米二氧化硅颗粒进行改性,得到的HCB值低,产生的是W/C乳状液;而Dickson利用二氯三甲基硅烷对纳米二氧化硅颗粒进行改性,得到的HCB值较高,产生的则是C/W泡沫[18]。
HCB值影响二氧化碳泡沫的稳定性。依据前面所介绍的脱附能理论及最大毛细压理论,颗粒与水相的接触角是影响泡沫稳定性的关键因素,通过改性调整HCB值可改变接触角的大小,从而使接触角达到最佳的稳定泡沫状态[29]。
3.2 纳米颗粒的粒径颗粒粒径对泡沫稳定性的影响与接触角相似。粒径小的颗粒最大毛细压大,对液膜有较好的稳定作用,但同时脱附能较小,在界面的吸附能力较弱。因此要想得到稳定的泡沫,颗粒的粒径不能过大也不能过小。能够用于稳定泡沫的颗粒粒径一般位于几纳米至几微米的范围内[23]。此外,Hariz T R在研究中发现,经过相同方式改性过的纳米二氧化硅颗粒在相同的浓度及实验条件下,5 nm粒径的颗粒相较于20 nm粒径的颗粒产生的泡沫更加稳定且气泡更小。这可能是由于相同浓度下颗粒粒径越小,颗粒数量越多、表面积越大并且在液相中的分散更均匀[30]。
3.3 纳米颗粒的浓度Espinoza D A在实验中发现,能够产生较为稳定的二氧化碳泡沫的颗粒浓度存在一个临界值。在温度为21.1 ℃、压力为1 350 psi(1 psi=6.895 kPa)的实验条件下,经过改性后包覆PEG的纳米二氧化硅颗粒在浓度低于0.05%时无法产生稳定的二氧化碳泡沫[31]。但同时颗粒浓度过高会对泡沫的稳定起到不利的作用。Yu Jianjia研究发现,在一定范围内(0.4%~0.6%),颗粒浓度越高产生的二氧化碳泡沫高度越高,而当颗粒浓度进一步升高后产生的泡沫高度有所下降。Yu Jianjia等认为这种现象是由于在低浓度范围内,颗粒浓度越高,吸附到CO2/水界面上的颗粒越多,对泡沫稳定作用越强;而当浓度增大到一定程度时,颗粒发生聚并使得粒径增大,从而不利于泡沫的产生[32]。
3.4 矿化度矿化度对于纳米二氧化碳泡沫主要产生两方面的影响。一方面,矿化度的增加会使得纳米颗粒的疏水性增强,HCB值降低,从而使得颗粒与CO2/水界面的接触角更有利于颗粒在界面的吸附[33]。Dickinson E等在实验研究中发现,0.1%纳米二氧化硅浓度下当NaCl浓度由0提高到2%时,以及0.5%纳米二氧化硅浓度下当NaCl浓度由2%提高到4%时,产生的泡沫黏度增加。另一方面,矿化度的增加会降低颗粒的zeta电位,从而降低了颗粒间的静电斥力,使得颗粒更易发生聚并,不利于泡沫的产生[34]。Yu Jianjia等在实验研究中发现,0.5%纳米二氧化硅浓度下当NaCl浓度增加到5%时,泡沫的产生受到了很大程度的抑制[32]。因此,合理控制矿化度,综合考虑矿化度对泡沫黏度及稳定性的影响对二氧化碳泡沫的流度控制具有重要意义。
3.5 温度与压力温度与压力主要是通过影响表张力的大小与二氧化碳在水中的溶解度影响泡沫的产生与稳定性[32]。一方面压力的升高可降低表面张力,有利于泡沫的稳定性;另一方面随着压力的升高,二氧化碳的溶解度增大,增强了重力排液作用,从而降低了泡沫的稳定性。Yu Jianjia在实验中发现,在压力为1 200~2 000 psi,随着压力的升高,产生的泡沫高度增加,但稳定性降低。温度越高,二氧化碳溶解度越低,但同时表面张力增加,并且由于加剧了纳米颗粒的热运动,不利于纳米颗粒在界面的吸附。Yu Jianjia在实验中发现,在温度为25~60 ℃,随着温度的升高,泡沫稳定性降低,当温度达到60 ℃时无泡沫产生。
4 纳米二氧化碳泡沫的应用情况目前尚没有针对纳米二氧化碳泡沫矿场试验的相关报道,并且针对这种新型二氧化碳泡沫体系的室内实验研究也较少,仅仅对该种泡沫体系在二氧化碳流度控制及驱油方面进行了少量的研究。
4.1 控制二氧化碳流度研究者们通过室内实验证实了纳米二氧化碳泡沫对二氧化碳的流度控制作用。Espinoza D A发现,在相同实验条件下加入纳米颗粒的二氧化碳泡沫的阻力因子是不加纳米颗粒的2~18倍[31];Yu Jianjia在实验中发现加入纳米颗粒后可将CO2/水体系流度降低至原来的1/10。Mo Di及Yu Jianjia等研究了纳米二氧化碳泡沫流度的影响因素,实验结果表明,泡沫质量(气液比)、纳米颗粒浓度、流速以及岩芯渗透率均对泡沫流度产生影响[35-36]。其中Yu Jianjia在实验中发现,纳米颗粒在岩芯中滞留较少,并且对岩芯渗透率的影响不大,说明纳米颗粒在孔隙结构中可以较好地运移,不会堵塞孔隙,这对纳米颗粒泡沫在现场的应用具有一定意义。
4.2 驱油Mo Di等通过室内实验模拟了纳米二氧化碳泡沫驱替剩余油的过程[36]。实验结果表明,纳米二氧化碳泡沫可在水驱后进一步提高35.8%~48.7%的原油采收率。相同实验条件下,加入纳米颗粒比未加入纳米颗粒的CO2/水体系提高采收率3%~6%,说明纳米颗粒的加入有利于泡沫的驱油。此外,相同的纳米泡沫体系在低渗(33 mD)岩芯中比在高渗(270 mD)岩芯中获得的采收率要高,这可能是由于在低渗岩芯中产生的二氧化碳泡沫更多的原因。
5 存在的问题及展望综上所述,纳米颗粒提高二氧化碳泡沫稳定性的研究已取得一定进展,但在许多方面还存在一些待解决的问题。
(1) 纳米颗粒对泡沫的稳定机理还需进一步完善,如最大毛细压理论是建立在颗粒处于静止状态的条件之上,并未考虑排液影响[37];纳米颗粒与表面活性剂对二氧化碳泡沫的协同稳泡作用已引起重视但相关研究有待深入。
(2) 由于针对纳米二氧化碳泡沫的室内实验研究较少,纳米二氧化碳泡沫在孔隙结构中的渗流机理、纳米颗粒在地层中的滞留机理以及由于加入纳米颗粒后带来的新的驱油机理等尚未进行相关研究。
(3) 纳米颗粒的成本相对较高,将此项技术应用于现场还需对颗粒的使用量及与现场工艺的结合进行深入的研究和分析。
虽然目前针对纳米二氧化碳泡沫的的应用研究较少,但已可以看出它在二氧化碳流度控制方面的潜力。随着纳米技术的进一步发展以及对纳米颗粒稳泡作用研究的继续完善,纳米二氧化碳泡沫对调剖堵水以及驱油等泡沫的现场应用问题,尤其是对解决泡沫在高温高盐地层条件下的应用问题将产生重要影响。
| [1] | Martin F D, Taber J J. Carbon dioxide flooding[J]. Journal of Petroleum Technology, 1992, 44 (4) : 396 –400. DOI:10.2118/23564-PA |
| [2] | Holm L W, Josendal V A. Mechanisms of oil displacement by carbon dioxide[J]. Journal of Petroleum Technology, 1974, 26 (12) : 1427 –1438. DOI:10.2118/4736-PA |
| [3] | Holm L W. Carbon dioxide solvent flooding for increased oil recovery[J]. Transaction of the AIME, 1959, 216 : 225 –31. |
| [4] | Nguyen N M. Systematic study of foam for improving sweep efficiency in chemical enhanced oil recovery[D]. Austin:The University of Texas, 2010. |
| [5] | Holm W L. Evolution of the carbon dioxide flooding processes[J]. Journal of Petroleum Technology, 1987, 39 (11) : 1337 –1342. DOI:10.2118/17134-PA |
| [6] | Wang D, Han P, Shao Z, et al. Sweep-improvement options for the Daqing Oil Field[J]. SPE Reservoir Evaluation & Engineering, 2008, 11 (1) : 18 –26. |
| [7] | Bernard G C, Holm L W, Harvey C P. Use of surfactant to reduce CO2 mobility in oil displacement[J]. Society of Petroleum Engineers Journal, 1980, 20 (4) : 281 –292. DOI:10.2118/8370-PA |
| [8] | Farajzadeh R. Enhanced transport phenomena in CO2 sequestration and CO2 EOR[D]. Delft:Delft University of Technology, 2009. |
| [9] | Hanssen J E, Dalland M. Increased oil tolerance of polymer-enhanced foams:Deep chemistry or just "simple" displacement effects[C]. SPE 59282, 2000. |
| [10] | Binks B P. Particles as surfactants-similarities and differences[J]. Current Opinion in Colloid & Interface Science, 2002, 7 (1) : 21 –41. |
| [11] | Binks B P, Horozov T S. Aqueous foams stabilized solely by silica nanoparticles[J]. Angewandte Chemie, 2005, 117 (24) : 3788 –3791. DOI:10.1002/(ISSN)1521-3757 |
| [12] | Zhang T T, Davidson D, Bryant S L, et al. Nanoparticlestabilized emulsions for applications in enhanced oil recovery[C]. SPE 129885, 2010. |
| [13] | 张水燕.锂皂石及HMHEC与表面活性剂协同稳定的泡沫[D].济南:山东大学, 2008. http://cdmd.cnki.com.cn/article/cdmd-10422-2008192402.htm |
| [14] | Rodriguez P E, Roberts M, Yu Haiyang, et al. Enhanced migration of surface-treated nanoparticles in sedimentary rocks[C]. SPE 124418, 2009. |
| [15] | Yu Haiyang, Kotsmar C, Yoon K Y, et al. Transport and retention of aqueous dispersions of paramagnetic nanoparticles in reservoir rocks[C]. SPE 129887, 2010. |
| [16] | Dickson J L, Binks B P, Johnston K P. Stabilization of carbon dioxide-in-water emulsions with silica nanoparticles[J]. Langmuir, 2004, 20 (19) : 7976 –7983. DOI:10.1021/la0488102 |
| [17] | Binks B P, Horozov T S. Colloidal particles at liquid interfaces:an introduction[M]. Cambridge: Cambridge University Press, 2006 . |
| [18] | Ip S W, Wang S W, Toguri J M. Aluminum foam stabilization by solid particles[J]. Canadian Metallurgical Quarterly, 1999, 38 (1) : 81 –92. DOI:10.1179/cmq.1999.38.1.81 |
| [19] | Kam S I, Rossen W R. Anomalous capillary pressure, stress, and stability of solids-coated bubbles[J]. Journal of Colloid and Interface Science, 1999, 213 (2) : 329 –339. DOI:10.1006/jcis.1999.6107 |
| [20] | Shrestha L K, Acharya D P, Sharma S C, et al. Aqueous foam stabilized by dispersed surfactant solid and lamellar liquid crystalline phase[J]. Journal of Colloid and Interface Science, 2006, 301 (1) : 274 –281. DOI:10.1016/j.jcis.2006.04.065 |
| [21] | Zhang T, Espinosa D, Yoon K Y, et al. Engineered nanoparticles as harsh-condition emulsion and foam stabilizers and as novel sensors[C]//Houston Texas USA:Offshore Technology Conference, 2011. |
| [22] | Horozov T S, Aveyard R, Clint J H, et al. Particle zips:vertical emulsion films with particle monolayers at their surfaces[J]. Langmuir, 2005, 21 (6) : 2330 –2341. DOI:10.1021/la047993p |
| [23] | Horozov T S. Foams and foam films stabilised by solid particles[J]. Current Opinion in Colloid & Interface Science, 2008, 13 (3) : 134 –140. |
| [24] | Binks B P, Lumsdon S O. Influence of particle wettability on the type and stability of surfactant-free emulsions[J]. Langmuir, 2000, 16 (23) : 8622 –8631. DOI:10.1021/la000189s |
| [25] | Sun Y Q, Gao T. The optimum wetting angle for the stabilization of liquid-metal foams by ceramic particles:Experimental simulations[J]. Metallurgical and Materials Transactions A, 2002, 33 (10) : 3285 –3292. DOI:10.1007/s11661-002-0315-y |
| [26] | Sullivan A P, Kilpatrick P K. The effects of inorganic solid particles on water and crude oil emulsion stability[J]. Industrial & Engineering Chemistry Research, 2002, 41 (14) : 3389 –3404. |
| [27] | Hunter T N, Pugh R J, Franks G V, et al. The role of particles in stabilising foams and emulsions[J]. Advances in Colloid and Interface Science, 2008, 137 (2) : 57 –81. DOI:10.1016/j.cis.2007.07.007 |
| [28] | Johnston K P, da Rocha S R P. Colloids in supercritical fluids over the last 20 years and future directions[J]. The Journal of Supercritical Fluids, 2009, 47 (3) : 523 –530. DOI:10.1016/j.supflu.2008.10.024 |
| [29] | Aroonsri A, Worthen A J, Hariz T, et al. Conditions for generating nanoparticle-stabilized CO2 foams in fracture and matrix flow[C]. SPE 166319, 2013. |
| [30] | Hariz T R. Nanoparticle-stabilized CO2 foams for potential mobility control applications[D]. Austin:The University of Texas, 2012. |
| [31] | Espinoza D A, Caldelas F M, Johnston K P, et al. Nanoparticle-stabilized supercritical CO2 foams for potential mobility control applications[C]. SPE 129925, 2010. |
| [32] | Yu Jianjia, Liu Ning, Li Liangxiong, et al. Generation of nanoparticle-stabilized supercritical CO2 foams[C]. SPE 150849, 2012. |
| [33] | Worthen A J, Bagaria H G, Chen Y, et al. Nanoparticlestabilized carbon dioxide-in-water foams with fine texture[J]. Journal of Colloid and Interface Science, 2013, 391 : 142 –151. DOI:10.1016/j.jcis.2012.09.043 |
| [34] | Dickinson E, Ettelaie R, Kostakis T, et al. Factors controlling the formation and stability of air bubbles stabilized by particle hudrophobic silica nanoparticles[J]. Langmuir, 2004, 20 (20) : 8517 –8525. DOI:10.1021/la048913k |
| [35] | Mo Di, Yu Jianjia, Liu Ning, et al. Study of the effect of different factors on nanoparticle-stablized CO2 foam for mobility control[C]. SPE 159282, 2012. |
| [36] | Mo Di, Yu Jianjia, Liu Ning, et al. The application of nanoparticle-stabilized CO2 foam for oil recovery[C]. SPE 164074, 2013. |
| [37] | Kruglyakov P M, Nushtayeva A V, Vilkova N G. Experimental investigation of capillary pressure influence on breaking of emulsions stabilized by solid particles[J]. Journal of Colloid and Interface Science, 2004, 276 (2) : 465 –474. DOI:10.1016/j.jcis.2004.03.059 |
 2014, Vol. 36
2014, Vol. 36

