2. 中国农业大学动物医院, 北京 100193;
3. 北京宠颐生动物医院, 北京 100021;
4. 北京世纪好未来科技教育有限公司, 北京 100192
2. Veterinary Teaching Hospital of China Agricultural University, Beijing 100193, China;
3. Beijing Chongyisheng Animal Hospital, Beijing 100021, China;
4. Beijing Century TAL Education Technology Co., Ltd, Beijing 100192, China
犬细小病毒(canine parvovirus,CPV)是临床上引起犬发病的重要病原体,最早于1977年从患出血性肠炎的犬粪便中分离得到[1]。大多数的犬科动物均有可能感染CPV,6周龄至6月龄的犬发病率较高。大多数CPV患犬会出现胃肠道症状,表现为呕吐、腹泻、脱水和胃肠道出血等,少数病例会出现心肌炎症状[2]。除此之外,CPV会抑制骨髓,造成白细胞的减少。细小病毒病的治疗通常包括抗病毒治疗、对症治疗、防止继发感染和支持疗法。其中抗病毒治疗除了使用干扰素、球蛋白等广谱抗病毒药物外,还包括针对CPV进行特异性治疗。国内目前广泛使用CPV单克隆抗体进行特异性抗病毒治疗,而关于CPV特异性免疫球蛋白的临床应用情况报道较少。本研究收集了中国农业大学动物医院2016年1月—2019年11月接收的CPV病患犬病例治疗信息,旨在探究CPV特异性免疫球蛋白在临床的应用效果。
1 材料与方法 1.1 病例选择选取2016年1月—2019年11月在中国农业大学动物医院就诊、经安捷CPV抗原检测试纸条(Anigen Rapid CPV Ag Test KitⓇ)检测结果阳性的患犬作为研究对象,跟踪回访其治疗情况。研究对象不包含同时感染犬瘟热致死的病例。
1.2 特异性抗病毒药物犬细小病毒特异性免疫球蛋白注射液来自于北京博莱得利生物技术有限责任公司。本品主要含有犬细小病毒特异性免疫球蛋白,纯度≥96%,犬细小病毒中和抗体效价≥1∶640,HI效价≥1∶1 280。
犬细小病毒单克隆抗体注射液来自哈尔滨元亨生物药业有限公司。本品主要含有犬细小病毒单克隆抗体,HI效价≥1∶1 280。
1.3 方法通过临床跟诊、病历查阅和电话回访等方式详细记录CPV患犬的基本信息、免疫史和病史,观察和询问动物主人治疗过程中病犬精神饮食情况、呕吐情况、粪便性状、体温等临床症状。以患犬首次出现食欲下降、精神不振或呕吐、腹泻等CPV相关临床症状作为发病的首日,以呕吐和腹泻症状消失、精神食欲恢复正常作为痊愈判定标准计算病程。以拜奥高犬三联抗体检测试剂盒(Canine VacciCheckⓇ)检测结果作为抗体HI效价检测依据。
将收集的病例数据录入Microsoft Excel软件中整理,并采用SPSS软件对数据进行分析。
2 结果 2.1 总体治愈率比较在收集的具有详细病程及转归情况记录的CPV病例中,使用CPV特异性免疫球蛋白治疗的病例共97例,其中痊愈77例,死亡20例,治愈率为79.38%。在同一时期使用CPV单抗治疗的病例共计143例,其中痊愈116例,死亡27例,治愈率为81.12%。数据经SPSS软件进行卡方检验,CPV特异性免疫球蛋白与CPV单抗的治愈率无显著差异(P>0.05)。
2.2 不同初始抗体水平的治愈率比较在完整记录初始抗体水平的病例中,使用CPV特异性免疫球蛋白进行治疗的共69例,使用CPV单抗的共78例。按照初始CPV抗体效价0~1∶40、1∶80~1∶160、≥1∶320进行划分,各抗体水平的治愈率结果见表 1。
|
|
表 1 不同初始抗体水平CPV患犬的治愈率比较 Table 1 Comparison of cure rates of CPV dogs at different initial antibody levels |
初始抗体效价为0~1∶40时,CPV特异性免疫球蛋白治愈率为71.43%,CPV单抗治愈率为74.36%;初始抗体效价为1∶80~1∶160时,CPV特异性免疫球蛋白治愈率为91.30%,CPV单抗治愈率为88.00%;初始抗体效价≥1∶320时,CPV特异性免疫球蛋白治愈率为90.91%。CPV单抗治愈率为78.57%。数据经SPSS软件卡方检验,CPV特异性免疫球蛋白和CPV单抗在各初始抗体水平下的治愈率均无显著性差异(P>0.05)。另外,约50%的CPV患犬的初始抗体水平小于1∶80,该组治愈率低于更高抗体水平组,但无统计学差异。
2.3 不同月龄的治愈率比较按照0~3、4~6以及≥7月龄对病例进行划分。使用CPV特异性免疫球蛋白进行治疗的共97例,使用CPV单抗的共143例,各月龄段病例的治愈率结果见表 2。
|
|
表 2 不同月龄CPV患犬的治愈率比较 Table 2 Comparison of cure rate of CPV dogs at different month ages |
0~3月龄的病例中,CPV特异性免疫球蛋白治愈率为67.24%,CPV单抗治愈率为68.42%;4~6月龄的病例中,CPV特异性免疫球蛋白治愈率为95.24%,CPV单抗治愈率为91.30%;,7月龄及以上的病例中,CPV特异性免疫球蛋白与CPV单抗的治愈率均为100.00%。数据经SPSS软件卡方检验,在相同月龄段下,CPV特异性免疫球蛋白和CPV单抗的治愈率均无显著差异(P>0.05)。0~3月龄患犬占总数的50%~60%,该月龄段的治愈率均显著低于更高月龄段(P<0.05)。
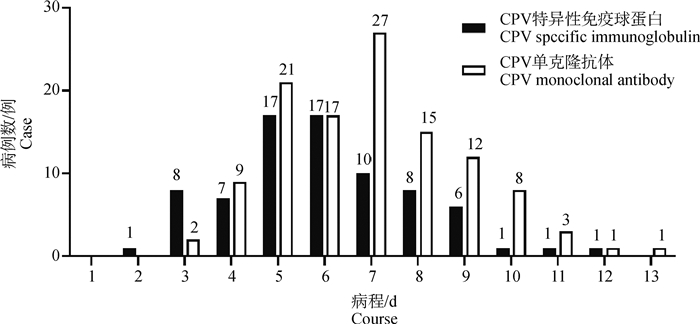
2.4 痊愈病例的病程比较CPV特异性免疫球蛋白与CPV单抗治疗的痊愈病例病程分布见图 1。由图可见CPV患犬的痊愈病程主要集中于4~9 d。使用CPV特异性免疫球蛋白后痊愈的病例共77例,其中病程为4~9 d的病例为65例,占84.42%。使用CPV单抗痊愈的病例116例,其中病程为4~9 d的病例为101例,占87.07%。经SPSS软件检验,两组病程数据均符合正态分布。使用独立样本T检验方法分析,使用CPV特异性免球蛋白治疗的病例痊愈时间为(6.00±2.01)d,使用CPV单抗治疗的病例痊愈时间为(6.95±2.06)d,特异性球蛋白组的治愈时间显著少于单抗组(P=0.02<0.05)。
|
图 1 不同药物治疗的CPV患犬的痊愈病程分布 Fig. 1 Distribution of recovery course of CPV infected dogs treated with different drugs |
犬细小病毒单克隆抗体是通过体外人工培养高效表达CPV特异性抗体的杂交瘤细胞株而获得的生物制品,其效价高且特异性强,在治疗犬细小病毒病方面发挥了重要作用。犬细小病毒特异性免疫球蛋白是通过对健康犬进行多次CPV免疫,从中筛选含有高效价CPV中和抗体的犬血清进行免疫球蛋白的提取和纯化而获得的血液制品。多种疾病中,高免血清的治疗效果已经被证实[3-4]。CPV特异性免疫球蛋白制剂与普通高免血清相比具有更高的安全性,在临床使用中未见明显不良反应。周灵等[5]使用与本研究相同的CPV特异性免疫球蛋白产品,结果显示其病毒中和效果优于CPV多克隆抗体,中和抗体效价达1∶873,HI效价达1∶211。姜旭等[6]、李六金等[7]证实了CPV免疫球蛋白对犬细小病毒病具有良好的治疗效果。
在本研究中,CPV特异性免疫球蛋白与临床较常使用的CPV单抗相比可以显著缩短痊愈病例的病程,原因可能在于以下两个方面。首先,CPV特异性免疫球蛋白来源于疫苗免疫的健康犬血清,经过蛋白提纯与灭活处理后,可以通过静脉注射直接进入血液循环,患犬吸收效率更高,起效更快。其次,与单克隆抗体比较,CPV特异性免疫球蛋白除了含有CPV特异性多克隆抗体外,还含有与生活环境和疫苗接种等相关的多种抗体和球蛋白,不仅可以中和病毒,还可以通过活化补体以及结合Fc受体产生抗体依赖性细胞毒性作用和调理吞噬作用,激活机体免疫细胞,清除细胞内的病毒,缩短治疗周期。
两种药物对相同月龄段患犬的治愈率并无差异,但0~3月龄病例的治愈率要显著低于更高月龄,这可能与3月龄以下幼犬免疫功能不完全和处于免疫窗口期有关。初始抗体效价达到1∶80以上的病例治愈率较高,这与Gooding和Robinson[8]的研究结果相同。部分高抗体水平的病例仍然出现死亡,首先可能是因为动物存在基础病或并发症。其次,部分患犬发病后数日首次测得的抗体滴度并不能完全代表其感染CPV时机体实际的抗体水平。另外,毒株变异可能导致致病性增强或抗原性改变,多篇报道指出接受完全免疫的犬暴发新亚型病毒的感染[9-11]。但疫苗免疫效果受多种因素影响,更多学者普遍认为目前CPV疫苗对各个亚型病毒均具有保护作用[12-14]。
犬细小病毒病作为宠物临床中死亡率较高的传染病,对养犬业带来了巨大的损失。寻找犬细小病毒病的有效治疗方法具有重要的临床意义,但防治犬细小病毒病更重要的是对幼犬进行免疫接种。世界小动物兽医协会(WSAVA)免疫小组研究指出,以正确程序接受核心疫苗的犬对疾病保护率达到98%以上[14]。在购买宠物犬时,要从正规渠道购买免疫完全的犬,尽可能保证动物健康。
4 结论CPV特异性免疫球蛋白和CPV单克隆抗体的总治愈率、相同初始抗体水平治愈率、相同月龄段治愈率均无显著差异(P>0.05),但使用CPV特异性免疫球蛋白的病例痊愈时间显著低于CPV单克隆抗体(P=0.02<0.05),这说明CPV特异性免疫球蛋白具有良好的临床应用效果。
| [1] |
EUGSTER A K, NAIRN C. Diarrhea in puppies: parvovirus like particles demonstrated in their feces[J]. South West Vet, 1977, 30(1): 59-60. |
| [2] |
AGUNGPRIYONO D R, UCHIDA K, TABARU H, et al. Subacute massive necrotizing myocarditis by canine parvovirus type 2 infection with diffuse leukoencephalomalacia in a Puppy[J]. Vet Pathol, 1999, 36(1): 77-80. DOI:10.1354/vp.36-1-77 |
| [3] |
MEUNIER P C, COOPER B J, APPEL M J G, et al. Pathogenesis of canine parvovirus enteritis: sequential virus distribution and passive immunization studies[J]. Vet Pathol, 1985, 22(6): 617-624. DOI:10.1177/030098588502200617 |
| [4] |
FOCOSI D, ANDERSON A O, TANG J W, et al. Convalescent plasma therapy for COVID-19: state of the art[J]. Clin Microbiol Rev, 2020, 33(4): e00072-20. |
| [5] |
周灵, 梁琳, 王宏伟, 等. 犬细小病毒免疫球蛋白对犬细小病毒中和活性的研究报告[J]. 中国兽医科学, 2016, 46(8): 1009-1014. ZHOU L, LIANG L, WANG H W, et al. Report on neutralization tests of immunoglobulin against canine parvovirus[J]. Chinese Veterinary Science, 2016, 46(8): 1009-1014. (in Chinese) |
| [6] |
姜旭, 赵健, 倪婷婷, 等. 犬细小病毒免疫球蛋白的有效性评价[J]. 实验动物科学, 2020, 37(5): 9-13. JIANG X, ZHAO J, NI T T, et al. Evaluation of the effectiveness of canine parvovirus immunoglobulin[J]. Laboratory Animal Science, 2020, 37(5): 9-13. (in Chinese) |
| [7] |
李六金, 屈红丽, 姜焕宏, 等. 抗犬细小病毒免疫球蛋白临床应用研究[J]. 中国兽药杂志, 2003, 37(3): 46-47, 32. LI L J, QU H L, JIANG H H, et al. Application of anti-canine-parvovirus immunoglobuline in the treatmeat of CPV infection[J]. Chinese Journal of Veterinary Drug, 2003, 37(3): 46-47, 32. (in Chinese) |
| [8] |
GOODING G E, ROBINSON W F. Maternal antibody, vaccination and reproductive failure in dogs with parvovirus infection[J]. Aust Vet J, 1982, 59(6): 170-174. DOI:10.1111/j.1751-0813.1982.tb15997.x |
| [9] |
DECARO N, DESARIO C, ELIA G, et al. Evidence for immunisation failure in vaccinated adult dogs infected with canine parvovirus type 2c[J]. New Microbiol, 2008, 31(1): 125-130. |
| [10] |
SHIMA F K, OMOBOWALE T O, ADESINA R D, et al. Molecular characterisation of canine parvoviruses from clinical samples and vaccines in Nigeria[J]. Infect Genet Evol, 2020, 85: 104553. DOI:10.1016/j.meegid.2020.104553 |
| [11] |
BATTILANI M, MODUGNO F, MIRA F, et al. Molecular epidemiology of canine parvovirus type 2 in Italy from 1994 to 2017:recurrence of the CPV-2b variant[J]. BMC Vet Res, 2019, 15(1): 393. DOI:10.1186/s12917-019-2096-1 |
| [12] |
SPIBEY N, GREENWOOD N M, SUTTON D, et al. Canine parvovirus type 2 vaccine protects against virulent challenge with type 2c virus[J]. Vet Microbiol, 2008, 128(1-2): 48-55. DOI:10.1016/j.vetmic.2007.09.015 |
| [13] |
SIEDEK E M, SCHMIDT H, STURE G H, et al. Vaccination with canine parvovirus type 2 (CPV-2) protects against challenge with virulent CPV-2b and CPV-2c[J]. Berl Munch Tierarztl Wochenschr, 2011, 124(1-2): 58-64. |
| [14] |
DAY M J, HORZINEK M C, SCHULTZ R D. WSAVA guidelines for the vaccination of dogs and cats[J]. J Small Anim Pract, 2010, 51(6): e1-e32. DOI:10.1111/j.1748-5827.2010.00959a.x |
编辑 白永平



