开放骨架结构的金属羧酸配位化合物, 作为一类新兴多孔材料, 因其在能源气体吸附分离、不对称催化、磁学、荧光、化学传感等众多领域有潜在应用, 其设计合成、晶体结构和性质研究成为国际国内研究热点[1-6]。对位四氮唑取代的苯甲酸配体同时含有N, O两类配位原子, 在溶剂热体系中与金属配位可组装形成一类化学组成丰富, 拓扑结构新颖的异核双金属有机骨架化合物。不同组成和维度的异核金属的合成和报道, 不仅丰富了金属有机骨架化合物的拓扑学结构, 还赋予此类材料一些有趣的磁学、光学性质及应用, 同时引起了物理学家和理论化学家的广泛关注[7]。LnⅢ因具有较大的离子半径和磁各项异性, 文献中广泛报道的是3d-4f异核金属有机骨架化合物的合成和磁学性质[8]。Gatteschi等报道了CuⅡ-GdⅢ配合物的合成和两种金属间的铁磁性相互作用[9]。N.Shikawa在文献中相继报道了使用LnⅢ(TbⅢ, DyⅢ and HoⅢ), 过渡金属和有机配体组装设计合成单分子磁体和单链磁体[10]。本文使用对位四氮唑取代的苯甲酸配体和两个过渡金属Cd, Cu在混合溶剂热体系中配位组装, 合成了一个新型异核双金属有机骨架配位化合物, C19H8N8O6CuCd(配合物1),并完成了配合物1晶体结构解析、结构表征和磁学性质测试工作。
1 实验部分 1.1 仪器与试剂配合物1的单晶结构分析使用Rigaku RAXIS-RAPID IP X-射线单晶衍射仪收集衍射数据。化合物元素分析采用Perkin-Elmer 3300DV ICP和elementer vario MICRO元素分析仪。红外光谱使用Bruker IFS-66V/S光谱仪抽真空测试。使用SQUID-VSM在1000 Oe, 2~300 K温度区间内测试配合物1的变温磁化率。
四氮唑苯甲酸配体4-(1H-Tetrazol-5-yl)-benzoic acid(C8H6N4O2)购于济南恒化科技有限公司, 合成中用到的其他化学试剂均是通过商业购买。所有试剂均未经提纯直接使用。
1.2 配合物1的实验合成将15 mg Cd(NO3)2·4H2O和12 mg Cu(NO3)2· 6H2O, 2.0 mg 4-(1H-Tetrazol-5-yl)-benzoic acid配体(H2L), 和1mL N-甲基甲酰胺(NMF)超声混合均匀, 转移到20 mL的玻璃小瓶中, 再依次加入0.10 mL H2O, 0.100 mL硝酸(2.8mol/L NMF), 再次超声混合均匀。用锡纸密封瓶口后再拧紧瓶盖, 放在85℃的烘箱内反应12 h得块状化合物1的单晶体。
2 晶体结构解析 2.1 单晶结构测试配合物1的单晶结构测试使用Rigaku RAXIS-RAPID IP X-射线单晶衍射仪收集衍射数据。在(20±2)℃用石墨烯单色器单色化的MoKα射线(λ=0.071 073nm), 扫描方式ω收集数据。扫描角范围3.12 < θ < 27.48, 共收集到19 273衍射点, 其中2164个独立衍射点(Rint=0. 069 5)。运行Process-auto程序还原衍射数据, 运行SHELXTL-97程序对配合物1的进行单晶结构解析和精修。单晶结构解析采用直接法(TREF), 单晶结构精修采用全矩阵最小二乘法(Full-matrix least-squares on F2)。在差傅立叶图上首先确定Cu, Cd原子的衍射峰位置, 再从残峰中依次确定四氮唑和苯甲酸结构中O,N和C原子衍射峰位置, 对所有非氢原子做各项异性精修。表 1是配合物1的详细晶体学数据表。
|
|
表 1 配合物1的晶体学数据表 Tab. 1 Crystal data and structure refinement for compound 1 |
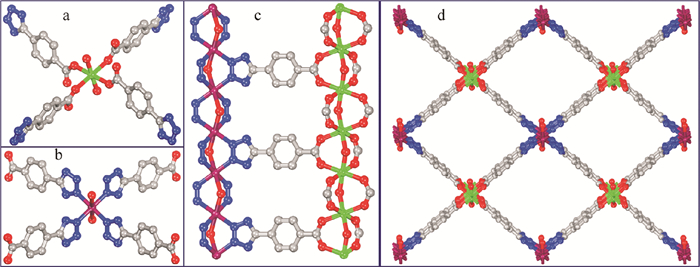
单晶X-射线衍射数据分析结果显示配合物1结晶在立方晶系(Cubic), 空间群Pmma (No.51), 化学式为C19H8N8O6CdCu。配合物1不对称结构单元包含1个晶体学独立Cd原子和1个晶体学独立的Cu原子,2个H2L配体、2个桥连O原子和一个客体分子。Cd1原子采取六配位的八面体配位模式(如图 1a), 分别和4个配体结构中的羧基氧原子配位, 另外两个配位点被桥连配位氧原子占据。CdO6八面体共顶点连接在x轴方向形成1D无限链结构[CdO6]n。Cu原子的配位环境和Cd原子类似, 分别和四氮唑配体结构中的4个氮原子和2个桥氧原子配位, 形成六配位的八面体结构CuN4O2(如图 1b), CuN4O2八面体共顶点连接在x轴方向形成1D无限链结构[CuN4O2]n。配体H2L的配位环境如图 1c所示, 链与链之间再通过H2L配体结构中氮和羧基氧原子配位连接在y,z轴方向进一步连接形成配合物1的3D开放骨架结构(如图 1d), 沿x轴方向可以观察到四方超大孔道。
|
图 1 Cd原子(a),Cu原子(b),HL(c)的配位环境和配合物1(d)的3D开放骨架结构 Fig. 1 The coordination geometries of Cd atom (a), Cu atom (b) and organic linker HL (c); the 3D open frameworks of compound 1 featuring large pore along x axis (d) |
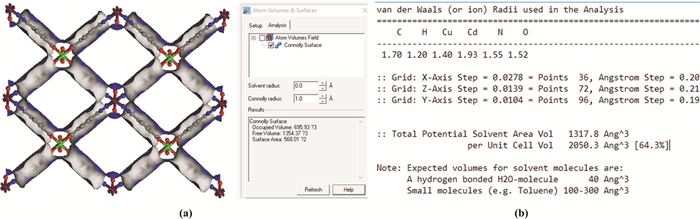
鉴于配合物1单晶结构中的存在的超大孔道, 使用MS 4.0软件模拟配合物1每个单胞的溶剂可占有体积0.695 93nm3、孔隙率66.1%和孔道比表面积5.680 1 nm2/per unit, 如图 2a所示。根据PLATON[11]软件计算结果输出文件(图 2b)可知:配合物1空旷的孔体积占据整个单胞体积的62.3 %。
|
图 2 (a) 配合物1每个单胞溶剂可占有体积, 孔隙率和孔表面积; (b)每个单胞溶剂可占有体积和孔隙率的PLATON软件计算结果 Fig. 2 (a) the solvent accessible volume and surface area per unit cell simulated by MS.4.0 software; (b) The solvent accessible volume per unit cell calculated by PLATON software in compound 1 |
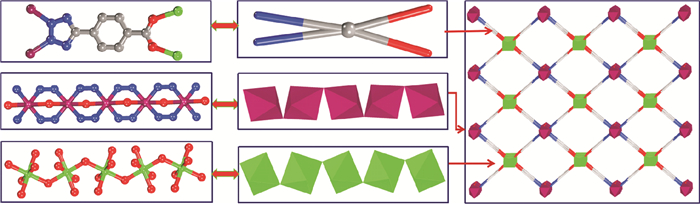
配合物1的拓扑学结构分析过程如下:有机配体H2L通过四氮唑结构中2个氮原子和2个Cu原子螯合配位, 通过2个羧基氧原子和2个Cd原子螯合配位, 采取平面四面形的配位模式, 在拓扑结构分析中可以抽象成一个4-连接的拓扑学节点, 金属Cu和Cd原子均是六配位, 都可以抽象成一个八面体构型的6-连接拓扑学节点, 整个化合物的拓扑学结构如图 3所示。异核双金属的主体骨架结构赋予了配合物1某些潜在的磁学性质及应用, 另外配合物1空旷的孔道结构为进一步探究开发其在能源气体吸附及分离等领域的潜在应用提供了可能性。
|
图 3 化合物1的拓扑学结构及分析 Fig. 3 Novel topological structure of compound 1 |
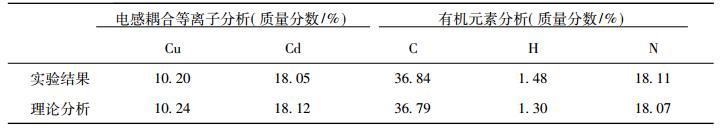
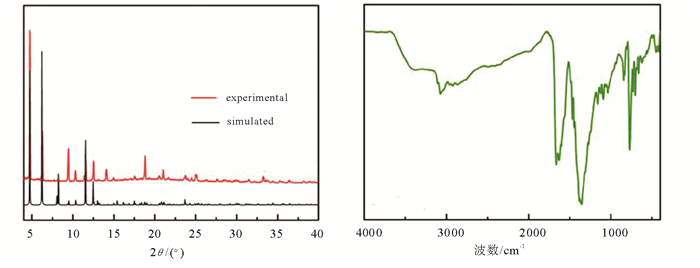
图 4给出了配合物1的PXRD(左图)和红外光谱(右图)。实验测试粉末X-射线衍射谱图(PXRD)和根据配合物1的单晶结构理论拟合衍射谱图的衍射峰位置一致, 表明合成产物为纯相, 而衍射峰强度的不同则是由于实验中配合物1的单晶晶面取向不同所致。红外光谱上高波数区3 200~2 800 cm-1的吸收峰归属于配体结构中四氮唑N—H, 苯环C—H伸缩振动, 在1 800~1 200 cm-1波数区间内出现了配体结构中四氮唑和苯环等芳香环的特征伸缩振动吸收峰。相应基团的弯曲振动吸收峰出现在更低波数区间内。配合物1的元素分析测定结果和根据单晶结构理论拟合结果基本一致, 详见表 2。
|
图 4 配合物1的(左)实验和理论拟合X-射线粉末衍射谱图, (右)红外光谱图 Fig. 4 Simulated and experimental X-ray powder diffraction patterns(left)and IR spectrum (right)for compound 1 |
|
|
表 2 化合物1的元素分析结果 Tab. 2 The result of elemental analysis for compound 1 |
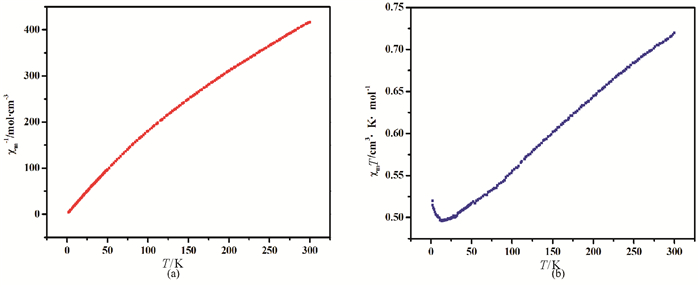
固定外加磁场强度80 000A/m, 在2~300K温度区间内测试配合物1的变温磁化率, 测试结果如图 5所示。图 5(a)给出了摩尔磁化率的倒数χm-1随T变化的曲线, 配合物1的磁学性质遵守居里-外斯定律, 拟合实验数据, 得到不同温度区间内的Curie常数C和Weiss温度θ:在2~16K区间, C=0.49 cm3·K/mol, θ=0.12K;在16~300K区间, C=0.74 cm3·K/mol, θ=-24.74 K。其中Weiss温度θ为负值, 证明了配合物1具有反铁磁性, 在较低温度条件下转变为铁磁性(2~16K, Weiss温度θ为正)。如图 5(b)所示, χm·T随温度升高先降低后升高也进一步佐证了上述结论。
|
图 5 配合物1的变温磁化率测试结果 Fig. 5 The experimental result of temperature variable susceptibility of compound 1 |
在NMF/H2O混合溶剂热体系中,本文选择同时含有N,O配位原子的四氮唑取代的苯甲酸配体4-(1H-Tetrazol-5-yl)-benzoic acid(C8H6N4O2, H2L)与两种过渡金属Cu和Cd配位组装合成了一例具有3D开放骨架结构的异核双金属配合物1, C19H8N8O6CuCd。单晶衍射分析结果显示:每个配体H2L作为一个平面4-连接的拓扑学节点分别和2个Cu, 2个Zn原子配位; 两种金属原子均采用六配位的八面体构型, 可抽象为6-连接拓扑学节点, 在x轴方向共顶点连接形成1D无限链结构, 链与链之间再通过配体H2L的配位连接形成配合物1的3D开放骨架结构, 沿x轴方向可以观察到四方超大孔道。另外还完成了对配合物1的粉末X-射线衍射, 红外光谱和元素分析等相关表征工作。变温磁化率实验测试结果显示配合物1显示反铁磁性, 较低温度条件下转化为铁磁性。
| [1] |
EDDAOUDI M, MOLER D B, LI H L, et al. Modular chemistry: Secondary building units as a basis for the design of highly porous and robust metal-organic carboxylate frameworks[J]. Acc Chem Res, 2001, 34(4): 319-330. DOI:10.1021/ar000034b |
| [2] |
YAGHI O M, O'KEEFFE M, OCKWIG N W, et al. Reticular synthesis and the design of new materials[J]. Nature, 2003, 423(6941): 705-714. DOI:10.1038/nature01650 |
| [3] |
ZHOU H C, LONG J R, YAGHI O M. Introduction to metal-organic frameworks[J]. Chem Rev, 2012, 112(2): 673-674. DOI:10.1021/cr300014x |
| [4] |
LI M, LI D, O'KEEFFE M, et al. Topological analysis of metal-organic frameworks with polytopic linkers and/or multiple building units and the minimal transitivity principle[J]. Chem Rev, 2013, 114(2): 1343-1370. |
| [5] |
NUGENT P, BELMABKHOUT Y, BURD S D, et al. Porous materials with optimal adsorption thermodynamics and kinetics for CO2 separation[J]. Nature, 2013, 495(7439): 80-84. DOI:10.1038/nature11893 |
| [6] |
AL-MAYTHALONY B A, SHEKHAH O, SWAIDAN R, et al. Quest for anionic MOF membranes: Continuous sod-ZMOF membrane with CO2 adsorption-driven selectivity[J]. J Am Chem Soc, 2015, 137(5): 1754-1757. DOI:10.1021/ja511495j |
| [7] |
ANDRUH M, COSTES J P, DIAZ C, et al. 3d-4f Combined chemistry: Synthetic strategies and magnetic properties[J]. Inorg Chem, 2009, 48(8): 3342-3359. DOI:10.1021/ic801027q |
| [8] |
BENELLI C, GATTESCHI D. Magnetism of lanthanides in molecular materials with transition-metal ions and organic radicals[J]. Chem Rev, 2002, 102(6): 2369-2388. DOI:10.1021/cr010303r |
| [9] |
BENCINI A, BENELLI C, CANESCHI A, et al. Crystal and molecular structure of and magnetic coupling in two complexes containing gadolinium(Ⅲ) and copper(Ⅱ) ions[J]. J Am Chem Soc, 1985, 107(26): 8128-8136. DOI:10.1021/ja00312a054 |
| [10] |
ISHIKAWA N, SUGITA M, WERNSDORFER W. Quantum tunneling of magnetization in lanthanide singe-molecule magnets: Bis(phthalocyaninato)terbium and bis(phthalocyaninato)dysprosium anions[J]. Angew Chem Int Ed, 2005, 44(19): 2931-2935. DOI:10.1002/(ISSN)1521-3773 |
| [11] |
SPEK A L. Single-crystal structure validation with the program PLATON[J]. J Appl Crystallogr, 2003, 36: 7-13. DOI:10.1107/S0021889802022112 |
 2017, Vol. 47
2017, Vol. 47