城市生活垃圾随意丢弃, 不仅占用土地资源, 而且污染环境[1]。利用热解技术研究城市生活垃圾高效转化对垃圾减容、减重具有重要意义。城市生活垃圾经过处理加工可制成RDF, 具有热值高、燃烧稳定和二噁英类物质排放量低等优点。褐煤具有易风化、易破碎等特点, 不利于长距离运输, 长期以来未能得到有效的利用, 因此低品质褐煤热解技术在能源短缺的背景下具有很大的优势。研究RDF与褐煤共热解能提高资源的经济效益, 在缓解“垃圾围城”带来的一系列问题的同时, 也能更好地理解RDF与煤的热解过程, 为其工业化热处置和新型能源工艺提供理论参考。
现有对RDF的研究主要集中在RDF单独热解。李延吉[2]和Efika[3]等研究了不同工艺条件对RDF的热解特性的影响。
最新研究发现, RDF与褐煤在共热解过程中, RDF中的微量元素及碱金属元素对褐煤具有催化作用[4]。何立模[5]、熊杰[6]等利用水洗、酸洗和碱金属浸渍样品, 发现酸洗样品气体产量(H2O,CO2,CO,CH4等)明显低于水洗样品和原样。Capablo[7]研究了生物质在锅炉表面碱盐沉积物的形成。Wu[8]和Shearer[9]通过对生物质与煤混烧, 分别研究了在富氧和富燃料情况下KCl和KOH气体释放以及共烧飞灰。Fatehi[10]和Saddawi[11]分别研究了碱金属在生物质中释放动力学分析和生物质热分解动力学分析。
现有关于碱金属对RDF与褐煤共热解催化特性的研究鲜有报道。在前述工作中发现RDF与褐煤在共热解过程中存在协同反应, 同时在RDF与褐煤质量配比为3:7时共热解轻质气体析出峰值最大, 协同作用反应最为明显[12], 因此取RDF与褐煤质量比为3:7。本文针对该质量配比, 利用XRF对RDF、褐煤及质量比为3:7的样品进行灰成分分析。对样品进行酸洗处理, 并以K,Na碱金属溶液浸渍, 利用TG-FTIR在线分析不同碱金属浸渍后RDF与褐煤共热解过程气体析出特性。
1 实验过程 1.1 实验样品制备RDF物质组成如表 1[13]所示, 从表 1可知RDF组成中纸、塑料成分相对比重较高。按照文献[13]中RDF-5分类要求, 去除金属和玻璃成分, 做成RDF-5样品[14]。为保证样品的可靠性, 将样品研磨粉碎筛分至0.074mm, 利用磁力搅拌机充分混合后, 平铺成圆形, 分成4等分, 取相对两份混合, 然后再平分, 直到达到四分法规定要求。
|
|
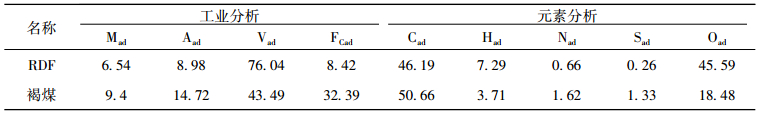
表 1 RDF物质组成 Tab. 1 The composition of RDF |
利用德国Elementar公司Vario Mac元素分析仪进行元素分析, 利用南京电炉厂马弗炉(GB/T 28731-2012标准)进行工业分析, 如表 2所示。
|
|
表 2 RDF与褐煤的工业分析与元素分析 Tab. 2 Proximate and ultimate analysis of RDF and lignite |
利用XRF分析需对样品进行灰处理, 遵照煤制灰标准(GB/T212-2001)确定灰化温度为815℃, 将粉碎后的样品放入南京电炉厂马弗炉灼烧1h后称量并观察灰皿内残留物, 元素组成及含量见表 3。
|
|
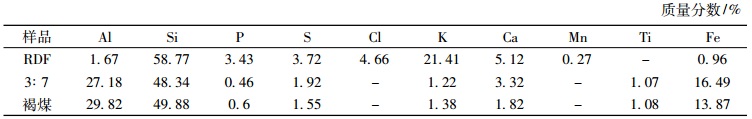
表 3 样品灰表面元素组成 Tab. 3 Composition and content of ash made by sample |
化学试剂为分析纯。利用摩尔分数为5%的硝酸, 将样品与硝酸以1:20(g/mL)的比例在恒温30℃, 160r/min的条件下浸泡24h, 并用去离子水反复洗涤至中性左右, 放入105℃烘箱内干燥; 浸渍时, 取酸洗烘干样品3g以1:20(g/mL)的比例浸渍于事先配制好的0.5mol/L的K,Na的氯化盐溶液中, 在磁力搅拌器中搅拌3h后过滤, 并用浸渍液反复冲洗以减少样品表面的金属盐, 抽滤后的样品放入105℃烘箱干燥。
1.4 仪器及实验条件实验仪器分别为耐驰公司热重分析仪(STA449F3)以及傅里叶变换红外光谱仪(Nicolet系列)。实验条件控制载气流量保持为30mL/min, 称取样品质量10mg, 实验温度范围为30~1 000℃, 反应升温速率为30℃/min。
2 结果与讨论 2.1 样品成分分析从表 2可知, RDF与褐煤主要元素组成为碳、氢及氧, 但RDF与褐煤成分具有较大区别。RDF挥发分含量较褐煤高, 固定碳含量少。RDF含氧量达45.59%(质量分数), 褐煤的含氧量为18.48%(质量分数), 说明RDF中含有较多的含氧官能团。RDF中含氮量和含硫量低于褐煤。
表 3为利用XRF分析出的各样品元素的定量组成, 由表 3可知, RDF与褐煤之间元素含量具有较大差异, 但主要元素种类没有发生大的波动, 主要含有Al,Si,P,S,K,Ca,Ti,Fe等元素。RDF与褐煤质量比为3:7时的元素组成与褐煤相似, 究其原因可能是该质量配比时褐煤含量较高所致。推测金属元素的催化作用是RDF与褐煤共热解发生协同反应的主要原因。
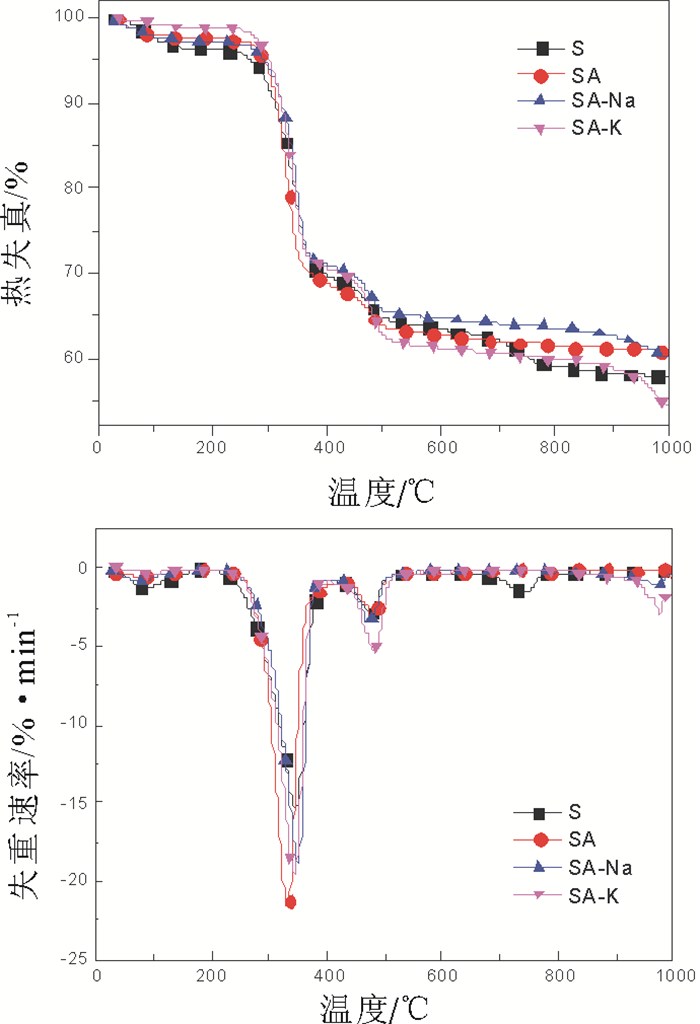
2.2 热解特性分析由图 1可知, 原样(S)、酸洗(SA)以及碱金属浸渍(SA-Na,SA-K)后具有相似的热解失重特性, 包括生物质组分热解(173~433℃)和塑料类物质热解(402~566℃)。但是,原样还存在无机碳酸盐热解过程, 酸洗后的样品不存在此阶段, 究其原因是酸洗去除了RDF和褐煤中的一些无机物成分(如纸中的碳酸钙)。从DTG曲线中可以发现酸洗样DTG曲线发生了较为明显的偏移量, K,Na金属浸渍样偏移量基本无变化, 最大失重速率(质量分数)的顺序为SA(21.517 9%/min)>SA-K(19.469 8%/min)>SA-Na(18.841 6%/min)>S(15.393 9%/min), 究其原因可能是酸洗后金属盐含量很低, 而金属盐有利于共热解过程中不同官能团的交联反应, 保持反应热稳定性, 这与文献[15]结论一致。在950℃左右, SA-K和SA-Na样品DTG曲线发生失重, 文献[16]以N2作为载气, 升温至900℃并恒温数分钟后通入空气燃尽试样, 发现热解过程中残留物为有机物, 燃烧后残留组分主要为灰分。
|
图 1 样品的TG和DTG曲线 Fig. 1 The TG and DTG curves of sample |
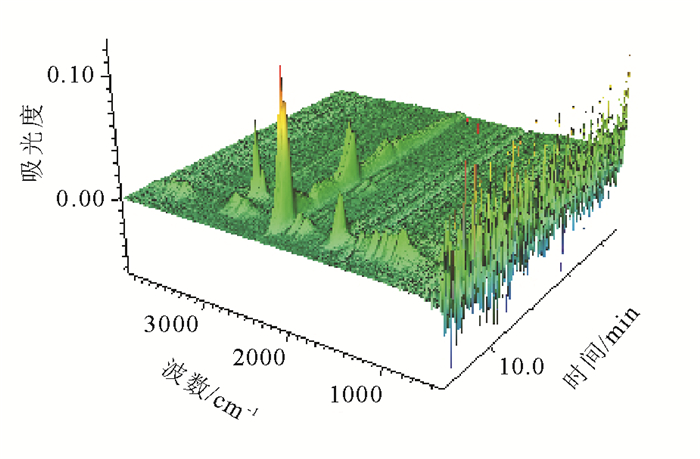
图 2为原样热解气体产物的三维图谱, 由图 2可知, RDF与褐煤共热解初期析出阶段的热解产物成分较为复杂, 具有较强的轻质气体(H2O,CO2,CO和CH4)以及醛、酮、酸和酚类等典型焦油类组分的吸收峰; 中期以塑料类高分子聚合物发生脱链解聚反应为主, 存在C—C键断裂反应后的烃族类的二次分解[17], 具有较强的CH4和CO2吸收峰; 热解后期以较强的CO2吸收峰为主。
|
图 2 原样热解气体产物的三维图谱 Fig. 2 Three-dimensional map of pyrolysis gas product |
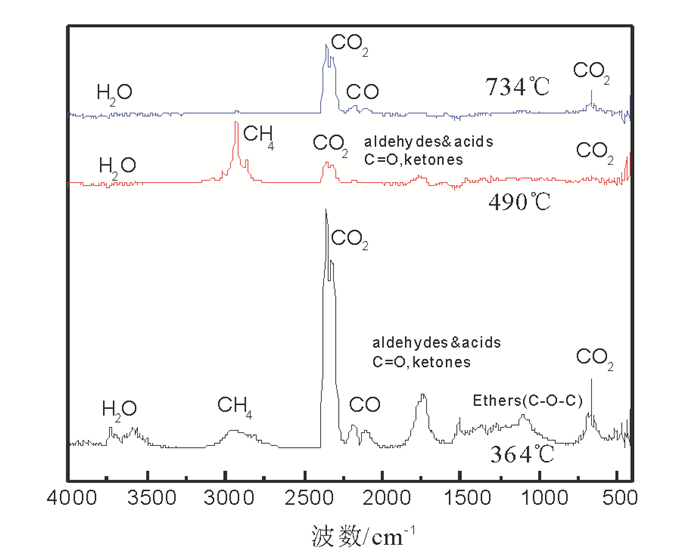
通过FTIR实验可以发现FTIR吸收峰与DTG曲线变化一致, 原样对应3个波峰, 酸洗及碱金属浸渍对应两个波峰。图 3所示为原样热解的3个失重阶段(364℃,490℃和734℃)的红外谱图, 具体析出物质已在图中标出。
|
图 3 364℃,490℃和734℃时共热解释放气体的红外谱图 Fig. 3 The release gas infrared spectrum of co-pyrolysis when the temperature were 364℃, 490℃ and 734℃ |
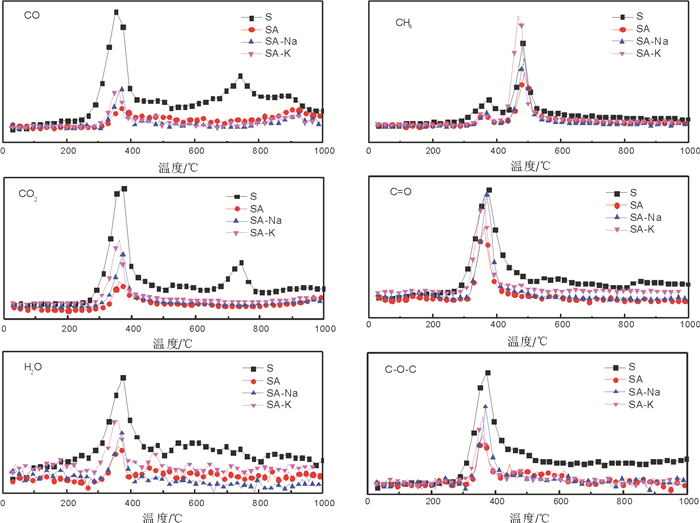
图 4为碱金属浸渍热解气体产物的FTIR曲线。根据兰伯特-贝尔定律, 特定波段的光谱强度正比于对应气体浓度,因此,图 4也反应了气体浓度变化趋势[19]。由此可知, 热解气体产物FTIR曲线中原样析出峰值最大, 碱金属K,Na浸渍样峰值要高于酸洗样析出峰值。究其原因可能是金属盐对RDF与褐煤共热解具有催化作用。金属盐的加入改变了一些活性中间大分子聚合物的裂解途径, 金属离子催化或抑制某些化学反应从而影响热解过程产生催化作用[20]。同时,部分金属盐吸附在褐煤表面, 改变了褐煤本身的表观孔隙结构, 阻碍颗粒的升温过程, 降低升温速率, 低升温速率能有效提高固定炭产率。碱金属盐通过吸附在褐煤表面改变孔隙结构, 阻塞挥发分析出, 将有利于气体产物的二次分解, 从而促进焦炭的生成[21]。
|
图 4 碱金属浸渍热解气体产物FTIR曲线 Fig. 4 FTIR curves of pyrolysis gas products impregnated by alkali metal |
从图 4中的CO2和CO的气体产物FTIR曲线可知, 原样呈双峰特性, 而酸洗和碱金属浸渍后的样品都呈单峰特性, 从DTG曲线中可以发现RDF和褐煤中一些无机物(如纸中的碳酸钙)热解发生在高温段(600~800℃), 酸洗去除了样品中的碳酸盐, 而CO在该温度段的产生主要是CO2与焦炭发生反应:C+CO2=2CO+171.5kJ/mol; 酸洗后CO2和CO析出单峰曲线主要集中在低温阶段生物质组分热解阶段(300~400℃)。在500~550℃时, 褐煤表面会形成阻碍气体逸出的气、液、固三相合一的胶质体, 由CO2的析出曲线可以发现, 原样在此温度区间存在1个不明显波峰, 而酸洗及添加碱金属K,Na对该温度区间产气特性无影响, 说明碱金属K,Na对胶质体无影响, 猜测影响其催化特性的金属可能为碱土金属[22]。
在C=O和C—O—C析出曲线中, SA-K浸渍气体产物要低于SA-Na浸渍, 而CO2,CO析出曲线中呈现相反的规律, 究其原因可能是碱金属盐K和Na能促进半挥发性有机物(C=O和C—O—C)和CH4的催化裂解和催化重整, 生成CO2和CO, 这与文献[5]结论一致。CO析出主要为C—O—C和C=O断裂产生, CO2主要为C=O和COOH断裂和重整[23]。CH4的析出主要集中在300~500℃, 呈双峰特性, 分别对应O—CH3官能团的断裂和塑料类物质的分解(伴随部分醛、醇、酸和酮等有机物发生了二次分解)[24-26]。在CH4析出曲线中, SA-K浸渍气体产物最高, 究其原因可能是碱金属K对共热解催化特性强于Na。H2O吸收峰的吸光度在370℃附近达到峰值, 这是由于样品内部的脱水反应造成的。
3 结论1) RDF与褐煤之间元素组成含量具有较大差异, 但主要元素种类没有发生大的波动, 主要含有Al,Si,P,S,K,Ca,Ti,Fe等元素。RDF与褐煤质量比为3:7时的元素组成与褐煤相似。
2) 酸洗能去除样品中的无机碳酸盐, 酸洗以及碱金属浸渍的样品具有相似的热解失重特性, 包括生物质组分热解(173~433℃)和塑料类物质热解(402~566℃), 却不存在碳酸盐热解阶段。
3) DTG曲线中最大失重速率(质量分数)呈现SA(21.5179%/min)>SA-K(19.4698%/min)>SA-Na(18.8416%/min)>S(15.3939%/min)。酸洗样较原样DTG曲线发生了较为明显的偏移量, K,Na金属浸渍样偏移量基本无变化。
4) 金属K和Na的催化作用是RDF与褐煤共热解协同反应的原因。RDF与褐煤共热解气体产物主要为轻质气体(CO,CO2,CH4,H2O)及半挥发性有机物(C=O和C—O—C)。气体产物FTIR析出曲线中原样气体峰值浓度最高, 碱金属K,Na浸渍样气体峰值浓度次之, 酸洗样气体峰值浓度最低。
| [1] |
王临清, 李枭鸣, 朱法华, 等. 中国城市生活垃圾处理现状及发展建议[J]. 环境污染与防治, 2015, 37(2): 106-109. |
| [2] |
李延吉, 邹科威, 姜璐, 等. 垃圾衍生燃料焚烧污染物排放实验与模拟[J]. 浙江大学学报(工学版), 2014, 48(7): 1254-1259. |
| [3] |
EFIKA E C, ONWUDILI J A, WILLIAMS P T. Products from the high temperature pyrolysis of RDF at slow and rapid heating rates[J]. Analytical and Applied Pyrolysis, 2014, 34: 402-410. |
| [4] |
SISTER V G, LUGOVOI Y V, KOSIVTSOV Y Y, et al. Catalytic pyrolysis of polymeric mixtures[J]. Russian Journal of Physical Chemistry A, 2011, 85(6): 1091-1093. DOI:10.1134/S003602441106029X |
| [5] |
何立模, 胡松, 孙路石, 等. 基于TG-FTIR的生物质内在金属盐催化热解研究[J]. 工程热物理学报, 2014, 35(10): 2093-2096. |
| [6] |
熊杰, 周志杰, 许慎启, 等. 碱金属对煤热解和气化反应速率的影响[J]. 化工学报, 2011, 62(1): 192-198. |
| [7] |
CAPABLO J. Formation of alkali salt deposits in biomass combustion[J]. Fuel Processing Technology, 2016, 153: 58-73. DOI:10.1016/j.fuproc.2016.07.025 |
| [8] |
WU Dongyin, WANG Yuhao, WANG Yang, et al. Release of alkali metals during co-firing biomass and coal[J]. Renewable Energy, 2016, 96: 91-97. DOI:10.1016/j.renene.2016.04.047 |
| [9] |
SHEARER C R, PROVIS J L, BERNAL S A, et al. Alkali-activation potential of biomass-coal co-fired fly ash[J]. Cement and Concrete Composites, 2016, 73: 62-74. DOI:10.1016/j.cemconcomp.2016.06.014 |
| [10] |
FATEHI H, LI Z S, BAI X S, et al. Kinetics of alkali metal release during biomass pyrolysis[J]. Proceedings of the Combustion Institute, 2016, 36: 2243-2251. |
| [11] |
SADDAWI A, JONES J M, WILLIAMS A. Influence of alkali metals on the kinetics of the thermal decomposition of biomass[J]. Fuel Processing Technology, 2012, 104: 189-197. DOI:10.1016/j.fuproc.2012.05.014 |
| [12] |
刘成, 刘亮, 尹艳山, 等. TG-FTIR研究垃圾衍生燃料轻质气体析出特性[J]. 燃烧科学与技术, 2017, 23: 1-7. |
| [13] |
余渡江.垃圾衍生燃料(RDF)流化床空气气化特性的实验研究[D].杭州: 浙江大学, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10335-1014162708.htm
|
| [14] |
HOU S S, CHEN M C, LIN T H, et al. Experimental study of the combustion characteristics of densified refuse derived fuel (RDF-5) produced from oil sludge[J]. Fuel, 2014, 116: 201-207. DOI:10.1016/j.fuel.2013.08.001 |
| [15] |
JAKAB E, MESZARONS E, BORSA J. Effect of slight chemical modification on the pyrolysis behavior of cellulose fibers[J]. Analytical and Applied Pyrolysis, 2010, 87(1): 117-123. DOI:10.1016/j.jaap.2009.10.012 |
| [16] |
牛淼淼, 黄亚继, 金保昇, 等. 鼓泡流化床垃圾衍生燃料富氧气化[J]. 化工学报, 2014, 65(12): 4971-4977. |
| [17] |
桑圣欢, 段钰锋, 陈惠超, 等. 热重-红外联用分析纸厂废弃塑料的热解特性[J]. 环境科学与技术, 2013, 36(2): 159-163. DOI:10.3969/j.issn.1003-6504.2013.02.033 |
| [18] |
翁诗甫. 傅里叶变换红外光谱分析[M]. 北京: 化学工业出版社, 2010.
|
| [19] |
车德勇, 孙艳雪, 孙佰仲, 等. 木质素热解气相产物释放特性实验研究[J]. 中国电机工程学报, 2015, 35(24): 6439-6444. |
| [20] |
刘金淼, 马欣欣, 黄燕, 等. 碱/碱土金属浸渍对酸洗生物质热解影响研究[J]. 北京化工大学学报(自然科学版), 2015, 42(5): 25-31. |
| [21] |
MANYÀ J J, GARCÍA-CEBALLOS F, AZUARA M, et al. Pyrolysis and char reactivity of a poor-quality refuse-derived fuel (RDF) from municipal solid waste[J]. Fuel Processing Technology, 2015, 140: 276-284. DOI:10.1016/j.fuproc.2015.09.014 |
| [22] |
赵淑蘅, 蒋剑春, 孙云娟, 等. 稻壳与褐煤共热解过程的TG-FTIR分析[J]. 煤炭转化, 2013, 36(1): 19-23. DOI:10.3969/j.issn.1004-4248.2013.01.005 |
| [23] |
车德勇, 蒋文强. 基于TG-FTIR分析的稻壳热解特性实验[J]. 中国农机化学报, 2016, 37(5): 241-247. |
| [24] |
白小元, 车德勇, 蒋文强, 等. 纤维素热解的TG-FTIR分析[J]. 可再生能源, 2015, 33(10): 1582-1588. |
| [25] |
柏继松, 余春江, 吴鹏, 等. 热重-红外联用分析垃圾衍生燃料的热解特性[J]. 化工学报, 2013, 64(3): 1042-1048. DOI:10.3969/j.issn.0438-1157.2013.03.036 |
| [26] |
YANG Haiping, YAN R, CHEN Hanping, et al. Characteristics of hemicellulose, cellulose and lignin pyrolysis[J]. Fuel, 2007, 86(12-13): 1781-1788. DOI:10.1016/j.fuel.2006.12.013 |
 2017, Vol. 47
2017, Vol. 47
 , 尹艳山, 龚千代, 艾锦瑾, 蔡宜捷
, 尹艳山, 龚千代, 艾锦瑾, 蔡宜捷