2. 渭南师范学院军民两用材料重点实验室,陕西 渭南 714099
2. Key Laboratory of Materials for Military and Civil,Weinan Normal University,Weinan 714099,China
盖玻片在医疗和生化研究中是常见的片基,因其在生产中有污物残留,且在存放过程中表面经常会滋生霉菌而影响其表面性能和透光度,故而在使用前需要进行表面处理以达到清洁和改善亲水性的效果[1-2]。普通清洗常用洗洁精溶液进行,但只能洗掉盖玻片表面的有机物等污物而不能提高其亲水性,化学清洗和表面等离子体处理可以提高盖玻片的亲水性,相比而言,化学清洗以其方便、灵活而被广泛使用[1]。化学清洗一般利用酸性或碱性腐蚀性溶液的羟基化作用提高玻璃表面的亲水性,例如,食人鱼溶液、氨水双氧水溶液、盐酸双氧水溶液等[1, 3-6]。
Fenton试剂是由H2O2和催化剂Fe2+构成的氧化还原性溶液,体系中Fe2+与H2O2能迅速反应并产生具有很强氧化能力的羟基自由基(·OH)。·OH能使大多数有机物降解和矿化,尤其对毒性大、一般氧化剂难以氧化或生化难降解的有机废水具有较强的氧化能力和较高的降解率[7],因此,Fenton试剂常被用在有机废水的处理中,以氧化降解水中的有机污物[8-11]。Fenton试剂的反应机理为[12-13]:
Fe2++H2O2→Fe3++OH-+·OH
Fe2++·OH→Fe3++OH-
Fe3++H2O2→Fe2++HO2·+H+
HO2·+H2O2→O2+H2O+·OH
鉴于Fenton试剂能够产生高活性的·OH,而·OH可能与玻璃表面的SiO2发生羟基化作用,有望改善盖玻片的亲水性。本研究探索采用Fenton试剂对盖玻片进行亲水性处理的可行性及方法,通过测试不同配比的Fenton试剂浸泡盖玻片一定时间后对水的动态接触角(DCA)来表征盖玻片的亲水性,该研究未见报道。
1 实验部分 1.1 仪器与试剂DCAT11表面张力仪(德国Dataphysics公司),TXH-05低温恒温循环器(宁波天恒仪器厂),PB-10酸度计(德国Sartorius公司),WSZ-100A回旋振荡器(上海一恒科技有限公司),GZY-P60-V超纯水制备系统(湖南科尔顿水务有限公司),BK-124001数显游标卡尺(美国邦克公司),SB75吹风机(上海超人电器有限公司)。
洗洁精(立白),30%H2O2、浓H2SO4、硫酸亚铁(FeSO4·7H2O)皆为分析纯,超纯水(自制,电阻率18.25MΩ·cm,表面张力72.8mN/m),盖玻片(24mm×24mm×0.17mm,上海帆船)。
1.2 盖玻片的表面处理 1.2.1. 表面清洁取盖玻片若干,在用洗洁精溶液浸泡的同时在回旋振荡器(190 r·min-1)上摇振30 min,然后用自来水冲洗至无泡,再用超纯水反复冲洗至水的电导率接近超纯水的电导率,冷风吹干后测试DCA。
1.2.2. 表面亲水性处理将30%的H2O2稀释至浓度为0.1mol·L-1,与浓度为0.1mol·L-1的FeSO4溶液分别以2∶1、1∶1、1∶2(v/v)混合,这3种配比的Fenton试剂依次标记为C1、C2、C3,各溶液的pH值依次为1.65、1.69、1.76,颜色皆为酒红色,且颜色随着FeSO4浓度的增加逐渐加深。将表面清洁后的盖玻片分别浸泡在现配的3种配比的Fenton试剂中,置于回旋振荡器上摇振(190r·min-1),于1h、2h、4h、8h和12h分别取出若干片,经自来水洗、超纯水洗、冷风吹干之后测试DCA。然后,再将盖玻片用洗洁精溶液浸泡洗涤30min,最后用食人鱼(H2O2∶H2SO4=7∶3(v/v))浸泡30min,经自来水洗、超纯水洗、冷风吹干之后测试DCA。
1.3 亲水性测试用表面张力仪测试盖玻片对水的DCA,采用Wilhelmy吊片法[14],测试条件及数据处理方法同课题组以前的报道[1, 15-16],在DCA曲线中取2个循环的前进角(θA)和后退角(θR),以浸入深度在4~6 mm范围内的平均值作为样片对水的接触角数值。
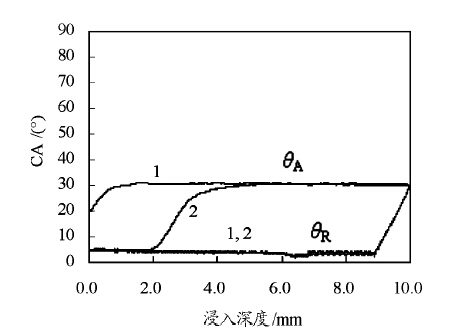
2 结果与讨论 2.1 表面清洁经洗洁精溶液洗涤后的盖玻片为无色透明,其DCA曲线如图 1所示,θA和θR的平均值分别为30.7°和5.2°,由此可见,表面清洁后的盖玻片有一定的亲水性。
|
图 1 洗洁精溶液洗涤后的DCA曲线 图中1代表DCA测试的第一循环,2代表第二循环 |
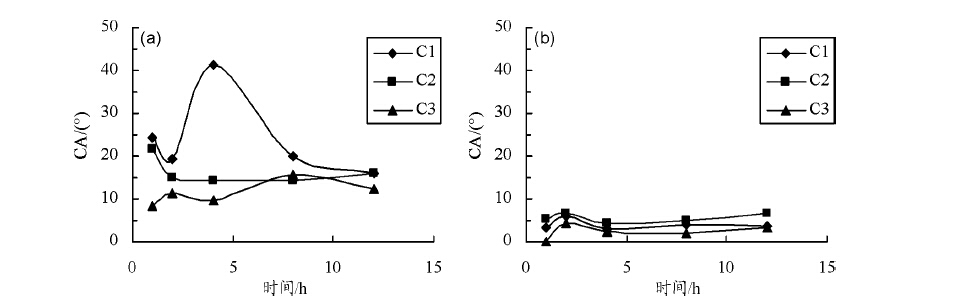
由三种配比的Fenton试剂浸泡洗涤1~12 h之后的盖玻片的θA和θR的变化趋势如图 2所示,对应的数据见表 1,盖玻片对应的颜色如图 3所示。
| 表 1 不同浓度Fenton试剂洗涤盖玻片的θA和θR |
|
图 2 不同浓度Fenton试剂洗涤盖玻片的接触角(a)θA和(b)θR |

|
图 3 Fenton试剂处理后的盖玻片颜色图 (第1列为经洗洁精溶液洗涤后的盖玻片,第2~6列分别代表再经Fenton试剂浸泡洗涤1、2、4、8、12 h后,第7列代表第6列盖玻片再经洗洁精溶液浸泡30 min后,第8列代表第7列盖玻片再经食人鱼溶液浸泡洗涤30 min后) |
由图 2和表 1可见,不同浓度的Fenton试剂浸泡处理一定时间皆能使盖玻片的θA和θR有不同程度的减小,其中配比为H2O2∶FeSO4=1∶2 (v/v)的Fenton试剂对盖玻片浸泡处理1 h的亲水性效果最佳,H2O2∶FeSO4=1∶1 (v/v)的Fenton试剂处理2 h的亲水性效果次之,H2O2∶FeSO4=2∶1 (v/v)的Fenton试剂处理2 h处理效果最差;随着Fenton试剂浸泡时间的延长,盖玻片的θA和θR都有所增大,即亲水性变差。此外,随着浸泡洗涤时间的延长,盖玻片之间的摩擦使其容易磨损、破碎,所以洗涤时间不宜过长。
如图 3所示,Fenton试剂浸泡处理过的盖玻片表面呈黄色,随着FeSO4浓度的增大,黄色加深;随着浸泡时间的延长,黄色变浅。结合图 2和表 1可知,盖玻片表面的黄色越重,其亲水性越好。
2.3 盖玻片表面亲水性原因分析据Fenton试剂的反应机理推测,Fenton试剂对盖玻片亲水性的改善可能与盖玻片表面键合·OH以及吸附Fe(OH)3胶体和Fe3+有关。Fenton试剂反应过程中有大量·OH生成,·OH的反应活性很高,可以与盖玻片表面SiO2反应而形成Si-OH,这会增加盖玻片的亲水性。随着催化氧化反应的不断进行,反应生成的Fe3+和OH-会逐渐增多,且体系的pH值会随之上升,一定酸度条件下,会形成Fe(OH)3胶体[17],Fe(OH)3胶体和Fe3+吸附在盖玻片表面,这导致盖玻片表面颜色变黄;同时,由于Fe(OH)3胶体多羟基结构和Fe3+的粒子性质会大大增加盖玻片的亲水性。在长时间振荡洗涤中,盖玻片相互摩擦会使部分吸附不牢固的Fe(OH)3胶体和Fe3+脱落而导致表面黄色变浅,亲水性也略变差。
Fenton试剂浸泡处理后的盖玻片虽然亲水性有所改善,但表面的黄色影响其透光性,故考虑一般使用时必须除去。虽然长时间振荡洗涤会使颜色变浅,但盖玻片的摩擦破损率过高,影响其表面的光滑、平整,且费时费力,不适合使用。有色盖玻片用洗洁精溶液洗涤30 min后,颜色依旧(见图 3中第7列盖玻片),这表明Fe(OH)3胶体和Fe3+与盖玻片之间的吸附作用力较强。据报道,食人鱼溶液浸泡处理盖玻片能够除去其表面金属离子,且对其表面亲水性有所改善[1, 3],本研究将有色的盖玻片在H2O2∶H2SO4=7∶3 (v/v)的食人鱼溶液中浸泡几分钟,表面铁黄色就逐渐褪去,浸泡30 min则可完全除去,盖玻片又恢复无色透明(见图 3中第8列盖玻片);然而,经食人鱼溶液浸泡后,盖玻片的接触角有所增大,且其亲水性变差(见表 2),尤其经H2O2∶FeSO4=1∶2 (v/v)的Fenton试剂处理的盖玻片(图 3中C3(7) 片)在食人鱼溶液处理前后的接触角变化很大,即Fenton试剂中FeSO4的浓度越大,其浸泡处理的盖玻片的亲水性越好。这就间接证明了Fe(OH)3胶体和Fe3+的大量吸附导致盖玻片表面亲水性显著提高,且Fe(OH)3胶体和Fe3+在盖玻片表面的吸附作用力确实很强。
| 表 2 Fenton试剂洗涤12 h后经食人鱼溶液浸泡30 min的盖玻片的θA和θR Table 2 英文标题 |
综上所述,Fenton试剂处理盖玻片可以改善其亲水性,但改善的主要原因是Fe3+在盖玻片表面的吸附、沉积,而非预测的表面羟基化作用,但也不能排除有表面羟基化作用的影响。虽然Fenton试剂对盖玻片亲水性的改善比食人鱼溶液的作用效果要好,但却对透光性不利,这就限制了该方法的使用。
3 结论研究Fenton试剂浸泡洗涤对盖玻片表面亲水性的影响。采用Wilhelmy吊片法测试盖玻片对水的动态接触角,研究0.1mol·L-1的H2O2和0.1mol·L-1的FeSO4的配比分别为2∶1、1∶1、1∶2(v/v)的Fenton试剂浸泡不同时间时盖玻片表面亲水性的效果和变化规律。结果发现,Fenton试剂浸泡洗涤能够改善盖玻片表面的亲水性,其主要原因是表面吸附,沉积了大量Fe3+;Fenton试剂中FeSO4的浓度越大,盖玻片的亲水性越好。Fenton试剂虽可改善盖玻片的亲水性,但Fe3+的黄色影响其透光性,故用Fenton试剂对盖玻片进行亲水性处理的方法应用受限。
| [1] | 杨珊, 王鹏, 崔颖鲁, 等. 化学清洗及干燥方法对盖玻片亲水性的影响[J]. 应用化工, 2014, 43(10): 1796–1799. |
| [2] | 王鹏. 盖玻片清洗方法比较[J]. 诊断病理学杂志, 2015, 22(10): 651. |
| [3] | UIC Environmental Health and Safety Office. Piranha solution[EB/OL].(2012-12-26)[2015-06-05]. University of Illinois at Chicago. http://www.uic.edu/depts/envh/HSS/Documents/PiranhaSolutionSafetyFactSheet.pdf. |
| [4] | 刘虹, 高志贤, 王源升, 等. 基于蛋白A定向固定的Love波免疫传感技术研究[J]. 分析化学, 2006, 34. |
| [5] | Chaikin Y, Kedem O, Raz J, et al. Stabilization of metal nanoparticle films on glass surfaces using ultrathin silica coating[J]. Anal Chem, 2013, 85(21): 10022–10027. DOI:10.1021/ac402020u |
| [6] | SFEZ R, LIU D Z, TURYAN I, et al. Polyaniline monolayer self-assembled on hydroxyl-terminated surfaces[J]. Langmuir, 2001, 17(9): 2556–2559. DOI:10.1021/la001343d |
| [7] | 陈华军, 尹国杰. Fenton及类Fenton试剂的研究进展[J]. 洛阳工业高等专科学校学报, 2007, 17(3): 1–4. |
| [8] | Barbusiński K. Toxicity of industrial wastewater treated by Fenton's reagent[J]. Polish J Environ Stud, 2005, 14(1): 11–16. |
| [9] | 武智, 石晶晶, 陈旭东. Fenton试剂氧化法在工业废水处理中的研究及应用进展[J]. 河北化工, 2009, 32(1): 61–63. |
| [10] | 吴丽雅, 宋秀兰, 林金华. Fenton试剂法深度处理焦化废水的研究及产物分析[J]. 科学技术与工程, 2015, 15(9): 271–274. |
| [11] | 郑先强, 尤特, 唐运平. Fenton试剂预处理化工综合废水的研究[J]. 环境工程学报, 2011, 5(10): 2226–2232. |
| [12] | Bossmann S H, Oliveros E, Göb S, et al. New evidence against hydroxyl radicals as reactive intermediates in the thermal and photochemically enhanced Fenton reactions[J]. J Phys Chem A, 1998, 102(28): 5542–5550. DOI:10.1021/jp980129j |
| [13] | Chen R, Pignatello J J. Role of quinone intermediates as electron shuttles in Fenton and photoassisted Fenton oxidations of aromatic compounds[J]. Environ Sci Technol, 1997, 31(8): 2399–2406. DOI:10.1021/es9610646 |
| [14] | HAYES R A, ROBINSON A C, RALSTON J A. Wilhelmy technique for the rapid assessment of solid wetting dynamics[J]. Langmuir, 1994, 10(8): 2850–2852. DOI:10.1021/la00020a057 |
| [15] | 杨珊, 宫永宽. 精确测定表面动态接触角的方法及影响因素[J]. 西北大学学报, 2011, 41(5): 821–826. |
| [16] | 杨珊,宫永宽.影响吊片法测试动态接触角的因素分析及数据处理程序的设计[EB/OL].(2010-08-26)[2015-06-05]. 中国科技论文在线,http://www.paper.edu.cn. |
| [17] | 张萍, 顾国维, 扬海真. Fenton试剂处理垃圾渗滤液技术进展的研究[J]. 环境卫生工程, 2004, 12(1): 28–31. |
 2016, Vol. 31
2016, Vol. 31