便血是慢性放射性肠病(chronic radiation enteropathy, CER)出血常见症状和就诊的主要原因,患者出血为顽固性的,常需要频繁输血,目前缺乏有效的治疗方法[1-4]。本研究对2008年6月至2016年10月42例CRE出血患者,应用结肠镜黏膜下药物注射联合氩离子凝固(argon plasma coagulation, APC)止血并进行随访,以观察疗效和治疗的安全性。
1 资料与方法 1.1 临床资料本组42例,均为妇科肿瘤放射治疗后并发CRE出血,年龄32-83岁,平均56.5岁。其中29例病变累及直肠,9例累及直肠和乙状结肠,4例仅累及乙状结肠。所有患者均经过水杨酸制剂、糖皮质激素、凝血酶等药物灌肠或口服治疗,3例还行高压氧治疗,仍有活动性出血和不同程度的贫血,其中34例需要每月甚至每周输血。所有病例血小板计数和凝血功能正常,无肠瘘和影响肠镜视野的肠狭窄,亦无结肠镜检查禁忌证。
1.2 治疗前后检查与评估治疗前后检查血常规和结肠镜,记录每天便血次数和出血量。根据治疗前后出血情况(便血次数和便血量)、血红蛋白(Hb)水平和结肠镜表现评估治疗效果[5]。
1.3 器材Olympus CF-Q260 AI结肠镜,ERBE APC 2氩离子凝固器;Olympus PW-52-1喷洒管,Olympus NM-200L-0432注射针,1 mg (1 ml)去甲肾上腺素加入100 ml 0.9%氯化钠注射液中,配成1%去甲肾上腺素生理盐水溶液。
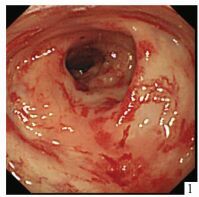
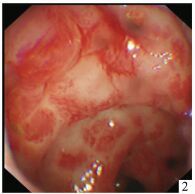
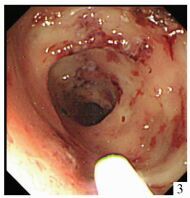
1.4 治疗方法CRE病变表现为黏膜弥漫性脆性增加,接触易出血,散在或密集的毛细血管扩张,呈草莓样改变,见图 1,部分患者有溃疡形成,溃疡边缘或基底有活动性出血。在内镜直视下,用内镜注射针将1%去甲肾上腺素生理盐水溶液,在病变范围内间隔3.0-5.0 cm黏膜下多点注射至黏膜明显抬起,见图 2。反复冲洗病灶后,用APC凝固扩张的毛细血管,见图 3,设定功率40 W,氩气流量1.6-2.0 L/min,距离病灶3-5 mm喷洒,时间1-3 s。溃疡边缘出血可用上述方法止血,但APC凝固时间限定为1 s,管头距病灶5 mm;基底部出血只能局部喷洒去甲肾上腺素或凝血酶等药物。
|
图 1 内镜治疗前大肠黏膜像:质脆,毛细血管扩张 |
|
图 2 黏膜下注射后大肠黏膜像:黏膜抬起 |
|
图 3 APC后大肠黏膜像:毛细血管凝固 |
1周内减少活动。3 d内流质饮食,2周内无渣饮食。应用抗生素3-5 d预防感染。
1.6 术后随访随访3-94个月,平均68.5个月,观察便血次数和量、Hb水平和肠镜表现。第1次随访应在治疗结束1月后,以后分别在3月、6月、12月,1年后为每6月或12月。
1.7 统计学方法数据用SPSS 13.0软件进行分析。计数资料用χ2检验,计量资料用配对t检验,内镜变量用Wilcoxon秩和检验。以P<0.05为差异有统计学意义。
2 结果 2.1 治疗前后便血和Hb量的变化见表 1。42例中有35例1次治疗即有效,7例行2次治疗后5例有效。
| 表 1 42例CRE出血治疗前后便血和Hb变化 |
内镜下黏膜脆性分级,见表 2[5]。患者治疗前后内镜表现,见图 1-5, 表 3。
|
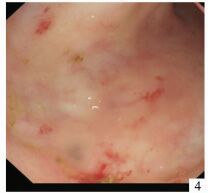
图 4 治疗后1年大肠黏膜像:扩张的毛细血管团基本消失,黏膜脆性减少,黏膜下机化(抬举征阴性,注:图中出血处为注射点) |

|
图 5 治疗后2年大肠黏膜像:黏膜变薄,毛细血管网减少 |
| 表 2 内镜下黏膜脆性分级 |
| 表 3 42例CRE治疗前后内镜表现(例) |
治疗有效的标准[5]:① 便血次数≤3次/d及出血量≤10 ml/d; ② Hb上升≥30.0 g/L; ③ 病变面积减少75%及黏膜脆性减少,即视为有效。42例第1次治疗有效率为83.3%(35/42),第1次、2次总有效率为95.2%(40/42);2例无效系溃疡基底部出血所致,排除该2例1次治疗有效率达87.5%(35/40),总有效率可达100%(40/40)。
2.4 并发症5例发生APC相关性浅溃疡,发生率为11.9%,无出血和穿孔风险。3例病变累及齿状线附近,治疗后有一过性里急后重或肛门痛,1月后症状逐渐消失。
2.5 随访40例治疗有效者随访期间无活动性出血或少量便血,其中21例随访超过5年仍维持缓解,所有病例随访期间均未输血。2例无效者便血次数及量明显减少,1-2次/年。治疗结束后1月复查结肠镜,治疗相关性溃疡愈合,6个月后2例原CRE溃疡面积缩小。
3 讨论出血性CRE及其相关性贫血极其顽固,严重影响患者的身心健康和生活质量,国内外尝试用药物(水杨酸制剂、糖皮质激素、短链脂肪酸等)灌肠或口服、甲醛烧灼、高压氧治疗和外科手术等,止血的有效性和安全性尚待肯定[1, 3, 4]。本级42例均经过1个月以上的药物治疗,部分还配合高压氧治疗仍无明显缓解。有报道APC用于CRE止血,便缺乏大宗且系统性临床观察,并发症和远期效果未明[3, 4]。
CRE出血的主要原因是病变黏膜弥漫性的脆性增加和畸形的毛细血管扩张(见图 1),少数与并发的溃疡有关。本文首先采用黏膜下注射1%去甲肾上腺素生理盐水溶液,使病变范围内黏膜充分抬起(见图 2),以达到压迫止血,去甲肾上腺素还有收缩血管作用。随访发现,经过注射治疗的病变黏膜下组织机化(抬举征阴性),黏膜变薄(见图 4, 5)。注射治疗作用面积大,主要用于黏膜弥漫性脆性增加和出血,对扩张的毛细血管作用短暂。APC作用面积有限,但对扩张的毛细血管凝固作用明显且持久(见图 3)。药物注射与APC结合应用于不同病变,以提高止血效果。本组42例1次治疗有效率83.3%,加上第2次治疗可达95.2%,排除2例合并溃疡出血者,1次治疗有效率达87.5%,2次治疗的总有效率达100%,均优于文献报道[2, 6]。
黏膜下药物注射对黏膜损伤小,如果操作规范(确保药物注入黏膜下)无并发症发生,但本组有3例病变累及齿状线附近,治疗后有一过性里急后重或肛门痛,可能与黏膜下注射刺激肛门括约肌有关,1月后可自行缓解。APC的并发症包括肠腔狭窄、溃疡、肠穿孔、瘘形成、气体爆炸等,发生率为20%-25%[1, 7];本组仅见5例APC相关溃疡,发生率为11.9%,低于文献报道[1, 7],且溃疡浅小。APC并发症的主要原因是功率过大,喷管头距黏膜太近或直接接触,凝固时间太长。本研究APC前用黏膜下注射,使黏膜与固有肌分离,减少APC对肠壁的损伤。对于CRE并溃疡出血,如果溃疡边缘出血,可采用距边缘2 cm处黏膜下药物注射,距离病灶5 mm处氩气喷洒(流量1.6 L/min, 时间1 s),避免伤及基底部;对溃疡基底部出血的处理必须慎重以免穿孔,可用止血药局部冲洗。
有关CRE出血内镜治疗远期效果缺乏随访资料。本组42例正在随访中,40例随访期间维持临床缓解,其中21例缓解期超过5年,血红蛋白水平逐渐上升,均未再输血。2例合并溃疡出血者便血次数及量、输血次数明显减少。总之,黏膜下药物注射联合APC治疗CRE出血安全有效,但其有效性和安全性有赖于适应证的严格掌握和操作的规范化。本研究选择病例的标准:病灶以黏膜脆性增加和毛细血管扩张为主,无超过2.0 cm的深溃疡、肠瘘、影响肠镜操作视野的肠狭窄,血小板计数和凝血功能正常。
| [1] |
王磊, 马腾辉. 放射性肠炎的治疗现状[J].
中华胃肠外科杂志, 2010, 13(3): 878-880.
Wang L, Ma TH. Current treatment of radiation enteritis[J]. Chinese J Gastrointest Surg, 2010, 13(3): 878-880. |
| [2] | Weiner J, Schwartz D, Martinez M, et al. Long-term results on the efficacy of argon plasma coagulation for patients with chronic radiation proctitis after conventionally fractionated, dose-escalated radiation therapy for prostate cancer[J]. Inter J Radiat Oncol Biol, 2016, 93(3): s200. |
| [3] | Hanson B, Macdonald R, Shaukat A. Endoscopic and medical therapy for chronic radiation proctopathy: a systematic review[J]. Dis Colon & Rectum, 2012, 55(10): 1081-1095. |
| [4] | Rustagi T, Mashimo H. Endoscopic management of chronic radiation proctitis[J]. World J Gastroenterol, 2011, 17(41): 4554-4562. DOI: 10.3748/wjg.v17.i41.4554. |
| [5] | Latorre SM, Sempere GJ, Barceló CS, et al. Evaluation of the endoscopic response to argon plasma coagulation in patients with chronic radiation proctopathy[J]. Rev Esp Enferm Dig, 2008, 100(10): 619-624. |
| [6] | Hortelano E, Gómez-Iturriaga A, Ortiz-De-Zárate R, et al. Is argon plasma coagulation an effective and safe treatment option for patients with chronic radiation proctitis after high doses radiotherapy?[J]. Rev Esp Enferm Dig, 2014, 106(3): 165-170. |
| [7] | Sato Y, Takayama T, Sagawa T, et al. Argon plasma coagulation treatment of hemorrhagic radiation proctopathy: the optimal settings for application and long-term outcome[J]. Gastroint Endosc, 2011, 73(3): 543-549. DOI: 10.1016/j.gie.2010.11.015. |
 2017, Vol. 38
2017, Vol. 38
