2. 湖北省通城县人民医院麻醉科 湖北 通城 437400;
3. 武汉大学基础医学院病理学教研室,湖北 武汉 430071;
4. 武汉市妇女儿童医疗保健中心麻醉科 湖北 武汉 430010
2. Dept. of Anesthesiology, People's Hospital of Tongcheng County, Tongcheng 437400, Hubei, China;
3. Dept. of Pathology, Basic School of Medical Sciences, Wuhan University, Wuhan 430071, China;
4. Dept. of Anesthesiology, Wuhan Women and Children Health Care Center, Wuhan 430010, China
前列腺素是中枢神经系统对伤害性刺激起反应时, 机体产生的重要炎症介质,而布洛芬作为前列腺素的抑制剂,对疼痛的抑制和对机体的保护作用,需进一步探讨,本文观察布洛芬对经甲醛刺激后的大鼠脊髓背角神经元Fos蛋白表达的影响,探讨其在脊髓水平对伤害性刺激的抑制作用。
1 材料与方法 1.1 实验仪器与药品von Frey纤毛(美国Stoelting公司),布洛芬注射液(Caldolor)由美国坎伯兰制药公司提供,批号:031562AA,规格:4 ml:400 mg, 为无色澄明液体(C13H18O2),含量为102.0%。溶媒对照采用生理盐水注射液,由华润双鹤药业股份有限公司提供,批号:2013030406,兔抗大鼠c-fos抗体(美国Oncogene science公司),生物素标记羊抗兔IgG (美国Vector Laboratorie公司),ABC试剂(美国Vector Laboratorie公司),DAB显色液(Sigma公司)。
1.2 动物健康雄性Sprague-Dawley大鼠30只,日龄90-100 d,体重180-200 g,SPF级,由武汉大学基础医学院动物实验中心提供。随机分为空白对照刺激组(A组),生理盐水注射液组(B组,腹腔注射给药容积为0.5 ml/20 g[1],其后与之相同),低剂量腹腔注射(由生理盐水注射液稀释到1 mg/kg)布洛芬组(C1组),中剂量腹腔注射(由生理盐水注射液稀释到10 mg/kg)布洛芬组(C2组),高剂量腹腔注射(由生理盐水注射液稀释到100 mg/kg)布洛芬组(C3组);每组6只。
1.3 方法大鼠腹腔先注射不同浓度布洛芬或生理盐水(对照组不给药),20 min后用5%(体积分数)甲醛0.2 ml注射于右侧后掌足底作成甲醛刺激模型,待时间分别达60 min, 120 min和180 min时,作50%机械触诱发痛阈值(50%paw withdrawalthreshold, 50%PWT,单位:g)测定,180 min后打开椎板,取脊髓L3-5节,免疫组化采用卵白素-生物素-过氧化物酶复合物法,ABC法(avidin-biotin-peroxidase complex technique)染色。
1.4 观察指标大鼠的50%缩足阈值判定,刻度分别为1, 2, 4, 6, 8, 10, 15, 26 g, 从刻度2 g开始,采用up-down法[2]测定;用von Frey (Stoelting,Chicago,IL,USA)纤维丝垂直刺激大鼠后足底中部,出现大鼠行走则重新测试,抬足或舔足行为视为阳性反应。每次刺激间隔30 s,对动物后脚掌中心位置进行刺激,如出现阴性反应,则予相邻高强度的刺激;如出现阳性反应,则予相邻低强度的刺激,直至出现第1次阳性和阴性反应的骑跨,以第一个转折点的前一点为起点连续6次的刺激结果(撤足反射为持续阳性为5次结果,撤足反射为连续阴性则为4次,刺激最多次数为9次)。根据公式50%缩足阈值PWT (g)=[10(Xf+Kδ)]/10000, 式中Xf=最末次测试纤维丝的对数值;K值可根据撤足反应模式查表得出;δ为纤维丝间对数差值的均值。
免疫组织化学ABC法检测(c-fos相关抗原具体步骤参照试剂盒说明书):将切片置于兔抗大鼠的c-fos (1:1 000, Oncogene science公司)抗体液中后,分别在生物素标记的羊抗兔IgG液(1:200, Vector)和ABC液(1:100, Vector)中室温下孵育,漂洗,显色封片。Fos蛋白以细胞核或胞质出现棕黄色颗粒为阳性反应。阴性对照组除细胞核染成蓝色外,应无棕黄色反应物。采用HPIAS-1000高清晰度彩色病理图文报告管理系统(同济千屏影像公司)对Fos蛋白的表达进行定量分析,每张脊髓切片随机选取15个完整而不重叠的高倍镜视野(×400),测定每个视野下阳性神经元数目。
1.5 统计学方法采用SPSS 13.0软件进行统计学分析,所有数据用x±s表示。组内, 组间比较采用方差分析,以P<0.05为差异有统计学意义。
2 结果实验动物大鼠30只,均进入结果分析,无脱失。
各组大鼠机械触诱发痛阈值测定:大鼠甲醛刺激后60 min,120 min,180 min 50% PWT较甲醛刺激前有明显降低,A, B组的50%PWT值较应用甲醛前有明显降低(P<0.05),腹腔注射布洛芬后,无论低中高剂量组,50%PWT值都较A, B组明显升高(P<0.05)。见表 1。
| 表 1 大鼠50%PWT试验结果(g,x±s)及脊髓背角浅层Fos样免疫阳性神经元数目(个) |
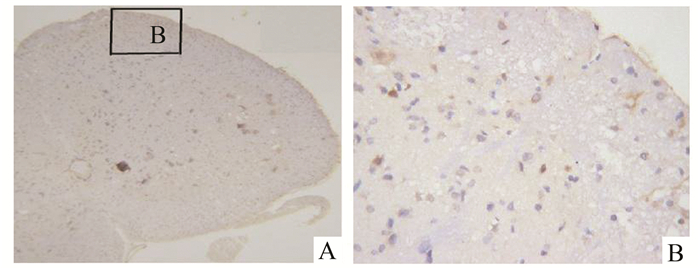
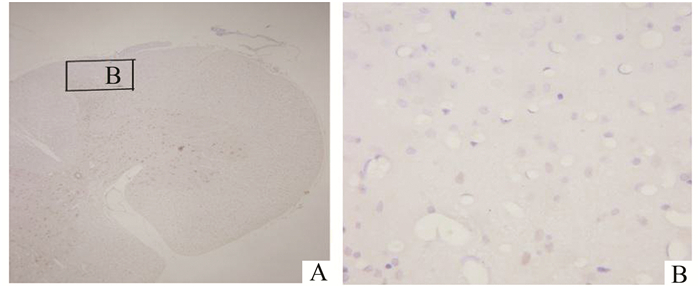
各组大鼠脊髓节段Fos蛋白免疫组化结果:对照组行甲醛刺激180 min (A组),生理盐水注射液并行甲醛刺激180 min组(B组)见大量Fos样免疫阳性神经元分布在背角浅层(Ⅰ、Ⅱ层),明显多于应用布洛芬各组(C1, C2和C3组)(P<0.05)。高剂量布洛芬组Fos样免疫阳性神经元数少于低和中剂量组(P<0.05)。见表 1和图 1-6。实验所用的各组剂量布洛芬都能使Fos蛋白部分抑制,但尚不能全部抑制。
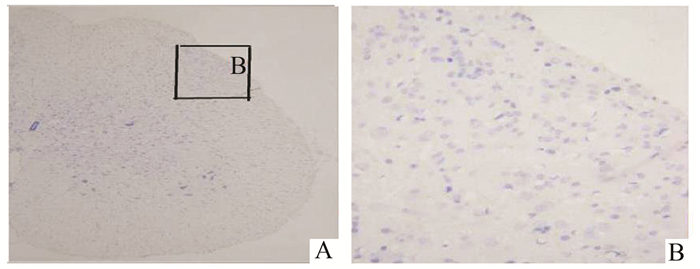
|
图 1 空白对照未予以甲醛刺激的脊髓病理照片 A:脊髓横切面; B:脊髓背角浅层 |
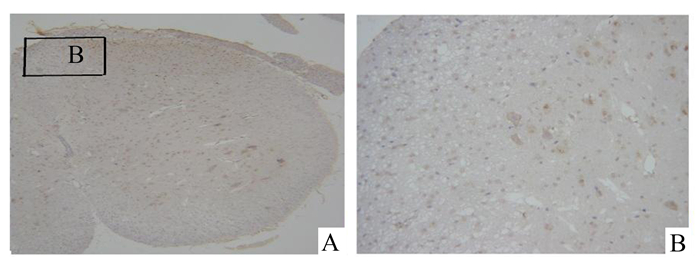
|
图 2 A组行甲醛刺激180 min后的脊髓病理照片 A:脊髓横切面; B:脊髓背角浅层 |
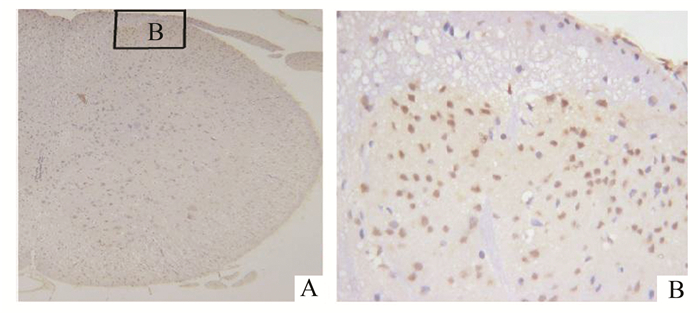
|
图 3 B组甲醛刺激180 min后的脊髓病理照片 A:脊髓横切面; B:脊髓背角浅层 |
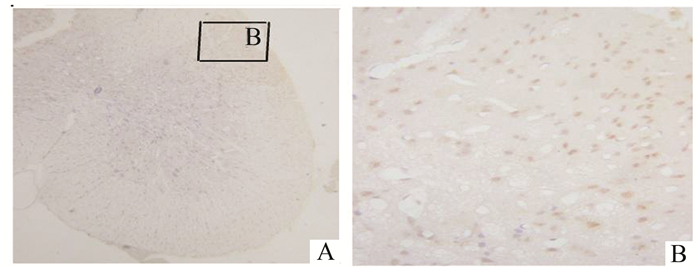
|
图 4 C1组甲醛化学刺激180 min的脊髓病理照片 A:脊髓横切面; B:脊髓背角浅层 |
|
图 5 C2组行甲醛化学刺激180 min的脊髓病理照片 A:脊髓横切面; B:脊髓背角浅层 |
|
图 6 C3组行甲醛化学刺激180 min的脊髓病理照片 A:脊髓横切面; B:脊髓背角浅层 |
布洛芬为非甾体类消炎镇痛药。它的传统作用机制认为是通过抑制体内前列腺素E合成来止痛。前列腺素会使“痛感”信号放大,使病人感到疼痛异常。非甾体类消炎镇痛药抑制了前列腺素,就等于减弱或者消除了疼痛。脊髓背角浅层是痛觉传入的中枢部位,布洛芬的作用部位目前认为是在外周和中枢,其止痛作用可能主要是由于S (+)异构体抑制了背角和脊髓丘脑中心的COX-2,并抑制了一氧化氮合酶,通过对血清素激活通路和肾上腺素通路的刺激作用,在背角水平抑制疼痛反应[3], 甲醛刺激模型与临床伤害性刺激的疼痛特征有相似之处, 被广泛用于疼痛研究[4]。Fos蛋白的表达作为接受一定刺激的神经元激活标志,与伤害性刺激应答有密切关系, 已被广泛应用于追踪各种刺激尤其是疼痛刺激的传导通路,确认参与反应的多级神经元的定位研究[5],常作为反映疼痛强度的金指标[6]。由于Fos蛋白对外界刺激非常敏感,正常情况下,细胞内没有或仅有少量Fos蛋白表达。当受到伤害性刺激时数分钟后, 脊髓背角突触后神经元内c-fos基因的mRNA增多,1-2 h细胞内c-fos基因翻译出的蛋白产物Fos增多,脊髓背角突触后神经元内c-fos免疫阳性神经元数量增多。c-fos基因的表达和蛋白质合成是目前较为理想的神经系统功能活动的定位标记。本实验中,应用甲醛刺激大鼠坐骨神经后引发脊髓神经元Fos蛋白表达,见大量Fos样免疫阳性神经元分布在背角浅层(Ⅰ、Ⅱ层), 明显多于C组,即应用布洛芬后,C1, C2和C3组明显减少,C3组明显少于C1和C2组,是因为发生神经元功能的变化要求基因表达上重新编程,c-fos基因及Fos蛋白是痛觉功能的客观指标之一[7],一定程度上,Fos阳性神经元的数量与所受刺激的强度成正比,可作为神经元接受伤害性刺激激活的标志[8],伤害性刺激诱导大鼠Fos蛋白样免疫阳性反应可被布洛芬抑制,使脊髓背角Fos蛋白表达减少,降低了大鼠脊髓背角浅层Fos蛋白含量,提示布洛芬降低脊髓背角相关神经元兴奋性,从而达到减轻伤害性刺激目的,且布洛芬100 mg/kg作用效果明显,但浅表层仍有少量淡染Fos样免疫阳性神经元, 说明脊髓应用外源性非甾体类镇痛药,在观察的剂量范围内,只能部分阻断感觉神经的伤害性信息传入,达到部分抑制伤害性刺激的效果。
综上所述,布洛芬能抑制大鼠对伤害性刺激引起的脊髓Fos样免疫阳性神经元增多效应,大鼠脊髓背角浅层可能参与了布洛芬抑制伤害性刺激的调制。
| [1] |
岳鹏, 蔡鸣, 刘晶, 等. 布洛芬注射液小鼠单次腹腔注射给药毒性的试验研究[J].
中国现代医生, 2011, 49 (23): 18-19.
Yue P, Cai M, Liu J, et al. studies on the acute toxicity of caldolor on ICR mice by single intraperitoneal injection[J]. China Modern Doctor, 2011, 49(23): 18-19. |
| [2] | Bonin RP, Bories C, De Koninck Y. A simplified up-down method (SUDO) for measuring mechanical nociception in rodents using von Frey filaments[J]. Mol Pain, 2014, 10: 26. DOI: 10.1186/1744-8069-10-26. |
| [3] | Terebetski JL, Michniak-Kohn B. Combining ibuprofen sodium with cellulosic polymers: A deep dive into mechanisms of prolonged supersaturation[J]. Int J Pharm, 2014, 475(1-2): 536-546. DOI: 10.1016/j.ijpharm.2014.09.015. |
| [4] | Wang LX, Wang ZJ. Animal and cellular models of chronic pain[J]. Adv Drug Deliv Rev, 2003, 55(8): 949-965. DOI: 10.1016/S0169-409X(03)00098-X. |
| [5] | Daou I, Tuttle AH, Longo G, et al. Remote optogenetic activation and sensitization of pain pathways in freely moving mice[J]. J Neurosci, 2013, 33(47): 18631-18640. DOI: 10.1523/JNEUROSCI.2424-13.2013. |
| [6] | Duplan H, Li RY, Vue C, et al. Graftsof immortalized chromaffin cells bio-engineered to improve met-enkephalin release also reduce formalin-evoked c-fos expression in rat spinal cord[J]. Neurosci Lett, 2004, 370(1): 1-6. DOI: 10.1016/j.neulet.2004.07.017. |
| [7] | Ralya A, McCarson KE. Acute estrogen surge enhances inflammatory nociception without altering spinal Fos expression[J]. Neurosci Lett, 2014, 575: 91-95. DOI: 10.1016/j.neulet.2014.05.035. |
| [8] | Hossaini M, Duraku LS, Kohli SK, et al. Spinal distribution of c-Fos activated neurons expressing enkephalin in acute and chronic pain models[J]. Brain Res, 2014, 1543: 83-82. DOI: 10.1016/j.brainres.2013.10.044. |
 2016, Vol. 37
2016, Vol. 37

