慢性气道炎症性疾病是指主要发生在气道、肺实质及肺血管的慢性炎症疾病的总称,主要包括慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)和支气管哮喘等。气道黏液高分泌是慢性气道炎症性疾病的重要病理特征之一[1]。黏蛋白(Mucin,MUC)广泛分布于机体各组织黏膜上皮表面,黏蛋白MUC5AC和MUC5B是人类气道黏液的主要成分[2]。目前研究表明,MUC蛋白家族的表达与各类炎症因子密切相关,如肿瘤坏死因子α(tumor necrosis factor alpha,TNF-α)可促进呼吸道上皮黏蛋白的表达和分泌[3],白细胞介素-8(interleukin-8,IL-8)对呼吸道上皮 MUC5AC 表达量增多中起着重要作用[4]。同时在人结肠癌细胞中IL-4,IL-13或TNF-α可以通过丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)通路促进MUC2的表达[5]; 在人呼吸道上皮细胞中,胰岛素样生长因子(insulin-like growth factors-1,IGF-1)可以通过MAPK通路中的ERK1和p38的磷酸化途径促进MUC8和MUC5B的表达等[6]。
白细胞介素-33(IL-33,白介素-33)是近年来发现的一种新的白介素家族成员,有报道表明它在气道炎症当中发挥着重要的作用[7],然而对于IL-33在A549细胞中对黏蛋白基因表达的影响及机制并未有过报道,因此,本文着重探究IL-33对A549细胞黏蛋白表达的影响及其作用机制。
1 材料与方法 1.1 主要材料与试剂人肺癌A549细胞株(武汉大学典型培养物保藏中心)、胎牛血清(浙江天杭生物科技有限公司)、RPMI 1640培养基(Thermo scientific)、磷酸盐缓冲液(PBS)、0.25%胰酶、青霉素-链霉素、组织/细胞RNA快速提取试剂盒(北京艾德莱生物科技有限公司)、逆转录试剂盒(日本TOYOBO公司)、实时荧光定量PCR缓冲液iQTMSYBR Green Supermix(美国Bio-Rad公司)、IL-33(上海近岸科技有限公司)、PDTC(碧云天生物技术研究所);一抗:小鼠Anti-β-actin(武汉爱博泰克生物科技有限公司)、小鼠IκBα磷酸化抗体(美国Cell Signaling Technology);二抗:Anti-mouse IgG-HRP(美国Jackson Immuno Researsh公司)。
1.2 细胞培养及处理RPMI 1640培养基使用前加入10%的胎牛血清和1%的青霉素-链霉素。于RPMI 1640培养基中培养A549 细胞,细胞密度达 70%-80%时传代。各组细胞接种于6孔培养皿中用于 RT-PCR 检测,每孔接种4×105个细胞,培养箱培养24 h后加入药物刺激,实验分组:①对照组:加入PBS处理;②IL-33刺激组:加入IL-33使其终浓度达到100 ng/ml。处理时间分别设置为12 h,24 h和36 h,收细胞,提取总的mRNA。
1.3 RT-PCR检测收集处理好的细胞,提取总的RNA,方法参照北京艾德莱生物科技有限公司试剂盒说明书。随后逆转录成cDNA,逆转录方法参照日本TOYOBO公司试剂盒说明书,进行PCR反应。实时荧光定量PCR采用美国Bio-Rad公司iQTM SYBR®Green Supermix试剂盒。本文中所使用的实时荧光定量PCR引物均是以人的基因为模板设计的,由武汉擎科生物技术有限公司合成。各引物的详细信息见表 1。
| 表 1 实时荧光定量PCR引物列表 |
数据均以xx±s表示,应用 SPSS Statistics 19.0软件包对结果进行统计学分析,采用t检验,两样本均数间比较采用t检验,多样本均数间比较采用单因素方差分析,P<0.05为差异有统计学意义。
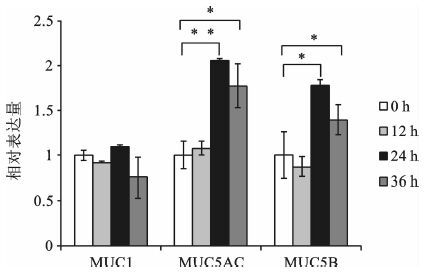
2 结果 2.1 RT-PCR法检测IL-33处理后MUC1,MUC5AC和MUC5B的mRNA表达水平如图 1所示,100 ng/ml的IL-33处理A549细胞12 h后,黏蛋白MUC1,MUC5AC和MUC5B的表达量与对照组相比,无显著性差异。在处理24 h以及36 h后,MUC5AC和MUC5B的表达量与对照组相比显著上升(P<0.05) ,MUC1的表达量没有显著的变化。
|
图 1 100 ng/ml的IL-33刺激A549细胞不同时长MUC1,MUC5AC和MUC5B mRNA的表达量 *P<0.05,**P<0.01 |
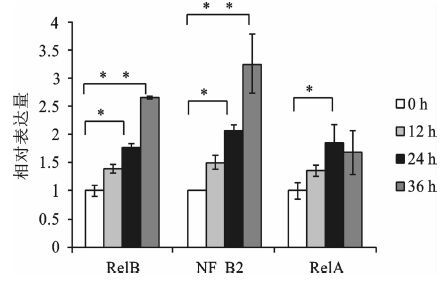
如图 2所示,100 ng/ml的IL-33处理A549细胞12 h后,NF-κB下游基因RELB,NF-κB2和RELA的表达量与对照组相比,无明显的差异。处理A549细胞24 h后,RELB,NF-κB2和RELA的表达量与对照组相比有所升高(P<0.05) 。处理36 h后,RELB和NF-κB2的mRNA水平与对照组相比显著升高(P<0.01) 。
|
图 2 100 ng/ml的IL-33刺激A549细胞不同时长NF-κB下游基因RELB,NF-κB2和RELA的表达量 *P<0.05,**P<0.01 |
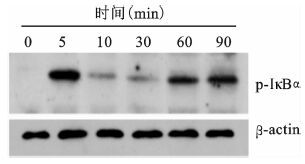
如图 3所示,100 ng/ml的IL-33刺激A549细胞5 min后IκBα蛋白磷酸化水平与对照组相比显著升高。
|
图 3 100 ng/ml的IL-33刺激A549细胞不同时长IκBα蛋白磷酸化水平的变化 |
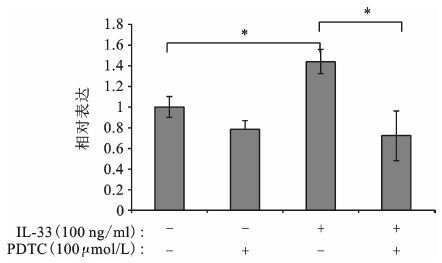
为进一步验证A549细胞中NF-κB信号通路与MUC5AC表达的关系,我们将实验分为4组:①对照组:加入PBS处理; ②IL-33刺激组:加入IL-33使其终浓度达到100 ng/ml;③PDTC处理组:加入PDTC使其终浓度达到100 μmol/L;④IL-33和PDTC共同刺激组:在加入终浓度为100 ng/ml的IL-33同时加入终浓度为100 μmol/L的PDTC。在IL-33和PDTC共同刺激组中MUC5AC相对于IL-33刺激组明显下降(P<0.05) ,MUC5B没有明显的变化(如图 4、图 5所示)。
|
图 4 100 ng/ml的IL-33和100 μmol/L的PDTC处理A549细胞24 h后MUC5AC的表达量 *P<0.05 |
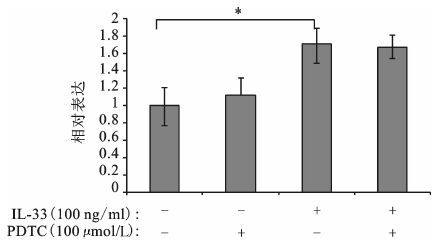
|
图 5 100 ng/ml的IL-33和100 μmol/L的PDTC处理A549细胞24 h后MUC5B的表达量 *P<0.05 |
白介素-33(IL-33) 是2005年作为homolog of sulfotransferase(ST2) 的配体被发现的一个新的白介素家族成员。ST2在结构上和其他的IL-1类受体相似,具有Toll样受体结构域,因此IL-33被归为IL-1家族。IL-33表达广泛,在受损的内皮细胞和上皮细胞、活化的Th2细胞和肥大细胞均有表达并参与介导细胞炎症反应[8]。有研究显示,IL-33 mRNA水平在哮喘患者血清和组织中表达量升高,在小鼠气道炎症哮喘模型中,患病鼠的血清和组织中IL-33的mRNA表达明显增加[9]。上述研究表明IL-33及其受体与上述慢性气道炎症性疾病尤其是哮喘的发病机制有密切关系,然而对于IL-33如何影响慢性气道炎症性疾病及其分子机制并不完善。
本研究结果显示,给予A549细胞IL-33处理后,MUC5AC和MUC5B的mRNA水平显著升高,而MUC1基因表达不受影响,可见IL-33并不是对A549细胞中所有的黏蛋白基因都有影响,但对MUC5AC和MUC5B基因的表达有促进作用。黏蛋白MUC5AC和MUC5B是人类气道黏液的主要成分之一[10],在慢性气道炎症性疾病如支气管哮喘、COPD、弥漫性泛细支气管炎和支气管扩张中MUC5AC和MUC5B通常呈现高表达状态[11]。结果提示IL-33可能通过上调黏蛋白MUC5AC和MUC5B的表达进而参与慢性气道炎症性疾病的发生。那么IL-33又是通过什么机制来促进黏蛋白基因MUC5AC和MUC5B的表达呢?
我们研究发现,给予A549细胞IL-33处理后,除了MUC5AC和MUC5B的mRNA水平显著升高之外,炎症信号通路NF-κB下游基因如RELB,RELA和NFκB2的mRNA水平也显著上升,同时IL-33刺激A549细胞5 min后IκBα蛋白磷酸化水平与对照组相比显著升高,说明IL-33在上调A549细胞中MUC5AC和MUC5B表达的同时还可以激活NF-κB信号通路。随后在细胞经过IL-33处理的同时加入NF-κB特异性抑制剂PDTC,结果显示给予PDTC处理后,IL-33对MUC5AC mRNA的促进作用被抑制,而对MUC5B没有明显影响,说明IL-33是通过激活NF-κB信号通路进而上调MUC5AC的表达,而IL-33可能是通过激活其他信号通路上调MUC5B的表达,这需要进一步的实验来证明。
作为白介素家族新发现的成员,IL-33参与慢性气道炎症性疾病的分子机制并不明确,本实验结果表明IL-33可以上调A549细胞中MUC5AC和MUC5B的表达,提示IL-33可能通过上调黏蛋白MUC5AC和MUC5B的表达进而参与慢性气道炎症性疾病的发生。并且我们的研究还表明IL-33是通过NF-κB通路激活MUC5AC的表达。然而黏蛋白MUC5AC和MUC5B的过表达又是如何影响慢性气道炎症性疾病有待进一步研究。
| [1] | Van Bruaene N, Bachert C. Tissue remodeling in chronic rhinosinusitis[J]. Current Opinion in Allergy and Clinical Immunology, 2011, 11(1): 8-11. DOI: 10.1097/ACI.0b013e32834233ef. |
| [2] | Oue N, Sentani K, Sakamoto N, et al. Clinicopathologic and molecular characteristics of gastric cancer showing gastric and intestinal mucin phenotype[J]. Cancer Science, 2015, 106(8): 951-958. DOI: 10.1111/cas.2015.106.issue-8. |
| [3] | Kufe DW. Mucins in cancer: function, prognosis and therapy[J]. Nature Reviews Cancer, 2009, 9(12): 874-885. DOI: 10.1038/nrc2761. |
| [4] | Ovrevik J, Refsnes M, Lag M, et al. Activation of Proinflammatory Responses in Cells of the Airway Mucosa by Particulate Matter: Oxidant and Non-Oxidant-Mediated Triggering Mechanisms[J]. Biomolecules, 2015, 5(3): 1399-1440. DOI: 10.3390/biom5031399. |
| [5] | Hugen N, Simons M, Halilovic A, et al. The molecular background of mucinous carcinoma beyond MUC2[J]. J Pathol Clin Res, 2015, 1(1): 3-17. DOI: 10.1002/cjp2.1. |
| [6] | Bae CH, Kim JS, Song SY, et al. Insulin-like growth factor-1 induces MUC8 and MUC5B expression via ERK1 and p38 MAPK in human airway epithelial cells[J]. Biochem Biophys Res Commun, 2013, 430(2): 683-688. DOI: 10.1016/j.bbrc.2012.11.091. |
| [7] | Shang J, Zhao J, Wu X, et al. Interleukin-33 promotes inflammatory cytokine production in chronic airway inflammation[J]. Biochem Cell Biol, 2015, 93(4): 359-366. DOI: 10.1139/bcb-2014-0163. |
| [8] | Lu J, Kang J, Zhang C, et al. The role of IL-33/ST2L signals in the immune cells[J]. Immunology Letters, 2015, 164(1): 11-17. DOI: 10.1016/j.imlet.2015.01.008. |
| [9] | Oboki K, Nakae S, Matsumoto K, et al. IL-33 and Airway Inflammation[J]. Allergy, Asthma & Immunology Research, 2011, 3(2): 81-88. |
| [10] | Sheng YH, Hasnain SZ, Florin TH, et al. Mucins in inflammatory bowel diseases and colorectal cancer[J]. J Gastroenterol Hepatol, 2012, 27(1): 28-38. DOI: 10.1111/jgh.2012.27.issue-1. |
| [11] | Ma R, Wang Y, Cheng G, et al. MUC5AC expression up-regulation goblet cell hyperplasia in the airway of patients with chronic obstructive pulmonary disease[J]. Chinese Medical Sciences Journal, 2005, 20(3): 181-184. |
 2017, Vol. 38
2017, Vol. 38

