2. 武汉大学中南医院干部保健处 湖北 武汉 430071
2. Dept.of Cadres Health Service, Zhongnan Hospital of Wuhan University, Wuhan 430071, China
获得性免疫缺陷综合征(acquired immunodeficiency syndrome,AIDS)是在感染人类免疫缺陷病毒(human immune deficiency virus,HIV)后导致的严重免疫抑制综合征。90%青少年HIV感染是以围产期母婴传播(mother to child tansmission, MTCT)所致[1],感染HIV孕妇在妊娠期经胎盘或分娩时经产道传播(血液或阴道分泌物)或产后经母乳传播均可使婴儿感染HIV。HIV-1易于亲嗜神经组织,儿童感染可直接导致中枢神经系统损害。
扩散加权成像(diffusion weighted imaging,DWI)是检测水分子布朗运动唯一无侵袭性方法,鉴于扩散敏感梯度强度(b值,单位s/mm2),与主磁场强度和施加扩散敏感梯度场幅度、持续时间、间隔时间有关;当b>1 000 s/mm2时组织中水分子信号强度明显表现出不再遵循单指数模型衰减。体素内不相干运动扩散加权成像(intravoxel incoherent motion diffusion weighted imaging,IVIM-DWI)首次由Le Bihan等[2]提出。IVIM-DWI采用双指数模型能评价水分子扩散和微循环灌注信息,应用低b值将水分子扩散与微循环灌注影响分离;DWI-IVIM双指数模型拟合后能得到3个参数,包括真实扩散系数D值、灌注扩散系数D*值及灌注分数f值;D值反映了组织内真实的水分子扩散,D*值反映了组织内微循环灌注不相干运动,f值表示微循环灌注分数,反映组织内毛细血管密集程度。本文探讨IVIM-DWI研究围产期HIV感染无症状型青少年脑扩散与灌注信息可行性及其变化特征。
1 材料与方法 1.1 一般资料搜集2013年6月至2014年12月武汉大学中南医院艾滋病培训中心确诊母婴传播HIV+儿童18例(男9例,女9例,年龄13-17岁,平均年龄15岁)和年龄、性别、受教育程度及中文蒙特利尔认知评估(MoCA评分)相匹配的对照组HIV-青少年17例;其父母双方一方或双方确诊为HIV+(表 1)。所有受试者排除HIV相关颅内机会性感染,无神经系统症状,MRI平扫未见异常;HIV+组经ELISA和蛋白印迹测试(Western Blot)确诊HIV+,感染途径为母婴垂直传播,年龄小于18岁;均早期确诊和早期接受高效抗逆转录病毒(highly active antiretroviral therapy,HAART)治疗;依据DSM-Ⅳ排除当前药物滥用和酒精依赖无药物滥用、无酒精依赖、无注意力缺陷障碍、无抑郁症(基于自我描述)和无癫痫、高血压及糖尿病;排除神经认知障碍,儿童受教育年限<12年,MoCA评分≥25分;受教育年限≥12年,MoCA评分≥26分;排除幽闭恐惧症、体内金属植入物等有MRI检查禁忌证。本研究经武汉大学中南医院医学伦理委员会批准,所有受试者均签署知情同意书。
| 表 1 两组受试者临床资料 |
采用Siemens Magnetom Trio 3.0T超导MR成像仪,8通道头颅矩阵线圈。IVIM-DWI采用单次激发平面回波(SS-EPI)序列,并行采集空间敏感编码技术(ASSET),前后连合间线(AP-PC)定位,横断面扫描,选取7个b值(0、50、150、200、400、600、800 s/mm2),TR 3 400 ms,TE 85 ms,FOV 220 mm,层厚4 mm,间距1 mm,NEX 3,矩阵192×192,序列扫描时间为3 min 26 s。同时采集常规T1WI、T2WI及T2-FLAIR序列图像,用于常规影像学诊断。
1.3 图像后处理首先将采集的IVIM-DWI原始图像导入MIKT-Diffusion软件(www.mitk.org,2012版),分别保存及导出D、D*及f图像;再将D、D*及f图像导入MRIcroN软件,然后进行手动勾画两侧尾状核和额叶白质感兴趣区(region of interest,ROI),尽量保持ROI大小、位置基本一致,避开脑脊液,分别测量左侧和右侧ROI的相对IVIM参数值,取其左侧和右侧ROI平均值,再经倍数校正得到ROI的D值、D*值及f值。
1.4 统计学分析采用SPSS 19.0统计软件包,P<0.05为差异具有统计学意义。应用独立样本t检验比较两组受试者D值、D*值及f值。应用卡方检验比较两组受试者临床基本信息。应用Pearson相关性分析评估HIV+组D值、D*值及f值分别与CD4+T淋巴细胞计数、CD4/CD8比值的相关性。
2 结果 2.1 受试者一般资料比较HIV+组和HIV-组年龄(P=0.67)、性别(P=1.00)、受教育程度(P=0.18)和MoCA评分(P=0.78)差异均无统计学意义。HIV阳性者CD4+T淋巴细胞计数平均值为(479.89±308.12)个/μl、CD4/CD8比值平均值为0.71±0.44(表 1)。HIV+组仅1例表现生长发育迟缓,其余17例临床表现未见异常;HIV-组临床表现未见异常。
2.2 IVIM参数值比较与HIV-组比较,HIV+组尾状核和额叶白质D*值显著降低,尾状核为(4.49±1.04)10-3mm2/s比(5.32±0.47)10-3mm2/s,P=0.005;额叶白质为(4.68±0.39)10-3mm2/s比(5.27±0.68)10-3mm2/s,P=0.003;而两组尾状核和额叶白质D值差异无统计学意义,尾状核(0.77±0.05)10-3mm2/s比(0.75±0.03)10-3mm2/s,P=0.121;额叶白质为(0.82±0.04)10-3mm2/s比(0.81±0.04)10-3mm2/s,P=0.623;两组尾状核和额叶白质f值差异亦无统计学意义,尾状核(5.30±0.81)%比(5.67±0.54)%,P=0.115;额叶白质(5.41±1.46)%比(5.55±0.42)%,P=0.722](表 2,表 3,图 1-3)。
| 表 2 两组受试者尾状核D值、D*值、f值比较结果 |
| 表 3 两组受试者额叶白质D值、D*值、f值比较结果 |
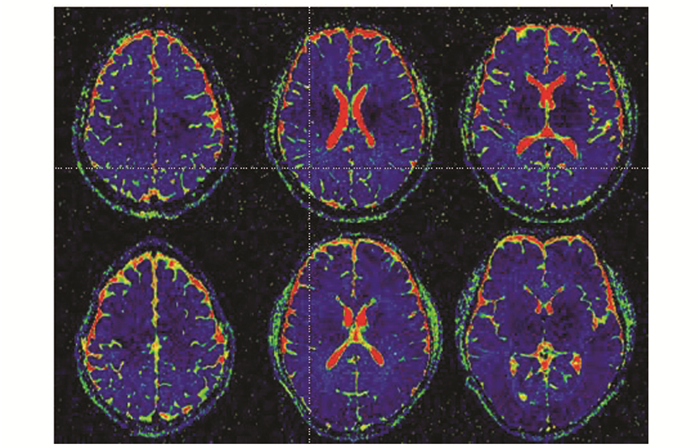
|
图 1 D值伪彩图 上排HIV+组,下排HIV-组 |
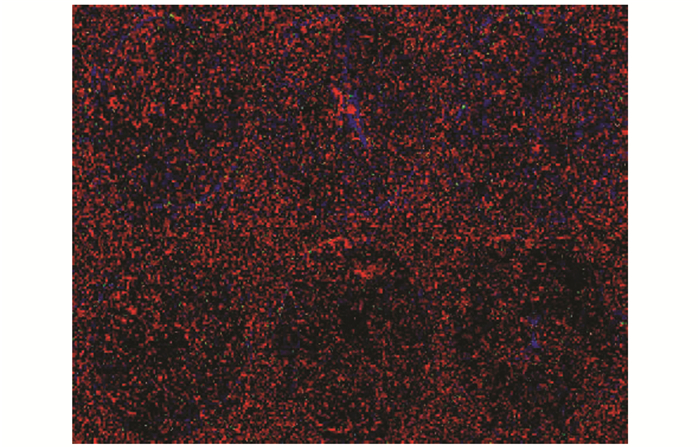
|
图 2 D*值伪彩图 上排HIV+组,下排HIV-组;P<0.05 |
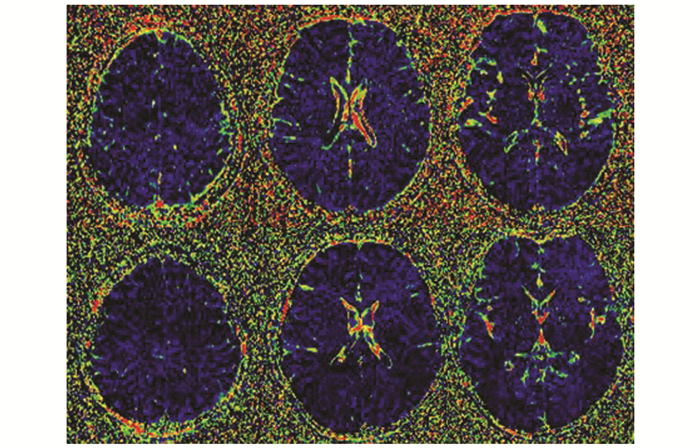
|
图 3 f值伪彩图 上排HIV+组,下排HIV-组;P>0.05 |
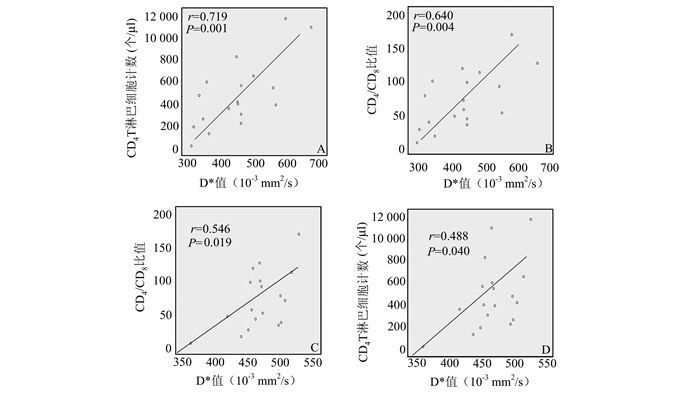
HIV+组尾状核D*值与CD4+T淋巴细胞计数呈显著正相关(r=0.719,P=0.001,图 4A),HIV+组尾状核D*值与CD4/CD8比值呈显著正相关性(r=0.640,P=0.004,图 4B);HIV组额叶白质D*值与CD4+T淋巴细胞计数呈显著正相关(r=0.488,P=0.040,图 4C),HIV+组额叶白质D*值与CD4/CD8比值呈显著正相关性(r=0.546,P=0.019,图 4D)。HIV+组尾状核和额叶白质D值和f值与CD4+T淋巴细胞计数及CD4/CD8比值无显著相关性。
|
图 4 HIV+组尾状核(A、B)、额叶(C、D)的D*值与CD4+T淋巴细胞及与CD4/CD8比值相关性的散点图 |
本研究筛选18例HIV+青少年均是母婴传播感染,同时也是“艾滋病孤儿”[3],他们父母一方或双方已去世,其中仅1例表现为生长发育迟缓;18例均无神经系统症状。17例HIV-组来自相似家庭,其经济状况、社会压力及受教育程度相似,对照性强。18例HIV+组早期明确诊断及早期接受HAART治疗,有效降低了艾滋病发病率和死亡率、延缓疾病进展,是难得的研究对象;但本文并未能排除HAART治疗对脑微观结构影响。
Le Bihan等[2] 1986年首次提出基于IVIM-DWI成像方法。在生物组织内水分子运动主要包含水分子扩散运动和毛细血管血流运动(即微循环灌注),微循环灌注被认为是不相关运动,是由于体素内毛细血管内血流运动类似于随机扩散运动。拉伸指数模型引入了异质性性参数α,反映体素内信号衰减方式,范围在0-1之间。当α等于1时,拉伸指数模型等同于单指数模型,表明体素内信号衰减方式单一,扩散异质性极低;当α接近0时,表明体素内信号衰减方式复杂,扩散异质性极高。IVIM通过采用双指数模型得到3个相关参数值:真实扩散系数D值、灌注扩散系数D*值及灌注分数f值。D值反映了组织内真实的水分子扩散,D*值反映了组织内微循环灌注不相干运动,f值表示微循环灌微循环灌注分数。多b值IVIM-DWI信号强度与b值之间关系为:Sb/S0=(1-f)·exp (-b·D)+f·exp (-b·D*);当b>200 s/mm2时,微循环灌注信号可忽略不计,上述公式简化为:Sb/S0=(1-f)·exp (-b·D)。本研究利用7个b值信号强度拟合出ADC值,较传统仅由两个b值获得的ADC值更精确。Kwee[4]等对高级别胶质瘤研究发现肿瘤区ADC值与分布扩散系数(Distributed diffusion coefficient,DDC)值呈显著性正相关,DDC值和ADC值存在紧密联系。Buckle[5]等对AIDS伴进行性多灶性脑白质病变患者行HAART治疗后发现免疫重建炎症综合征患者较未出现免疫重建炎症综合征患者在治疗前病变区与对侧镜像白质区最大ADC值明显偏高。彭雯佳[6]等在对单侧大脑前循环动脉狭窄者IVIM-DWI研究发现DDC值和ADC值在无动脉狭窄和狭窄者之间差异显著。本研究未显示HIV+组较健康者D值、ADC值在左右两侧基底节区有显著性差异,这可能是因为本组病例并未合并脑内机会性感染、无颅内肿瘤及中枢神经系统疾病,其脑部基底节区域尚未出现较为明显结构及功能性病变[7]。
本研究发现与HIV-组比较,HIV+组尾状核和额叶白质D*值减低,且与CD4+T淋巴细胞计数和CD4/CD8比值呈显著正相关;提示IVIM-DWI较常规脑MRI和DWI检查更敏感地检测和提示围产期HIV感染无症状青少年脑部D*值变化,即脑部微循环灌注不相干运动的变化。D*值降低提示尾状核和额叶白质微循环灌注减低;随着艾滋病进程加重(CD4+T淋巴细胞计数下降、CD4/CD8比值下降),尾状核和额叶白质微循环灌注逐渐减低,D*值能潜在反映HIV感染脑部病变进程。有研究显示HIV感染早期其前额叶血流灌注减低,其形态学结构表现正常[7]。HAART治疗后HIV感染者常规CT检查显示正常,但SPECT检测治疗发现额叶血流灌注不足有所缓解[8]。Chang等[9]研究发现脑灌注异常程度与艾滋病严重程度(CD4+T淋巴细胞计数、血浆病毒载量及Karnofsky评分)有关。Li等[10]纵向研究SIV感染猕猴模型发现尾状核脑血流下降与CD4+T淋巴细胞计数和CD4/CD8比值显著相关。Zhang等[11]研究表明SIV感染猕猴尾状核CBF显著减低与感染期CD4+T淋巴细胞计数和CD4/CD8比值相关,提示特定区域CBF异常与SIV感染免疫功能障碍有关。
HIV+者脑血流量减低机制可能与HIV直接影响血小板功能有关[12],HIV激活血小板,血小板黏附聚集血管壁,刺激血清素释放导致血管收缩,脑血流量减低[13]。HIV还可促使细胞因子和趋化因子释放,但并未促进内皮细胞迁移、增殖和新血管形成[14];细胞趋化因子增加造成神经元损害,引起脑血流量减低。还可能与动脉粥样硬化发生有关,CT提示部分HIV+青少年基底节区小血管壁钙化,病理学也证实HIV+者小血管壁钙化发生机率高[16]。提示无症状HIV+青年受试者尾状核和额叶白质D*变化可能与上述因素有关。
本研究HIV+组尾状核及额叶白质D值有稍升高趋势,但D值和f值组间差异均无统计学意义;且D值、f值与CD4+T淋巴细胞计数、CD4/CD8比值无显著相关性,提示D值和f值不能反映HIV+无症状青少年脑部隐匿性病变。有关HIV-DWI研究报道结果并不一致。有研究SIV感染猫脑白质、灰质和基底节区ADC值显著升高[16];伴轻微运动障碍HIV+者全脑ADC值、基底节区ADC值未见异常[17]。轻微痴呆HIV+者额叶白质水分子扩散不受限,ADC值明显升高。HIV+者额叶白质ADC值升高,但无统计学意义[18]。
总之,IVIM-DWI能敏感检测围产期HIV感染无症状型青少年尾状核和额叶白质微循环灌注不相干运动D*值的变化,D*值可能作为HIV感染脑部变化早期和进展评估的可视化标志物。但本研究病例有限;人工测量两侧尾状核及额叶白质IVIM参数平均值,存在测量偏倚;未能完全剔除抗逆转录病毒药物对神经成像影响。
| [1] | 周先志, 赵敏. 艾滋病诊疗新技术[M]. 北京: 人民军医出版社, 2005: 139. |
| [2] | Le Bihan D, Breton E, Lallemand D, et al. MR imaging of intravoxel incoherent motions:application to diffusion and perfusion in neurologic disorders[J]. Radiology, 1986, 161(2): 401-407. DOI: 10.1148/radiology.161.2.3763909. |
| [3] | 吕新辉, 毕振强, 钱跃升. 中国艾滋孤儿现状及应对策略[J]. 中国公共卫生, 2006, 22(7): 872-873. |
| [4] | Kwee TC, Galbán CJ, Tsien C, et al. Comparison of apparent diffusion coefficients and distributed diffusion coefficients in high-grade gliomas[J]. J Magn Reson Imaging, 2010, 31(3): 531-537. DOI: 10.1002/jmri.v31:3. |
| [5] | Buckle C, Castillo M. Use of Diffusion-Weighted Imaging to Evaluate the Initial Response of Progressive Multifocal Leukoencephalopathy to Highly Active Antiretroviral Therapy: Early Experience[J]. AJNR Am J Neuroradiol, 2010, 31(6): 1031-1035. DOI: 10.3174/ajnr.A2024. |
| [6] | 彭雯佳, 陆建平, 王鹤, 等. 拉伸指数与单指数模型DWI对单侧大脑前循环动脉狭窄者的评价[J]. 放射学实践, 2012, 27(1): 11-16. |
| [7] | TranDinh YR, Mamo H, Cervoni J, et al. Disturbances in the cerebral perfusion of human immune deficiency virus-1 seropositive asymptomatic subjects: a quantitative tomography study of 18 cases[J]. J Nucl Med, 1990, 31(10): 1601-1607. |
| [8] | Tozzi V, Narciso P, Galgani S, et al. Effects of zidovudine in 30 patients with mild to end-stage AIDS dementia complex[J]. AIDS, 1993, 7(5): 683-692. DOI: 10.1097/00002030-199305000-00012. |
| [9] | Chang L, Ernst T, Leonido-Yee M, et al. Perfusion MRI detects rCBF abnormalities in early stages of HIV-cognitive motor complex[J]. Neurology, 2000, 54(2): 389-396. DOI: 10.1212/WNL.54.2.389. |
| [10] | Li C, Zhang X, Komery A, et al. Longitudinal diffusion tensor imaging and perfusion MRI investigation in a macaque model of neuro-AIDS: a preliminary study[J]. Neuroimage, 2011, 58(1): 286-292. DOI: 10.1016/j.neuroimage.2011.05.068. |
| [11] | Zhang X, Li C. Quantitative MRI measures in SIV-infected macaque brains[J]. J Clin Cell Immunol, 2013, Suppl7: 7-005. |
| [12] | Wachtman LM, Skolasky RL, Tarwater PM, et al. Platelet decline: an avenue for investigation into the pathogenesis of human immunodeficiency virus-associated dementia[J]. Arch Neurol, 2007, 64(9): 1264-1272. DOI: 10.1001/archneur.64.9.1264. |
| [13] | Holme PA, Muller F, Solum NO, et al. Enhanced activation of platelets with abnormal release of RANTES in human immunodeficiency virus type 1 infection[J]. FASEB J, 1998, 12(1): 79-89. |
| [14] | Persidsky Y, Buttini M, Limoges J, et al. An analysis of HIV-1-associated inflammatory products in brain tissue of humans and SCID mice with HIV-1 encephalitis[J]. J Neurovirol, 1997, 3(6): 401-416. DOI: 10.3109/13550289709031186. |
| [15] | Ortiz G, Koch S, Romano JG, et al. Mechanisms of ischemic stroke in HIV-infected patients[J]. Neurology, 2007, 68(16): 1257-1261. DOI: 10.1212/01.wnl.0000259515.45579.1e. |
| [16] | Bucy DS, Brown MS, Bielefeldt-Ohmann H, et al. Early detection of neuropathophysiology using diffusion-weighted magnetic resonance imaging in asymptomatic cats with feline immunodeficiency viral infection[J]. J Neurovirol, 2001, 17(4): 341-352. |
| [17] | Wenserski F, von Giesen HJ, Wittsack HJ, et al. Human immunodeficiency virus 1-associated minor motor disorders: perfusion-weighted MR imaging and H MR spectroscopy[J]. Radiology, 2003, 228(1): 185-192. DOI: 10.1148/radiol.2281010683. |
| [18] | Thurnher MM, Castillo M, Stadler A, et al. Diffusion-tensor MR imaging of the brain in human immunodeficiency virus-positive patients[J]. AJNR Am J Neuroradiol, 2005, 26(9): 2275-2281. |
 2016, Vol. 37
2016, Vol. 37

