2. 广西中医药大学第一附属医院 广西 南宁 530023;
3. 广西中医药大学 广西 南宁 530001
2. The First Affiliated Hospital of Guangxi University of Chinese Medicine, Nanning 530023, China;
3. Guangxi University of Chinese Medicine, Nanning 530001, China
肝纤维化是各种慢性肝病向肝硬化发展过程中不可避免的组织病理学改变,主要表现在慢性肝病进展中纤维生成与降解平衡状态被破坏,致使肝内沉积过多的胶原,进而发展为肝硬化[1]。胆石病是临床常见病、多发病,其形成是遗传、环境、饮食、细菌感染等多种因素综合作用的结果[2]。胆结石的形成与慢性肝损伤密切相关,并与肝损伤的严重程度和性质有关。目前手术是结石的有效治疗手段,但其存在复发率高、手术创伤等多方面副作用,而经过长期临床及实验研究显示大黄灵仙颗粒预防及治疗结石有显著效果。因此,本次研究是在前期研究基础上并参考金博的模型制备方法建立慢性肝纤维化兔胆石病模型[3, 4],使用大黄灵仙颗粒进行干预,研究其对慢性肝纤维化胆石病的作用机制。
1 材料与方法 1.1 实验动物体重为2.5 kg、4月龄左右SPF级雄性新西兰大白兔50只(实验动物使用许可证:SYXK桂2011-0010,由右江民族医学院动物中心提供)。每笼2只,室内温度保持在20-24 ℃,控制湿度在42%-60%,适应性喂养1周后开始实验。
1.2 实验试剂各生化试剂管分别采购于南宁博仁生物技术有限公司;病理切片及染色试剂由右江民族医学院附院医院病理科提供。
1.3 实验药品①四氯化碳(由天津市进丰化工有限公司生产,500 ml/瓶);②橄榄油(由成都市科龙化工试剂厂生产,批号:20130513,规格:500 ml/瓶);③水合氯醛(成都市科龙化工试剂厂,批号:2014031102,规格:250 g/瓶);④胆固醇(由上海通用药业股份有限公司生产);⑤胆酸(购自德国Sigma公司,code:101335972,规格:100 g/瓶);⑥羟脯氨酸测定试剂盒(南京建成生物工程研究所,货号:A030-2,批号:20141104);⑦大黄灵仙颗粒制剂由广西中医药大学第一附属医院中心药房提供,药物组成及剂量如下:生大黄150 g,威灵仙300 g,芒硝100 g,金钱草300 g,枳壳120 g,鸡内金100 g,泽兰150 g,柴胡120 g,郁金120 g,磁石120 g,黄芪300 g,甘草50 g。上药按照广西壮族自治区药品监督管理局文件(桂药监注[2002]175号,桂药监注[2003]88号)批准的医院内制剂制作颗粒剂。
1.4 动物实验 1.4.1 实验动物的分组及模型建立将50只雄性新西兰大白兔随机分为3组:正常组、肝纤维化组、肝纤维化胆石病组,其中肝纤维化组、肝纤维化胆石病组各20只,正常组10只。肝纤维化组、肝纤维化胆石病组予20%的CCl4-橄榄油溶液腹腔注射0.2 ml/kg造模,每4 d一次,连续12周,同时肝纤维化胆石病组予高胆固醇、高热量致石饲料(普通饲料加入1.2%胆固醇、0.1%胆酸、5%蔗糖及3.5%鱼肝油)饲养,空白对照组正常饲养。
1.4.2 肝纤维化模型成功的标准病理学检查:将肝脏标本在体积比为10%多聚甲醛溶液中固定24-48 h,石蜡包埋,切片,采用HE染色。分期采用如下标准[4]:0期:正常,无纤维化;1期:肝小叶汇管区的纤维化扩大,但仍局限于肝窦周围以及肝小叶内纤维化;2期:纤维化明显集中于肝小叶汇管区及其周围,逐渐形成纤维间隔,仍保留完整小叶结构;3期:肝小叶纤维间隔明显伴结构紊乱,未出现肝硬化;4期:假小叶形成并增多,早期肝硬化。
1.4.3 胆结石造模成功标准解剖发现肉眼可见的结石,墨绿色或黑色,多呈不规则状或针尖样,其中少量大者如绿豆,小者呈泥沙样改变。
1.4.4 造模成功后分组及大黄灵仙颗粒剂干预药物注射12周病理明确肝纤维化形成后,将各组实验兔随机分为两组,即:正常组5只、正常+大黄灵仙颗粒组5只(以下称为:正常+Y组);肝纤维化组9只、肝纤维化+大黄灵仙颗粒组8只(以下称为:肝纤维化+Y组);肝纤维化胆石病组8只、肝纤维化胆石病+大黄灵仙颗粒组7只(以下称为:肝纤维化胆石病+Y组)。其中正常+Y组、肝纤维化+Y组、肝纤维化胆石病+Y组灌喂中药制剂大黄灵仙颗粒0.4 g/(kg·d),其余各组灌喂等量生理盐水,各组大白兔均正常饲料饲养。
1.4.5 中药药效评定标准病理观察提示肝纤维化病理改变减缓,相应生化指标好转,解剖提示胆囊或胆管结石形成几率减小。
1.5 标本采集用药12周后,用10%水合氯醛按4 ml/kg将实验兔麻醉,耳缘静脉采血,用作生化检测,取血后尽快送医院检验科进行检测检测指标包括:丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、总胆汁酸(TBA)、总胆红素(TBIL)、甘油三酯(TG)、总胆固醇(TC)。切取相同部位肝组织,大小为5 mm×5 mm×10 mm,将肝组织样品投入10%的多聚甲醛固定液,固定48 h后送检;另取体积为0.1 cm3大小肝脏组织,沿肝脏边缘切下肝脏组织,放入液氮罐中,并尽快置于-80 ℃超低温冰箱中保存备用,行羟脯氨酸含量测定;同时,观察胆囊结石情况并记录。取完标本后用空气栓塞法处死实验兔。
1.6 羟脯氨酸含量测定 1.6.1 操作方法①水解样本:精确称取湿重组织50 mg放入试管中,准确加入水解液1 ml,混匀,加盖后95 ℃水浴水解20 min;②加入调pH的乙液,调节pH值为6.0-6.8左右;③加双蒸水达10 ml,使混匀;④取4 ml稀释的水解液,加25 mg活性炭,使混匀,3 500 r/min离心10 min,取上清1 ml作测。⑤具体操作方法如下:先将1 ml的双蒸水、5×10-9 g/L标准应用液和检测液分别加到空白管、标准管和测定管中,然后向各管中各加入0.5 ml的试剂一,混匀后静置10 min;再加入0.5 ml的试剂二,混匀后静置10 min,最后加入0.5 ml的试剂三;混匀,60 ℃水浴15 min,冷却后,3 500 r/min离心10 min,取上清在550 nm处,1 cm光径,双蒸水调零,测各管吸光度。
1.6.2 肝组织羟脯氨酸含量的计算计算公式:
| $ \begin{gathered} 羟脯氨酸含量\left( { \times {{10}^6}\;{\text{ng/g}}湿重} \right) = \frac{{测定{\text{OD - 空白OD}}}}{{标准{\text{OD - 空白OD}}}} \times \hfill \\ 标准品含量\left( {5 \times {{10}^{ - 9}}\;{\text{g/L}}} \right) \times \frac{{水解液总体积\left( {10\;{\text{ml}}} \right)}}{{组织湿重\left( { \times {{10}^{ - 3}}\;{\text{g}}} \right)}} \hfill \\ \end{gathered} $ |
通过标本固定,脱水透明,石蜡包埋,切片使厚度在4 μm,展片;捞片、烘片脱去溶化组织间隙的石蜡,将烤好的切片,用弹簧夹夹好,放入仪器中自动进行HE染色,取出吹干、封片。干燥后观察切片病理变化。
1.8 统计学分析采用SPSS 17.0统计软件进行数据分析,方差齐时,各组间计量资料比较采用两样本t检验,方差不齐时采用秩和检验。计量数据以均数±标准差(x±s)表示,P < 0.05表示差异有统计学意义。
2 结果 2.1 各组实验兔死亡率、成石率结果比较在连续注射CCl4-橄榄油溶液12周后,统计各组实验兔的死亡率、成石率。计算公式为:死亡率=(原始例数-剩余例数)/原始例数×100%,成石率=存活例数/原始例数×100%。结果正常组、纤维化组、纤维化胆石病组的存活例数分别是10只、17只、15只,成石例数分别0只、1只、14只,死亡率分别是0%、15%、25%,成石率分别是0%、5.9%、70%。
2.2 血清生化指标检测结果与未喂食大黄灵仙颗粒的对照组相比,各喂食大黄灵仙颗粒组的ALT、AST、TBIL、TBA、TG和TC均有不同程度的偏高(均为P<0.05),说明大黄灵仙颗粒在减轻肝损伤方面有一定疗效。见表 1。
| 表 1 各组血清生化指标的比较(U/L, x±s) |
与未喂食大黄灵仙颗粒的对照组相比,各喂食大黄灵仙颗粒组的吸光度均有不同程度偏低,(均为P<0.05),说明大黄灵仙颗粒在减轻肝纤维化方面有一定疗效。具体结果见表 2。
| 表 2 各组大白兔羟脯氨酸含量的测定(x±s,mg/g) |
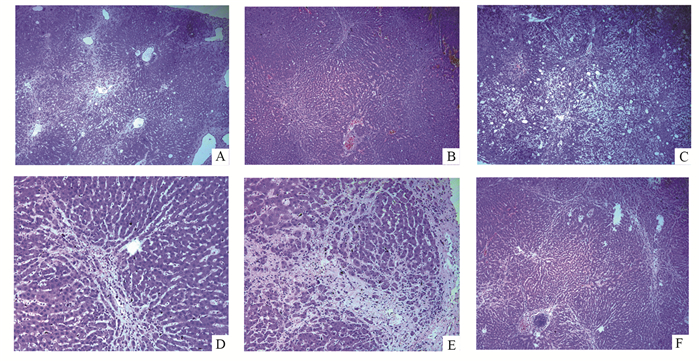
用药12周后,正常组、正常对照组+大黄灵仙胶囊组可观察到肝小叶结构完整,肝细胞索排列整齐,肝血窦间隙未见明显异常,未见炎性细胞浸润,两者未见明显差异(见图 1A、1B,均为HE染色,下同)。肝纤维化组、肝纤维化胆石病组:光镜下可见部分肝小叶结构不完整,肝细胞索排列紊乱,肝血窦间隙逐步增大,出现胆管增生、肝细胞肿胀,纤维组织增多,纤维化胆石病组症状较重些,有些出现假小叶(见图 1C、1D)肝纤维化组+大黄灵仙颗粒组、肝纤维化胆石病组+大黄灵仙颗粒组:光镜下可见遭到破坏的肝小叶逐渐修复,肝细胞排列稍规则,汇管区纤维有所减少,仍有少量淋巴细胞浸润,未见假小叶,肝纤维化+大黄灵仙颗粒组症状较轻,肝功能恢复较快(见图 1E、1F)。
|
图 1 各用药组与对照组病理结果(HE×40) A.正常组;B.正常+大黄仙灵;C.肝纤维化组;D.肝纤维化治疗组;E.肝纤维化胆石病组;F.肝纤维化胆石病治疗组 |
本实验采用CCl4-橄榄油溶液腹腔注射进行慢性肝损伤动物模型构建,同时慢性肝纤维化胆石病组予高胆固醇、高热量致石饲料饲养,进行慢性肝纤维化兔胆石病模型的构建。在造模过程中发现慢性肝纤维化胆石病组的死亡率(25%)较正常组(0%)、肝纤维化组(10%)偏高。肝纤维化会使肝细胞和胆管上皮细胞遭到进行性破坏,肝脏细胞呈现代偿性增生,肝内纤维生成与降解失衡,致使过多的胶原在肝内沉积,同时伴随着肝脏纤维组织过度增生的复杂过程,在各种慢性肝病进展中由于常伴有炎症并可发展为肝硬化[5]。许多研究表明:肝脏与胆结石的形成紧密相关,肝脏不仅是唯一产生胆汁的器官,且是产生致石性胆汁(如减少胆汁酸的合成、增多非结合胆红素等改变胆汁成分)的场所[6]。胆结石的形成主要与胆汁成分的改变相关,肝细胞在正常生理状态下分泌各种胆汁酸,各成分的比例总是维持在一个相对恒定的范围内[7]。肝脏病变时,肝脏功能降低,胆汁主要成分改变,胆囊功能降低,免疫功能下降,多种因素产生协同作用,促使胆石病发生率升高;肝硬变时肝内酶产生不足,胆固醇向胆汁酸的转化减少,导致血清胆汁酸减少,促使胆汁酸池缩小,增加胆固醇易于聚集、沉淀而形成结石。
羟脯氨酸(hydroxyproline, Hyp)是一种非必需氨基酸,为胶原蛋白分子所特有,多分布在皮肤、腱、软骨和血管等处,大约占胶原蛋白氨基酸总含量的13.4%。通过羟脯氨酸含量测定可以反映结缔组织疾病中胶原代谢情况。肝纤维化时肝内增加的主要成分则是胶原纤维,因此测定肝脏组织的Hyp含量,是直接反映肝脏纤维化程度的重要指标[8]。本项目通过测定各组实验兔肝组织羟脯氨酸含量,发现大黄灵仙颗粒治疗组肝组织吸光度均有不同程度下降,单纯肝纤维化组降低的程度较慢性肝纤维化胆石病组更为明显,正常组实验兔无明显改变,说明大黄灵仙颗粒除在胆石病的防治方面外,在保护肝组织减轻肝损伤方面,有着独特的优势。
同时,大黄灵仙颗粒能够有效改善肝功能异常,降低转氨酶、胆红素等指标,增加血清总胆汁酸、总胆固醇、甘油三酯含量,通过促进肝脏功能恢复,改变胆汁成分,减少致石性胆汁的形成,具有良好的减少结石形成的作用[9]。病理结果显示喂食大黄灵仙颗粒的药物组光镜下可见遭到破坏的肝小叶逐渐修复,肝细胞排列稍规则,汇管区纤维增宽、减少,未见明显胆管增生,对减轻胆汁淤积、肝损伤修复具有良好的作用。解剖后发现药物组的实验兔胆囊内的结石明显少于对照组,考虑大黄灵仙颗粒制剂对已形成的结石具有减少和预防复发的作用。项目组前期研究结果表明肝损伤与胆结石的形成有关,对各组实验兔血浆的1H NMR谱图进行观察比较后发现,大黄灵仙颗粒具有降低低密度脂蛋白、丙氨酸和甘油含量的作用,减少胆结石的形成,并提高胆碱、牛磺酸含量,进而保护肝细胞功能及结构完整。通过其代谢组学特征及超微病理改变,均说明大黄灵仙颗粒有预防胆结石的作用[10]。通过本实验研究证实大黄灵仙颗粒可降低肝损害,改善肝组织病理结构,对慢性肝纤维化胆石病具有较好的干预作用,其具体作用机制将有待进一步深入研究。
| [1] | Ferro JM, Oliveira S. Neurologic manifestations of gastrointestinal and liver diseases[J]. Curr Neurol Neurosci Rep, 2014, 14(10): 487. DOI: 10.1007/s11910-014-0487-z. |
| [2] | Kwon YH, Cho CM, Jung MK, et al. Risk factors of open converted cholecystectomy for cholelithiasis after endoscopic removal of choledocholithiasis[J]. Dig Dis Sci, 2015, 60(2): 550-556. DOI: 10.1007/s10620-014-3337-6. |
| [3] | Jin B, Alter HJ, Zhang ZC, et al. Reversibility of experimental rabbit liver cirrhosis by portal collagenase administration[J]. Lab Invest, 2005, 85(8): 992-1002. DOI: 10.1038/labinvest.3700304. |
| [4] |
王兵, 秦军, 俞渊, 等. 慢性肝损伤兔胆石病动物模型的构建[J].
右江民族医学院学报, 2015, 37(2): 271-274.
Wang B, Qin J, Yu Y, et al. Establishment of the Cholelithiasis Animal Model in Rabbits with Chronic Liver Injures[J]. Journal of Youjiang Medical College For Nationalities, 2015, 37(2): 271-274. |
| [5] |
中华肝脏病学会肝纤维化学组. 肝纤维化诊断及疗效评估共识[J].
药品评价, 2007, 4(4): 265-266.
The liver fibrosis group of the Chinese Society of Hepatology. Diagnosis of liver fibrosis and curative effect evaluation[J]. Drug Evaluation, 2007, 4(4): 265-266. |
| [6] | Ding GQ, Cai W, Qin MF. Is intraoperative cholangiography necessary during laparoscopic cholecystectomy for cholelithiasis[J]. World J Gastroenterol, 2015, 21(7): 2147-2151. |
| [7] | Clichici S, Olteanu D, Nagy AL, et al. Silymarin inhibits the progression of fibrosis in the early stages of liver injury in CCl4-treated rats[J]. J Med Food, 2015, 18(3): 290-298. DOI: 10.1089/jmf.2013.0179. |
| [8] |
张宇飞, 王峰, 宗光全, 等. 合并肝硬化门脉高压症胃癌患者手术后并发症的危险因素分析[J].
中华胃肠外科杂志, 2015, 18(1): 30-32.
Zhang YF, Wang F, Zong GQ, et al. Risk factor analysis of postoperative complications in gastric carcinoma patients complicated with liver cirrhosis[J]. Chin J Gastrointest Surg, 2015, 18(1): 30-32. |
| [9] | Yu F, Ji S, Su L, et al. Adipose-derived mesenchymal stem cells inhibit activation of hepatic stellate cells in vitro and ameliorate rat liver fibrosis in vivo[J]. J Formos Med Assoc, 2015, 114(2): 130-138. DOI: 10.1016/j.jfma.2012.12.002. |
| [10] |
唐乾利, 黄欣, 俞渊, 等. 兔胆石症的代谢组学特征及大黄灵仙胶囊的干预作用[J].
医学导报, 2013, 32(12): 1538-1542.
Tang QL, Huang X, Yu Y, et al. Characteristics of Metabolism in Rabbits with Gallstone and Intervention by Dahuanglingxian Capsule[J]. Herald of Medicine, 2013, 32(12): 1538-1542. |
| [11] |
俞渊, 唐乾利, 黄欣, 等. 大黄灵仙胶囊防治兔胆石病的代谢组学及超微病理研究[J].
中华中医药杂志, 2013, 28(11): 3359-3362.
Yu Y, Tang QL, Huang X, et al. Dahuang Lingxian Capsule for prevention and treatment of rabbit cholelithiasis[J]. China Journal of Traditional Chinese Medicine and Pharmacy, 2013, 28(11): 3359-3362. |
 2017, Vol. 38
2017, Vol. 38
