2. 河南科技大学医学院病原生物学教研室 河南 洛阳 471003
2. Dept. of Pathogen Biology, Medical College of Henan University of Science and Technology, Luoyang 471003, Henan, China
硫化氢(hydrogen sulfide, H2S)是继一氧化氮、一氧化碳后的第三种重要的气体信号分子。内源性的H2S在心血管组织内主要通过胱硫醚-γ-裂解酶(cystathionine-γ-lyase,CSE)催化产生,是体内H2S的重要来源之一。近年,H2S在对抗缺氧、缺血引起的心肌损伤中的作用日益受到重视[1]。Kang等[2]报道H2S能减轻培养的心肌细胞及整体大鼠心脏缺血再灌注引起的损伤。细胞在受到如缺氧、氧化应激、钙离子稳态失衡、异常糖基化、内质网内氧化还原环境紊乱等刺激时,内质网内环境稳态失衡,可触发内质网应激(endoplasmic reticulum stress,ERS)。最近,Toko[3]等在对ATF6通路的激活对心肌缺血再灌注损伤引起的内质网应激中的重要性研究中发现,阻断ATF6可使缺血大鼠心脏心功能恶化、心肌梗死面积增加,提示内质网应激中ATF6通路的激活对心肌缺血再灌注有保护作用。另有研究显示,通过基因敲除、microRNA技术沉默ATF6后,体外培养的心肌细胞内GRP78蛋白的表达量降低,细胞凋亡数目增多[4],进一步提示ATF6通路的激活在心肌组织应激损伤中的重要性。基于上述研究现状,本实验利用H9C2细胞建立心肌细胞缺氧/复氧(hypoxia/reoxygenation, H/R)模型,探讨H2S后处理在心肌细胞缺血再灌注损伤中的保护作用及其与ATF6活化的内质网应激间的关系。
1 材料与方法 1.1 实验材料 1.1.1 细胞株H9C2细胞购自武汉博士德生物工程有限公司。
1.1.2 药物与试剂NaHS (H2S供体)、DMSO、PAG (胱硫醚-γ-裂解酶阻断剂)(美国Sigma公司);高糖型DMEM溶液、F12培养液(吉诺生物医药技术有限公司);胎牛血清(杭州四季青有限公司);Trizol试剂(美国Invitrogen公司);逆转录试剂盒、SYBR Green Real-time PCR Master Mix (日本TOYOBO公司);大鼠GRP78单克隆抗体、大鼠ATF6单克隆抗体(美国Santa Cruz公司);羊抗鼠IgG-HRP (科瑞公司)。
1.1.3 仪器二氧化碳培养箱(法国Jouan公司);三气培养箱(长沙华曦电子科技有限公司);倒置显微镜(日本Olympus有限公司);超净工作台(苏净安泰);冷冻离心机(美国Thermo Electron公司);凝胶成像系统(法国Vilber Fusion fx7公司);流式细胞仪(美国Beckman公司);荧光酶标仪(奥地利TECAN GENios VA200);PCR仪、荧光定量PCR仪(美国Bio-rad公司)。
1.2 模型的建立及主要指标的观察、检测 1.2.1 H9C2细胞培养H9C2细胞培养于含10%FBS、1%双抗的高糖型DMEM培养基中,于37 ℃、5%CO2及饱和湿度条件的密闭培养箱内培养,当培养瓶内细胞生长至80%-90%融合时,按1:3传代。细胞按5×105个/ml接种至30 mm培养皿或6孔板。
1.2.2 实验分组实验时用F12培养液置换正常培养液,于37 ℃、5% CO2、94%N2及饱和湿度条件作为缺氧培养;弃去F12培养液换等量含10% FBS高糖型DMEM培养液,于37 ℃、5% CO2及饱和湿度条件下作为复氧培养,建立缺氧/复氧损伤模型[5]。所给药物均在缺氧后复氧前给予。实验分组:①正常对照组(con):正常细胞培养,不做任何处理;②缺氧/复氧组(H/R):按上述方法缺氧12 h,复氧4 h;③NaHS后处理组(H/R+NaHS):同上,在复氧时加入200 μmol/L NaHS;④CSE阻断剂干预组(H/R+PAG):复氧时加入10 μmol/L PAG。
1.2.3 实时荧光定量PCR检测CSE mRNA相对表达量用Trizol试剂提取细胞中总RNA,紫外分光光度计测量RNA样品的纯度,OD260/280值在1.8-2.0之间的RNA样品进行RT-PCR。cDNA合成按照Toyobo RNA PCR kit说明书操作,将mRNA反转录成cDNA,进行半定量PCR反应。根据GenBank中大鼠的CSE及GAPDH序列设计相应引物,
CSE正义:5′-TCCGGATGGAGAAACACTTC-3′;
CSE反义:5′-GCTGCCTTTAAAGCTTGACC-3′;
GAPDH正义:5′-GCCTTCCGTGTTCCTACC-3′;
GAPDH反义:5′-AGAGTGGGAGTTGCTGTT-3′。使用实时荧光定量PCR仪进行实验,反应条件如下:95 ℃ 1 min,95 ℃ 10 s,60 ℃ 30 s,共40个循环。
1.2.4 倒置显微镜观察细胞形态倒置显微镜观察各组H9C2细胞形态的变化。
1.2.5 PI单染检测细胞凋亡率各组细胞用胰酶消化后,收集细胞悬液;1 200 r/min×6 min离心,弃上清;70%冷乙醇重悬固定,-20 ℃过夜;离心,弃上清;用50 μg/ml PI染液避光染色10 min;过滤后用流式细胞仪检测细胞内DNA的含量(激发波长:488 nm;发射波长:610 nm)。
1.2.6 Western blotting检测ATF6、GRP78的表达各组模型制备后,D-hanks洗两次,弃上清,加入蛋白裂解液;离心,取上清,采用BCA法进行蛋白定量。总蛋白经SDS-PAGE分离后,转移至PVDF膜上。加入新鲜封闭液稀释的一抗(稀释比例ATF6 1:300;GRP78 1:500),4 ℃冰箱中孵育过夜,用TBST洗5次,加入羊抗鼠IgG-HRP (1:5 000),孵育1.5 h,漂洗3次。ECL显色后,用Image J图像分析软件定量分析。
1.2.7 统计学方法采用Image J、SPSS 16.0软件分析,数据以x±s表示,统计分析采用正态分布检验、方差齐性检验、单因素方差分析等对数据进行统计学处理,P<0.05为差异有统计学意义。
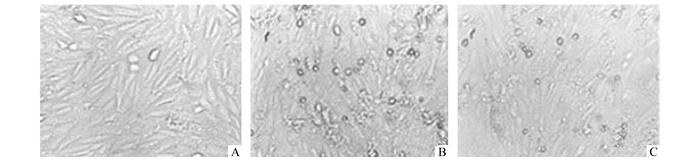
2 结果 2.1 倒置显微镜下细胞形态学变化H9C2细胞常规培养,倒置显微镜下观察细胞形态如图 1所示。对照组细胞呈梭形、细胞间间隙正常(A);H/R组细胞损伤后,细胞边缘皱缩,且细胞间间隙增大(B);在缺氧后给予200 μmol/L NaHS后处理,细胞损伤情况较缺氧/复氧组明显减轻(C)。
|
图 1 各组H9C2细胞的形态(×20) A:对照组;B:缺氧/复氧组;C:缺氧/复氧+NaHS后处理组 |
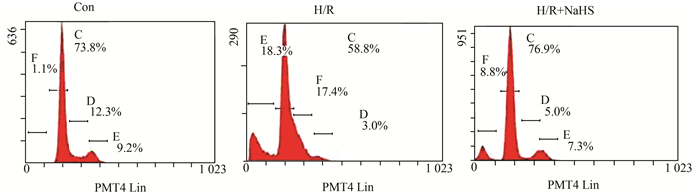
如图 2所示,与对照组(1.0±0.36)%比较,缺氧12 h复氧4 h细胞凋亡率为明显升高[(20.3±2.4)% vs (1.0±0.36)%, P<0.01],而NaHS后处理可明显降低缺氧/复氧损伤细胞凋亡率。
|
图 2 NaHS后处理对缺氧/复氧细胞凋亡率的影响 Con:对照组;H/R:缺氧/复氧组;H/R+NaHS:缺氧/复氧+NaHS后处理组 |
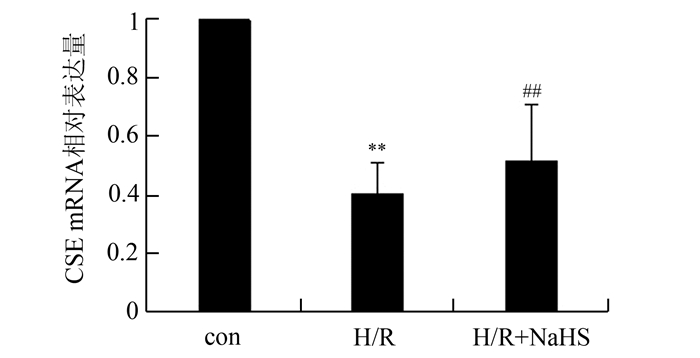
各组CSE mRNA的相对表达量如图 3所示,con组相对表达量设为1,H/R组CSE mRNA表达量较con组明显降低(0.41±0.10 vs 1.0±0.28, P<0.01);H/R+ NaHS组较H/R组明显升高(0.51±0.20 vs 0.41±0.10, P<0.01)。上述结果提示,200 μmol/L NaHS可改善缺氧复氧引起的心肌细胞CSE mRNA表达的降低。
|
图 3 各组CSE mRNA相对表达量
对照组;H/R:缺氧/复氧组;H/R+NaHS:缺氧/复氧+NaHS后处理组 **P<0.01,与正常对照组比较;# #P<0.01,与缺氧/复氧组比较 |
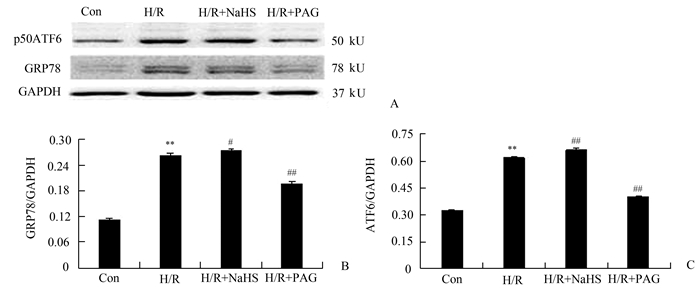
内质网应激时,可促进内质网跨膜蛋白ATF6(p90 ATF6)转位至高尔基体,经裂解后生成具有转录活性的p50ATF6。Western blotting结果如图 4所示,与对照组比较,H/R组p50ATF6、GRP78蛋白表达量均明显升高,分别为:(0.620±0.003 vs 0.320±0.003, P<0.01; 0.260±0.005 vs 0.110±0.004, P<0.01)。与H/R组比较,H/R+NaHS组p50ATF6和GRP78表达量均升高,分别为:(0.660±0.008 vs 0.620±0.003, P<0.01; 0.270±0.004 vs 0.260±0.005, P<0.05);给予H2S合成酶CSE抑制剂后,即H/R+PAG组p50ATF6、GRP78均较H/R组蛋白表达量降低,分别为:(0.400±0.006 vs 0.620±0.003, P<0.01; 0.190±0.005 vs 0.260±0.005, P<0.01)。
|
图 4 各组H9C2细胞中ATF6、GRP78蛋白表达的变化
A:Western blotting检测显示各组心肌细胞ATF6、GRP78的表达;B、C:各组ATF6、GRP78蛋白的相对表达量 Con:对照组;H/R:缺氧/复氧组;H/R+NaHS:缺氧/复氧+NaHS后处理组;H/R+PAG:缺氧/复氧+ PAG后处理组 **P<0.01,与正常对照组比较;#P<0.05,# #P<0.01,与缺氧/复氧组比较 |
在心血管系统内内源性H2S主要是由胱硫醚-γ-裂解酶(CSE)催化L-半胱氨酸合成的,对机体心血管功能的病理、生理性调节发挥着重要的作用,已成为心血管系统研究的新热点。相关文献已证明内源性H2S的减少与心肌缺血再灌注损伤明显有关,给予外源性H2S后处理对整体水平大鼠及细胞水平心肌缺血复氧损伤均具有保护作用[1, 6]。本实验通过采用形态学和PI单染流式细胞检测术观察NaHS后处理对缺氧/复氧损伤心肌细胞的影响,结果均提示NaHS后处理可减轻缺氧/复氧所致的心肌细胞损伤,这一结果与文献报道一致[7]。实时定量PCR检测CSE mRNA的相对表达量显示:与对照组比较,H/R组CSE mRNA表达量降低(P<0.01),而NaHS后处理组其表达量较H/R组明显升高(P<0.01)。这一结果提示NaHS后处理可改善缺氧/复氧引起的心肌细胞CSE mRNA表达的降低。
内质网应激参与心脏的发育和多种心脏疾病的发生发展,包括心肌缺血和再灌注损伤,心肌病和心力衰竭等[8]。ERS有关的细胞凋亡及其分子机制是目前生物医学领域致力研究的细胞生物学现象。内质网应激可通过三个感受器蛋白(ATF6、PERK、IRE1)介导激活未折叠蛋白反应(unfolded protein response,UPR),使早期蛋白质合成暂停。其中ATF6途径介导的UPR在心肌保护中起着重要作用[3]。ERS发生时,ATF6可释放出分子质量约50 kU的活性片段,即p50ATF6。p50ATF6转移至细胞核内,可引起内质网分子伴侣如GRP78、PDI等基因的表达[9, 10],进而促进对蓄积在内质网内的错误折叠和未折叠蛋白质的处理,有利于维持细胞的正常功能并使之存活。
为进一步探讨H2S保护心肌缺血再灌注损伤是否涉及活化ATF6从而降低内质网应激损伤,本实验通过检测ERS相关蛋白ATF6和GRP78的表达,研究H2S后处理对H9C2心肌细胞H/R诱导的ERS的影响。结果显示,H/R组p50ATF6、GRP78蛋白表达量均较对照组明显升高;而H/R+NaHS组p50ATF6和GRP78表达量均较H/R升高,此结果提示缺氧/复氧损伤可使心肌细胞内p50ATF6、GRP78代偿性增高;而外源性H2S可进一步活化p50ATF6进而提高内质网分子伴侣GRP78的表达,以帮助蛋白折叠而发挥保护作用。在细胞H/R损伤基础上给予H2S合成酶CSE抑制剂PAG阻断H2S的合成后,结果显示,p50ATF6和GRP78均较H/R组蛋白表达量降低,提示PAG可通过阻断H/R过程中内源性H2S的合成进而抑制p50ATF6和GRP78的增高,从而降低其保护作用。
综上所述,H2S在心肌缺血性疾病中发挥重要的保护作用。本实验初步探讨了外源性H2S后处理保护心肌细胞缺氧/复氧损伤可能涉及其活化ATF6,启动内质网应激,上调GRP78蛋白表达来发挥心肌保护作用。
| [1] | Polhemus DJ, Calvert JW, Butler J, et al. The cardioprotective actions of hydrogen sulfide in acute myocardial infarction and heart failure[J]. Scientifica (Cairo), 2014, 2014: 768607. |
| [2] | Kang B, Hong J, Xiao J, et al. Involvement of miR-1 in the protective effect of hydrogen sulfide against cardiomyocyte apoptosis induced by ischemia/reperfusion[J]. Mol Biol Rep, 2014, 41(10): 6 845-6 853. DOI: 10.1007/s11033-014-3570-2. |
| [3] | Toko H, Takahashi H, Kayama Y, et al. ATF6 is important under both pathological and physiological states in the heart[J]. J Mol Cell Cardiol, 2010, 49(1): 113-120. DOI: 10.1016/j.yjmcc.2010.03.020. |
| [4] | Doroudgar S, Thuerauf DJ, Marcinko MC, et al. Ischemia activates the ATF6 branch of the endoplasmic reticulum stress response[J]. J Biol Chem, 2009, 284(43): 29 735-29 745. DOI: 10.1074/jbc.M109.018036. |
| [5] | Hu F, Koon CM, Chan JY, et al. The cardioprotective effect of danshen and gegen decoction on rat hearts and cardiomyocytes with post-ischemia reperfusion injury[J]. BMC Complement Altern Med, 2012, 12: 249. DOI: 10.1186/1472-6882-12-S1-P249. |
| [6] | Yang Z, Yang C, Xiao L, et al. Novel insights into the role of HSP90 in cytoprotection of H2S against chemical hypoxiainduced injury in H9C2 cardiac myocytes[J]. Int J Mol Med, 2011, 28(3): 397-403. |
| [7] | Szabó G, Veres G, Radovits T, et al. Cardioprotective effects of hydrogen sulfide[J]. Nitric Oxide, 2011, 25(2): 201-210. DOI: 10.1016/j.niox.2010.11.001. |
| [8] | Brown DI, Griendling KK. Regulation of signal transduction by reactive oxygen species in the cardiovascular system[J]. Circ Res, 2015, 116(3): 531-549. DOI: 10.1161/CIRCRESAHA.116.303584. |
| [9] | Minamino T, Komuro I, Kitakaze M. Endoplasmic reticulum stress as a therapeutic target in cardiovascular disease[J]. Circ Res, 2010, 107(9): 1 071-1 082. DOI: 10.1161/CIRCRESAHA.110.227819. |
| [10] | Benham AM. The protein disulfide isomerase family:key players in health and disease[J]. Antioxid Redox Signal, 2012, 16(8): 781-789. DOI: 10.1089/ars.2011.4439. |
 2016, Vol. 37
2016, Vol. 37

