2. 武汉大学人民医院 检验科 湖北 武汉 430060;
3. 武汉大学人民医院 心内科 湖北 武汉 430060
2. Dept. of Clinical libratory, Renmin Hospital of Wuhan University, Wuhan 430060, China;
3. Dept. of Cardiology, Renmin Hospital of Wuhan University, Wuhan 430060, China
急性肺损伤(acute lung injury,ALI)是临床常见的危重症,病死率居高不下,认识其发病机制是寻找有效治疗措施,改善预后的关键。多种炎症细胞、炎症介质参与其发生发展,炎症介质/抗炎症介质失衡是目前的研究热点。新近的研究显示CXC趋化因子受体3(CXCR3)可通过募集CD8+T细胞及促进干扰素-γ(IFN-γ)和IFN-γ诱导蛋白-10(IFN-γ induced protein-10,IP-10/CXCL10)等细胞因子的释放而启动炎症级联反应。而白细胞介素-10(Interleukin 10,IL-10)是一种重要的抗炎因子,对CD8+T细胞有抑制作用,可减轻ALI的炎症反应。本实验探讨CXCR3在LPS所致小鼠ALI发病机制中的作用及与IL-10的关系,为该病的防治提供理论依据和新的方法。
1 材料与方法 1.1 实验动物24只健康10-12周龄雄性C57BL/6小鼠,体重20-22 g/只,购自湖南斯莱克景达实验动物有限公司,动物合格证号:HNASLKJ20122321。
1.2 主要仪器与试剂内毒素脂多糖(LPS)、牛血清白蛋白(BSA)、藻红蛋白(PE)、异硫氰酸荧光素(FITC)、RPMI-1640培养液、胎牛血清(FBS)、青链霉素双抗、胶原酶、ELISA试剂盒(美国Sigma公司),磷酸缓冲盐(PBS)、乌拉坦(北京化工厂),Trizol Reagent (美国Invitrogen公司),EPICS XL型流式细胞仪(美国COULTER公司),实时荧光定量PCR仪(美国Illumina公司),cytospin2Ⅱ型细胞离心涂片机(英国SHANDON公司)。
1.3 方法 1.3.1 动物分组及造模将24只雄性C57BL/6小鼠随机分为正常组、LPS 2 h组及LPS 12 h组,每组8只。LPS 2 h组及LPS 12 h组通过尾静脉注射LPS (10 mg/kg)制作ALI模型,并分别于造模后2 h和12 h获取标本。
1.3.2 标本采集用12%乌拉坦(0.15 ml/10 g)腹腔注射过量麻醉处死并固定小鼠。动静脉留置针进行气管插管,用PBS灌洗肺组织并获取肺泡细胞灌洗液(bronchoalveolar lavage fluids,BALF)。细胞计数板计数细胞总数,行流式细胞检测及ELISA测定。肺组织分别行流式细胞检测、荧光定量PCR检测及HE染色。
1.3.3 CD8+T细胞和CD4+T细胞表达的流式细胞分析将BALF离心后弃上清,加入流式细胞封闭液(BSA +PBS配制)重悬浮细胞层。以PE标记的CD4+和FITC标记的CD8+ T细胞,在流式细胞仪上分析T细胞亚群。肺组织在流式细胞工作液(RPMI1640+FBS+青链霉素双抗+胶原酶+DNAase配制)中剪碎,离心后弃上清,加入流式细胞封闭液重悬浮细胞层。加入PE标记的CD4+T细胞和FITC标记的CD8+T细胞,上机检测。
1.3.4 BALF细胞分类计数将BALF离心后用PBS重悬浮细胞,并进行点片,空气干燥后用95%乙醇固定15 min,行HE染色。显微镜下进行细胞分类计数。
1.3.5 ELISA检测BALF中炎症因子的表达取BALF上清液检测IL-10和CXCR3的表达。实验步骤严格按照ELISA试剂盒说明书进行。
1.3.6 实时荧光定量PCR检测小鼠肺组织中CXCR3和IL-10 mRNA的表达引物探针由武汉金斯瑞生物科技有限公司设计和合成。各引物序列详见表 1。按照试剂盒说明书提取细胞总RNA并逆转录为cDNA。在PCR上以cDNA为模板扩增CXCR3、IL-10和β-actin,将回收产物作为标准品,计算出拷贝数并行荧光定量PCR,根据每个标准品达到阈值时的循环数(Ct值)绘制标准曲线,再由标准曲线和样品的Ct值计算出样本的初始拷贝数。
| 表 1 PCR扩增引物序列 |
采用SPSS 19.0统计软件进行统计分析,数据以x±s表示。计量资料分别以t检验及方差分析评价其差异的显著性,相关性分析采用Pearson相关系数。P<0.05为差异具有统计学意义。
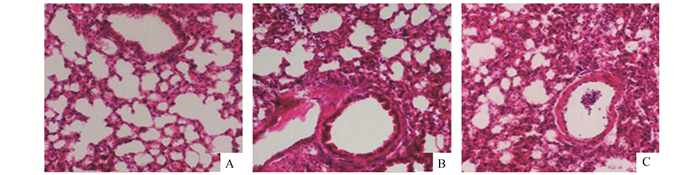
2 结果 2.1 肺组织HE染色结果正常组小鼠气道上皮结构完整,肺泡结构正常。肺泡内未见炎性细胞浸润,肺泡间隔无明显水肿。LPS 2 h及12 h组气道黏膜上皮细胞部分脱落,部分气道壁有炎症细胞浸润,部分肺泡间隔增宽。且LPS 12 h组气道壁炎症细胞浸润及肺泡间隔增宽程度更重(图 1)。
|
图 1 各组小鼠肺组织病理学改变(HE×400) A.正常组; B. LPS 2 h组; C. LPS 12 h组 |
LPS 12 h组BALF白细胞总数、淋巴细胞数、中性粒细胞数及巨噬细胞数均较LPS 2 h组和正常组明显增高(P<0.05)。LPS 2 h组BALF白细胞总数及中性粒细胞数较正常组明显增高,具有统计学意义(P<0.05)(表 2)。
| 表 2 各组小鼠BALF细胞分类的变化(x±s) |
LPS 12 h组小鼠BALF与肺组织中CD8+T细胞的百分比均较正常组及LPS 2 h组显著升高(P<0.05)。LPS 2 h组小鼠BALF与肺组织中CD8+T细胞数较正常组明显升高(P<0.05)。LPS 12 h组小鼠BALF与肺组织中CD4+T细胞百分比明显低于正常组及LPS 2 h组(P<0.05),而正常组与LPS 2 h组CD4+T细胞差异无统计学意义(P>0.05,表 3、表 4)。
| 表 3 各组小鼠BALF中T细胞亚群检测结果的比较(x±s) |
| 表 4 各组小鼠肺组织中T细胞亚群检测结果的比较(x±s) |
LPS 12 h组小鼠BALF中CXCR3的表达显著高于正常组和LPS 2 h组(P<0.05),且LPS 2 h组高于正常组(P<0.05)。正常组与LPS 2 h组BALF中IL-10的表达均较LPS 12 h组明显升高,具有统计学意义(P<0.05),且正常组高于LPS 2 h组(P<0.05,表 5)。
| 表 5 各组小鼠BALF中炎症因子表达情况(x±s) |
LPS 12 h组小鼠肺组织中CXCR3 mRNA的表达显著高于正常组和LPS 2 h组(P<0.05),LPS 2 h组CXCR3 mRNA的表达高于正常组(P<0.05)。正常组与LPS 2 h组小鼠肺组织中IL-10 mRNA的表达均较LPS 12 h组明显升高,具有统计学意义(P<0.05),且正常组高于LPS 2 h组(P<0.05,表 6)。
| 表 6 各组小鼠肺组织中炎症因子mRNA表达情况(x±s) |
小鼠BALF及肺组织中CXCR3的表达均与IL-10呈负相关,相关系数r分别为-0.969、-0.664(P<0.05)。小鼠BALF及肺组织中CD8+T细胞数与IL-10的表达亦呈负相关,相关系数r分别为-0.965、-0.612(P<0.05)。
3 讨论ALI是指由严重感染、休克、创伤及烧伤等心源性以外的各种因素导致的肺实质损伤,是常见的危重症,认识其发病机制是寻找有效治疗措施,改善预后的关键。研究认为,ALI时中性粒细胞、淋巴细胞等多种炎症细胞在肺内聚集以及血管内皮细胞的功能受损,释放多种炎症介质、氧自由基、蛋白酶,炎症介质/抗炎症介质失衡机制在其发生发展过程中起重要作用[1]。因此,阻断炎症介质和细胞因子的释放,重建炎症介质/抗炎症介质平衡成为治疗ALI的研究热点。
IL-10主要由T细胞、巨噬细胞和活化的B细胞产生,对CD8+T细胞有抑制作用,是一种重要的抗炎细胞因子和免疫抑制剂,可抑制单核细胞分泌多种细胞因子,减少前炎症介质和细胞因子的释放,发挥抗炎作用[2, 3]。我们推测,IL-10的激活可能下调ALI炎症反应。趋化因子是重要的细胞因子,与趋化因子结合后,可募集炎症细胞,释放细胞因子,从而在机体炎症中发挥作用[4]。研究显示,CXCR3可由炎症细胞、气道上皮细胞、内皮细胞等释放,主要表达于活化的T细胞、自然杀伤细胞和肺泡巨噬细胞等表面,在炎症反应中起重要作用[5]。研究发现[6],CXCL10通过与CXCR3结合而趋化炎症细胞,参与肺部炎症的发展和损伤。CXCR3是慢性阻塞性肺疾病(COPD)的重要炎症介质,可能是通过调节细胞免疫反应和炎性细胞因子的产生,从而介导COPD肺部炎症反应过程,并与气流受限程度呈负相关[7]。COPD患者的肺内淋巴细胞分泌更多的IFN-γ、CXCL9以及CXCL10,其中IFN-γ由Th1细胞释放,而CXCL9和CXCL10与CXCR3结合,可吸引Th1细胞并诱导肺内巨噬细胞分泌基质金属蛋白酶-12(MMP-12)增加,导致肺组织的破坏和肺气肿的产生[8]。我们的前期实验亦显示,CD8+T细胞募集可使IFN-γ分泌增加,从而诱导CXCR3释放,进而促进吸烟导致的ALI的炎症反应[9, 10]。
LPS是脂质和多糖的复合物,为革兰阴性杆菌细胞壁的主要成分,是内毒素的特异性抗原(O抗原)。LPS不仅可通过刺激中性粒细胞、内皮细胞等炎症细胞产生炎症介质和细胞因子,还可损伤肺泡毛细血管膜,使之通透性升高,从而诱发ALI。我们的实验显示,LPS 12 h组小鼠BALF中多种炎症细胞较正常组及LPS 2 h组增多。结合HE染色结果,表明我们成功制备LPS致小鼠ALI模型,并且随着LPS作用时间的延长,炎症程度加重。ALI时CD8+T细胞募集增加,CXCR3的表达增加,且LPS 12 h组BALF及肺组织中CXCR3的释放较正常组及LPS 2 h组增多。IL-10亦参与LPS所致小鼠ALI的炎症反应过程,且IL-10与CXCR3的变化呈负相关。我们采用流式细胞术测定对照组小鼠和不同时间点ALI小鼠BALF和肺组织CD8+T细胞的百分比,结果显示CD8+ T细胞的变化与IL-10呈负相关,故可推测,IL-10的释放增加后,CD8+ T细胞募集可减少,下调CXCR3的表达,炎症反应从而减弱。这也为进一步的实验提供了方向。
以上实验显示,CXCR3及IL-10分别是ALI重要的炎症介质及抗炎症介质,两者的表达呈负相关。重建CXCR3及IL-10的平衡可能会为ALI的治疗提供新的靶点。
| [1] | Johnson ER, Malthay MA. Acute lung injury:Epidemiology, pathogenesis, and treatment[J]. J Aerosol Med Pulm Drug Deliv, 2010, 23: 243-252. DOI: 10.1089/jamp.2009.0775. |
| [2] | Shanley TP, Vasi N, Deneberg A. Regulation of chemokine expression by IL-10 in lung inflammation[J]. Cytokine, 2000, 12: 1054-1064. DOI: 10.1006/cyto.1999.0655. |
| [3] | Kono H, Fujii H, Tsuchiya M, et al. Inhibition of the kupffer cells and neutralization of IL-10 increase the expression of chemokines in the lung in a rat peritonitis model[J]. J Surg Res, 2008, 150: 169-182. DOI: 10.1016/j.jss.2008.04.015. |
| [4] | Kopecky J, Kopecky O. NKcells, chemokines and chemokine receptors[J]. Klin Onkol, 2010, 23: 5-9. |
| [5] | Aksoy MO, Yang Y, Ji R, et al. CXCR3 surface expression in human airway epithelial cells:cell cycle dependence and effect on cell proliferation[J]. Am J Physiol Lung Cell Mol Physiol, 2006, 290: L909-L918. DOI: 10.1152/ajplung.00430.2005. |
| [6] | Hardaker EL, Bacon AM, Carlson K, et al. Regulation of TNF-α-and IFN-γ-induced CXCL10 expression: participation of the airway smooth muscle in the pulmonary inflammatory response in chronic obstructive pulmonary disease[J]. The FASEB Journal, 2004, 18: 191-193. |
| [7] | 聂莉, 李婷, 刘淑华, 等. 慢性阻塞性肺疾病患者外周血单个核细胞CXCR3的表达及与气流受限的关系[J]. 武汉大学学报:医学版, 2013, 34(2): 241-244. |
| [8] | Maeno T, Houghton AM, Quintero PA, et al. CD8+T cells are required for inflammation and destruction in cigarette smoke-induced emphysema in mice[J]. J Immunol, 2007, 178: 8090-8096. DOI: 10.4049/jimmunol.178.12.8090. |
| [9] | Nie L, Xiang RL, Liu Y, et al. Acute pulmonary inflammation is inhibited in CXCR3 knockout mice after short-term cigarette smoke exposure[J]. Acta Pharmacologica Sinica, 2008, 29: 1432-1439. DOI: 10.1111/j.1745-7254.2008.00899.x. |
| [10] | Nie L, Liu ZJ, Zhou WX, et al. CXCR3 is important for lung tissue damage and airway remodeling induced by short-term exposure to cigarette smoking in mice[J]. Acta Pharmacologica Sinica, 2010, 31: 436-442. DOI: 10.1038/aps.2009.192. |
 2016, Vol. 37
2016, Vol. 37
