癫痫所造成的认知功能损害,如记忆力、计算力、语言和思维能力下降等,使癫痫患者的智力、劳动力和生存质量都受到很大的影响,给患者本人、家庭和社会都造成了沉重的负担。因此,在控制癫痫发作的同时,如何改善癫痫患者的认知功能障碍,是目前临床医生尤为关注的热点问题之一。丁苯酞是我国原研的神经保护剂,已有研究表明其对认知功能损害有保护作用,本研究通过水迷宫和免疫组化等方法,观察丁苯酞对癫痫大鼠认知功能的影响和可能作用机制。
1 材料与方法 1.1 动物健康成年雄性SPF级SD大鼠40只(购自武汉大学医学院动物实验中心),体重200-220 g,在具有通风设备的动物房笼养,在实验前后过程中均给予充足的食物和水(12 h的明/暗周期,室温保持在22-24 ℃)。
1.2 分组及造模按照体重匹配,将大鼠随机分为4组,每组10只:对照组,致痫组,丁苯酞低剂量组(30 mg/kg),丁苯酞高剂量组(60 mg/kg)。隔日上午9:00,戊四氮(PTZ)按40 mg/kg腹腔注射(Sigma公司),浓度为1%,实验前用生理盐水配制。对照组每日上午9:00以等量的生理盐水腹腔注射。丁苯酞低剂量组(30 mg/kg)和丁苯酞高剂量组(60 mg/kg)大鼠分别于实验第12天始,分别将丁苯酞30 mg/kg和60 mg/kg (石药集团恩必普制药有限公司)于PTZ注射前予以腹腔注射。4组大鼠每次给药前皆称重,根据体重调整PTZ的给药量。所有模型经注射PTZ (20.00±1.58) d,全部点燃。此后,PTZ给药由隔天1次,改为隔3-4d一次,剂量不变,以维持点燃效应。模型成功与否以其发作时的行为变化为主要依据。
1.3 行为学观察模型成功按Racine[2]分级分为5级,凡获连续5次3级或3级以上惊厥发作的大鼠为完全点燃的大鼠癫痫模型并可入组观察。每日用药后观察大鼠行为1 h,按其惊厥发作程度记录。其中,1-2级记为轻度发作;3-4级为中度发作;5-6级为重度发作,并记录各组发作潜伏期及发作持续时间。
1.4 Morris水迷宫本实验采用Morris水迷宫进行学习记忆检测,参照Vorhees等[3]的方法进行。水迷宫为直径150 cm,高60 cm的圆形水池,水深32 cm,水温保持(19.5±0.5)℃。在池壁上等距离依次标记东(E)、南(S)、西(W)和北(N)4个方向,在NE象限正中离池壁30 cm处放一个直径为10 cm,高30 cm的圆形平台,平台低于水面2 cm。迷宫上方装有摄像头,图像经视频采集卡输入计算机,同步记录大鼠的运动轨迹。在连续5 d的训练中,每天训练4次,每次随机在NW、W、SW和E方向中选择一个作为入水点,观察并记录大鼠爬上平台所需的时间(潜伏期)。如果60 s内未找到平台,则将大鼠引导至平台并在平台上停留20 s,此时潜伏期记为60 s。训练期结束后(第6天)去除平台,选择SW作为入水点,观察并记录大鼠的游泳速度以及30 s内在NE象限的游泳时间,作为对原平台的记忆,每只大鼠检测1次。
1.5 灌注取材Morris水迷宫结束第2天,10%水合氯醛(350 mg/kg)腹腔注射麻醉大鼠后,快速暴露心脏,用生理盐水经左心室快速灌注约3-5 min,再灌注4%多聚甲醛(PBS溶解,pH=7.4)约250 ml。灌注后断头取脑,浸入4%多聚甲醛液中固定,24 h内石蜡包埋。根据Paxinos等[4]的大鼠脑立体定位图谱第5版,切取前囟-3.84 mm至前囟-5.04 mm的脑组织(包含完整的皮质和海马亚区)行切片制备,切片厚度为4.5 μm,用于免疫组化实验。
1.6 免疫组化染色免疫组化染色采用SABC法。切片常规脱蜡至水洗;0.01 mol/L Tris-EDTA缓冲液微波修复后,3%H2O2室温孵育10 min;滴加5% BSA (牛血清白蛋白)37 ℃封闭20 min;滴加兔多克隆抗体NR1(1:500;ab17345,Abcam公司,美国)和NR2B (1:500;ab65875,Abcam公司,美国)约50 μl覆盖到组织,4 ℃过夜;50-100 μl A液室温下孵育45 min;50-100 μl新鲜配制的DAB溶液,显微镜控制显色。空白对照实验:除用PBS代替一抗外,其余步骤均相同,结果为阴性。免疫组化染色阳性反应为细胞膜呈黄棕色。Image-Pro Plus 6.0图像分析软件测量目标区域阳性细胞的积分光密度值,分析NR1和NR2B的表达。
1.7 统计学方法所有数据均采用GraphPad Prism 5.0进行统计分析。Morris水迷宫潜伏期采用两因素方差分析,进一步分析采用Bonferroni post-test检验;其他数据采用单因素方差分析,进一步分析采用Dunnett’s post-test检验。以P<0.05认为差异有统计学意义。
2 结果 2.1 行为学观察致痫组大鼠在实验第(19.5±1.48)天开始出现癫痫发作;丁苯酞低剂量组(30 mg/kg)在第20天开始有癫痫发作出现,发作程度也逐渐加重,最高发作级别为4级;丁苯酞高剂量组(60 mg/kg)在第20天开始出现癫痫发作,最高级别为3级。根据Racine[2]分级标准可以认为上述实验动物均达到点燃标准,癫痫模型制作成功。由表 1可知对照组实验中无发作;而致痫组发作明显多于丁苯酞干预组;致痫组发作潜伏期明显短于丁苯酞低剂量和高剂量干预组,差异有统计学意义(P<0.01);丁苯酞低剂量和高剂量干预组发作持续时间明显短于致痫组,差异也有统计学意义(P<0.05;P<0.01)。
| 表 1 实验动物痫样发作程度、潜伏期和持续时间比较 |
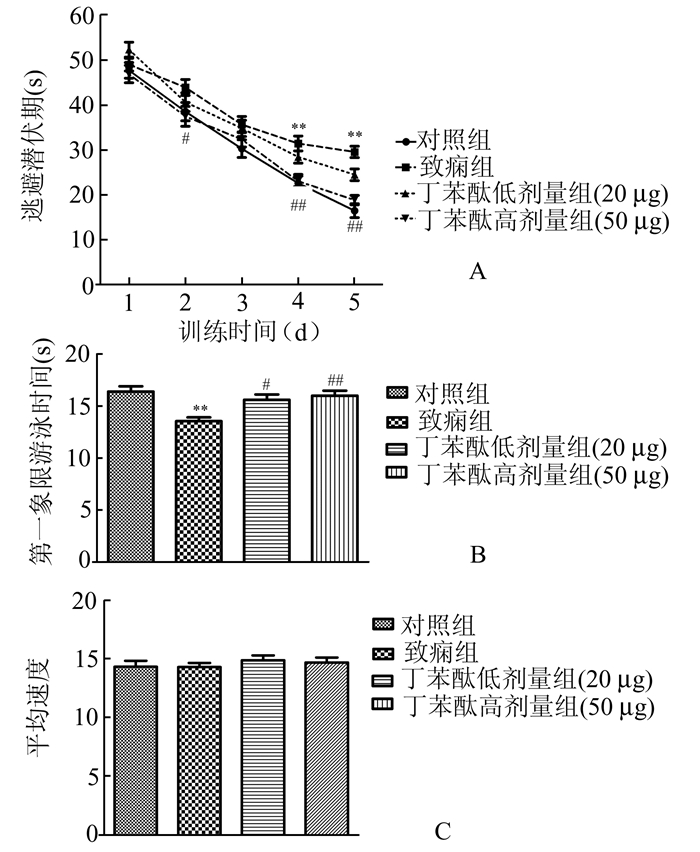
训练期每天记录的大鼠在4个象限的平均潜伏期反映了大鼠的学习能力。ANOVA分析提示组间(P<0.05)和组内(P<0.01) Morris水迷宫的平均潜伏期有明显差异(如图 1A所示)。Bonferroni posttest检验结果表明,致痫组大鼠在训练的第4天和第5天找到平台的时间显著多于对照组大鼠,差异有显著性意义(均P<0.01);而与致痫组大鼠相比,丁苯酞高剂量组在训练期的第2天,第4天和第5天找到平台的时间明显减少,差异有显著性意义(P<0.05;P<0.01)。这些研究结果说明致痫组大鼠在Morris水迷宫中的空间学习能力出现了损害;而高剂量丁苯酞可以减少致痫组大鼠的空间学习时间。
|
图 1 Morris水迷宫试验结果 A:逃逸潜伏期;B:第一象限游泳时间;C:平均游泳速度。数据均以x±s表示,n=10。与对照组比较,**P<0.01;与致痫组比较,#P<0.05,##P<0.01 |
第6天大鼠在第一象限的游泳时间反映了大鼠的记忆能力。ANOVA分析提示丁苯酞干预对大鼠的记忆能力有明显影响(F3, 44=7.2,P<0.01)。Tukey's post-test检验提示,致痫组大鼠的记忆能力明显低于对照组(P<0.01);而丁苯酞低剂量和高剂量干预组大鼠的记忆能力都明显高于致痫组(P<0.05;P<0.01)(图 1B)。这些研究结果说明致痫组大鼠在Morris水迷宫中的记忆能力出现了损害;而低剂量和高剂量丁苯酞干预都可以改善致痫组大鼠的空间学习能力。
此外,我们统计了大鼠在第6天空间探索试验中的游泳速度,结果显示各组大鼠之间的游泳速度没有差异(P=0.72;图 1C),说明大鼠的游泳能力没有影响逃逸潜伏期的结果。
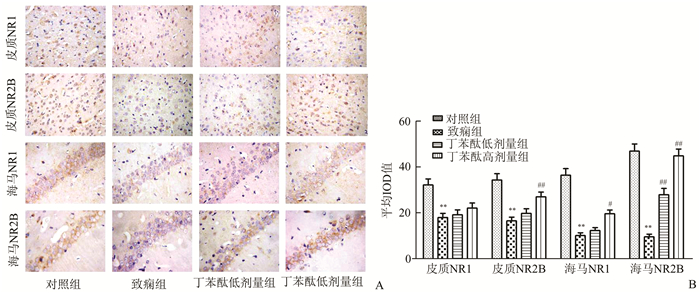
2.3 免疫组织化学染色免疫组化检测大鼠皮质和海马NR1和NR2B的蛋白免疫活性如图 2所示,ANOVA分析显示,丁苯酞干预后各组大鼠皮质NR1和NR2B,以及海马NR1和NR2B的蛋白免疫活性有明显变化(均为P<0.01)。Dunnett’s post-test检验显示,与对照组比较,致痫组大鼠皮质和海马NR1和NR2B的积分光密度值均明显降低(P<0.01);而与致痫组大鼠比较,丁苯酞低剂量干预组大鼠海马NR2B的积分光密度值明显升高(P<0.01);丁苯酞高剂量干预组大鼠皮质NR2B,海马NR1和NR2B的积分光密度值均明显升高(P<0.05,P<0.01)。
|
图 2 丁苯酞干预后各组大鼠皮质和海马NR1和NR2B的免疫组化结果 A:代表性的免疫组化染色结果(×400);B:平均积分光密度值。数据均以x±s表示,n=6。与对照组比较,**P<0.01;与致痫组比较,#P<0.05,##P<0.01 |
目前国内外对癫痫发作导致认知功能障碍的机制还不十分清楚。临床研究发现,单次癫痫发作并不引起认知功能障碍,动物实验研究结果也显示,反复短暂的缺血比一次较长时间缺血再灌注更容易导致认知功能障碍[5],这也与临床上认知功能障碍一般发生在反复癫痫发作之后相符合。神经元功能损害是学习记忆障碍的基础,大脑在反复缺血和缺氧后,海马和皮层神经元会出现严重损伤。Morris水迷宫试验能较准确地反映动物的空间学习和记忆能力,是实验室应用较多的一种检测认知功能的方法。有研究表明,反复痫性发作大鼠Morris水迷宫实验和八臂迷宫实验中的空间记忆能力明显受损,组织学观察也发现海马CA1区、CA3区和DG区神经元脱失以及CA3区苔藓纤维发芽[6, 7]。徐玉振等以Morris水迷宫实验证明,丁苯酞能改善血管性痴呆模型大鼠的学习记忆能力并对海马神经元具有保护作用[8],另外丁苯酞可以通过减轻海马神经元的损伤而对脑缺血后的学习和记忆功能有改善作用[9]。但是丁苯酞对于癫痫大鼠学习和记忆能力影响的报道较少。本实验研究结果显示,虽然丁苯酞不能阻止癫痫发作,但能延长癫痫发作的潜伏期,且丁苯酞干预组的发作次数明显少于致痫组;同时丁苯酞低剂量和高剂量干预组癫痫发作的持续时间也明显短于致痫组,差异有统计学意义,这说明丁苯酞可能因其神经元保护作用延缓和减轻了癫痫发作的频率和程度。在本研究的Morris水迷宫试验中,反复痫性发作大鼠的空间学习和记忆能力出现了损害,而丁苯酞干预组癫痫大鼠的空间学习和记忆能力明显好于致痫组,说明丁苯酞可以改善癫痫大鼠的认知功能损害。
已有的研究表明,癫痫发作引起的认知功能损害是多因素作用的结果,包括海马结构损伤,胆碱酯酶受体的变化以及谷氨酸N-甲基-D-天门冬氨酸(N-methyl-D-asparate,NMDA)受体激活等。NMDA受体是广泛分布于中枢神经系统的谷氨酸敏感离子通道受体,在大脑皮层和海马中广泛分布,是中枢神经系统的学习和记忆的基础[10]。目前已经发现的NMDA受体有七种亚基,主要包括NR1和NR2两大类;其中NR2B亚单位主要分布于海马CA1区,在学习和记忆中起关键作用[11]。有研究发现,NR2B基因敲除的小鼠出现记忆能力下降[12],而转染NR2B基因的大鼠记忆能力明显增高[11]。癫痫发作后,NMDA受体参与了癫痫发作的病理损伤过程,NR2B亚单位可以阻止神经元痫样放电在脑内的播散[13]。近来有报道提示丁苯酞能影响NR2B受体在大鼠海马的表达[14],本研究亦发现癫痫大鼠皮质和海马NR1和NR2B的表达都明显降低,而与致痫组相比,丁苯酞的干预可以增加皮质NR2B,海马NR1和NR2B的表达;说明NMDA亚单位参与了癫痫发作导致的认知功能损害,而丁苯酞可能通过改善皮质和海马NMDA亚单位的表达来改善癫痫大鼠的认知功能。
此外,有研究证明,无论是癫痫动物模型还是癫痫患者的脑内均存在着活跃的自由基反应,癫痫发作时自由基进一步明显增加,远远超过机体对自由基的清除能力,导致神经元和线粒体的损伤。而丁苯酞有改善全脑缺血后的能量代谢、保护线粒体功能、减轻神经功能损伤的程度等作用。这些机制是否参与丁苯酞对癫痫大鼠认知功能的改善,还有待进一步研究。
| [1] | Ure JA, Perassolo M. Update on the pathophysiology of the epilepsies[J]. J Neurol Sci, 2000, 177(1): 1-17. DOI: 10.1016/S0022-510X(00)00356-7. |
| [2] | Racine RJ. Modification of seizure activity by electrical stimulation. Ⅱ. Motor seizure[J]. Electroencephalogr Clin Neurophysiol, 1972, 32(3): 281-294. DOI: 10.1016/0013-4694(72)90177-0. |
| [3] | Vorhees CV, Williams MT. Morris water maze: procedures for assessing spatial and related forms of learning and memory[J]. Nat Protoc, 2006, 1(2): 848-858. DOI: 10.1038/nprot.2006.116. |
| [4] | Paxinos G. The Rat Brain in Stereotaxic Coordinates [M]. 5th ed San Diego:Academic Press, 2005:50-52, 105-115. |
| [5] | 李巍, 张世仪, 赵惠敏, 等. 小鼠脑缺血性学习记忆障碍模型的建立[J]. 基础医学与临床, 1995, 15(6): 46-49. |
| [6] | de Rogalski Landrot I, Minokoshi M, Silveira DC, et al. Recurrent neonatal seizures: relationship of pathology to the electroencephalogram and cognition[J]. Brain Res Dev Brain Res, 2001, 129(1): 27-38. DOI: 10.1016/S0165-3806(01)00177-8. |
| [7] | Kotloski R, Lynch M, Lauersdorf S, et al. Repeated brief seizures induce progressive hippocampal neuron loss and memory deficits[J]. Prog Brain Res, 2002, 135: 95-110. DOI: 10.1016/S0079-6123(02)35010-6. |
| [8] | 徐玉振, 秦丽晨, 刘运林. 消旋-3-正丁基苯酞对血管性痴呆大鼠学习记忆能力的影响[J]. 中华行为医学与脑科学杂志, 2011, 20(4): 309-311. |
| [9] | Xu J, Wang Y, Li N, et al. L-3-n-butylphthalide improves cognitive deficits in rats with chronic cerebral ischemia[J]. Neuropharmacology, 2012, 62(7): 2424-2429. DOI: 10.1016/j.neuropharm.2012.02.014. |
| [10] | Stramiello M, Wagner JJ. D1/5 receptor-mediated enhancement of LTP requires PKA, Src family kinases, and NR2B-containing NMDARs[J]. Neuropharmacology, 2008, 55(5): 871-877. DOI: 10.1016/j.neuropharm.2008.06.053. |
| [11] | Tang YP, Shimizu E, Dube GR, et al. Genetic enhancement of learning and memory in mice[J]. Nature, 1999, 401(6748): 63-69. DOI: 10.1038/43432. |
| [12] | Clayton DA, Mesches MH, Alvarez E, et al. A hippocampal NR2B deficit can mimic age-related changes in long-term potentiation and spatial learning in the Fischer 344 rat[J]. J Neurosci, 2002, 22(9): 3628-3637. |
| [13] | Berretta N, Ledonne A, Mango D, et al. Hippocampus versus entorhinal cortex decoupling by an NR2 subunit-specific block of NMDA receptors in a rat in vitro model of temporal lobe epilepsy[J]. Epilepsia, 2012, 53(5): e80-e84. DOI: 10.1111/epi.2012.53.issue-5. |
| [14] | 杜爱林, 李爽, 美洪波, 等. 丁苯酞对酒精依赖大鼠海马谷氨酸含量及NR2B表达的影响[J]. 中国应用生理学杂志, 2012, 28(1): 18-19, 27. |
 2016, Vol. 37
2016, Vol. 37

 ,
,