2. 新疆医科大学第一附属医院呼吸科 新疆 乌鲁木齐 832000
2. Dept. of Respiration, the First Affiliated Hospital of Xinjiang Medical University, Urumqi 832000, China
研究表明,70%以上的非小细胞肺癌(non-small cell lung cancer,NSCLC)患者初次确诊时即已为中晚期(Ⅲb-Ⅳ期),已经失去手术治疗的最佳时机[1]。晚期NSCLC患者1年生存率约为40%,5年生存率仅为2%[2],严重影响了患者的生命安全。化疗是治疗晚期NSCLC的首选方案。Ⅱ期及Ⅲ期临床试验表明,以紫杉醇、吉西他滨及多西他赛等化疗药物为主的为常规化疗方案可取得一定的疗效,但配合含铂类制剂的联合治疗方案可增加常规化疗的效果,可改善患者的症状、提高患者的生活质量[3]。本文对比分析紫杉醇、吉西他滨及多西他赛三种一线化疗药物联合奈达铂对晚期NSCLC的临床治疗效果,旨在为晚期NSCLC患者的临床治疗提供参考。
1 资料与方法 1.1 临床资料搜集2010年1月-2014年3月收治的晚期NSCLC患者64例的临床资料,均组织病理学和(或)细胞学检查确诊为晚期NSCLC。病例纳入标准[4, 5]:①均为初次确诊并接受治疗者,无化疗药物禁忌症,可接受紫杉醇、吉西他滨、多西他赛的化疗;②无严重心血管疾病,肝、肾功能未见异常;③拒绝接受手术治疗或不能接受手术治疗;④Karnofsky功能状态评分(KPS评分)>80分,预计生存期>3个月。病例排除标准[4, 5]:合并心血管、肾脏、造血系统、免疫系统等原发性疾病和精神病患者。随机将64例患者分为紫杉醇组22例、吉西他滨组21例及多西他赛组21例,3组患者一般资料(性别、年龄、吸烟史、肿瘤病理类型及TNM分期等)经比较,差异无统计学意义(P>0.05),具有可比性。3组患者一般资料见表 1。所有患者均知情同意。本研究获得医院伦理委员会批准执行。
| 表 1 组患者一般资料比较(n, x±s) |
①紫杉醇组:采用紫杉醇注射液(扬子江药业集团有限公司,百时美施贵宝,规格:5 ml:30 mg; )联合注射用奈达铂(山东齐鲁制药有限公司生产,规格:10 mg),其中,紫杉醇给药剂量为135 mg/m2(体表面积),第1 d;奈达铂给药剂量为80 mg/m2,第1天;均加入500 ml氯化钠注射液充分溶解后静脉滴注。②吉西他滨组:采用注射用盐酸吉西他滨(江苏豪森药业股份有限公司,规格:1 000 mg,200 mg)联合奈达铂治疗,其中,吉西他滨按照1 000 mg/m2的剂量给药,第1、8天,每周一次,连续3周,休息1周;奈达铂同紫杉醇组。③多西他赛组:采用多西他赛注射液(江苏恒瑞医药有限公司生产,规格:3 ml:60 mg;安万特医药公司:20 mg;山东齐鲁制药有限公司,规格:0.5 ml; 20 mg;1 ml; 40 mg)联合奈达铂治疗,多西他赛给药剂量为75 mg/m2,第1天,每3周1次;奈达铂同紫杉醇组。以上化疗21 d为一周期,至少化疗2周期。所有患者联合化疗期间常规给予镇吐药物对症治疗,并定期监测血常规及肝肾功能。
1.3 疗效判定化疗2周期后进行以下疗效判定:①治疗有效率及临床受益率比较:根据实体肿瘤化疗疗效评价标准(RECIST),分为:完全缓解(CR)、部分缓解(PR)、稳定(SD)及进展(PD);治疗总有效率为CR+PR之和;临床获益率为CR+PR+SD之和。②生活质量改善情况比较:以KPS评分统计3组患者治疗后生活质量改善率(为显著改善+改善之和)。其中,治疗后KPS评分增加大于20分计为显著改善,增加大于10分计为改善,减少小于10分计为稳定,减少大于10分计为下降。③不良反应评价:根据WHO有关抗癌药物不良反应统计3组治疗期间的不良反应。④随访:随访至2014年6月,统计3组患者中位无进展生存期(PFS)。
1.4 统计学方法SPSS 17.0统计学软件作数据处理。率的比较,采用χ2检验;生存期分析采用Kaplan-Meier法。以P < 0.05为差异具有统计学意义。
2 结果 2.1 治疗有效率及临床受益率比较见表 2。紫杉醇组临床受益率高于吉西他滨组及多西他赛组,差异有统计学意义(P<0.05);3组治疗有效率比较差异无统计学意义(P>0.05)。
| 表 2 近期疗效评价比较[n(%)] |
见表 3。紫杉醇组生活质量改善率优于吉西他滨组及多西他赛组,差异有统计学意义(P<0.05)。
| 表 3 生活质量改善情况[n(%)] |
见表 4。3组不良反应中,紫杉醇组神经毒性大于其他二组,差异有统计学意义(P<0.05);其他不良反应发生率组间比较差异无统计学意义(P>0.05)。
| 表 4 不良反应比较[n(%)] |
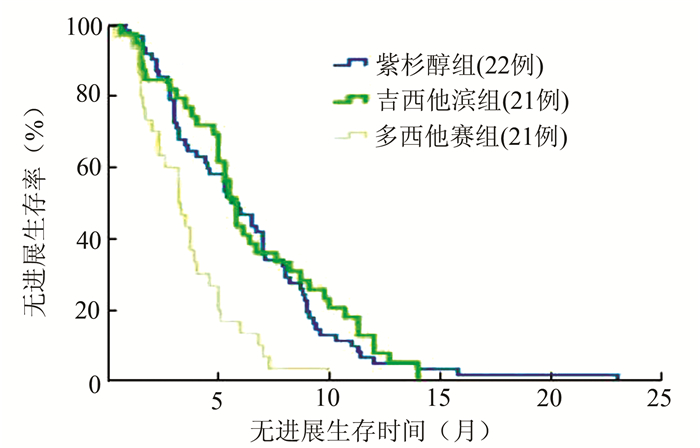
随访至2014年6月,均获随访,紫杉醇组、吉西他滨组及多西他赛组的PFS分别为5.65、4.55及3.50个月(P<0.05)。3组生存曲线见图 1。
|
图 1 3组患者出生存曲线 |
晚期NSCLC的治疗一直是学者们研究的热点,由最初的最佳支持治疗发展到后来的以顺铂为基础的化疗,再发展至目前的铂类联合第三代化疗药物双药联合治疗方案,晚期NSCLC的治疗效果有了一定程度的提高[6]。第三代化疗药物中,紫杉醇、吉西他滨及多西他赛的临床应用最为广泛,为一线化疗药物,多个临床实践均已证实它们对NSCLC的疗效。随着研究的不断进展,学者[7, 8]们认为第三代化疗药物联合铂类制剂对晚期NSCLC进行化疗可取得更好的效果。赵玲娣[9]等学者探讨了不同三代新药联合铂类制剂对晚期NSCLC的化疗效果,其研究表明长春瑞滨、紫杉醇等联合卡铂或顺铂化疗可延长患者的PFS,与单药化疗比较差异有统计学意义(P<0.05),表明一线化疗药物联合铂类制剂可取得更好化疗效果。
本组资料中,经比较紫杉醇、吉西他滨及多西他赛3种药物联合奈达铂的治疗效果发现,3组患者的治疗有效率比较差异无统计学意义(P>0.05),但紫杉醇组可更好的改善患者的临床受益率(CR+PR+SD),与其他两组比较差异有统计学意义(P<0.05),表明了紫杉醇联合奈达铂治疗方案可更好的控制晚期NSCLC患者疾病的进展。本文随访结果也证实了此结论。本组资料所有患者均获随访,其中,紫杉醇组随访PFS高于其他两组(P<0.05),也提示了其对患者病情的控制作用更好。
奈达铂为新一代铂类化合物,与卡铂、顺铂类似,可发挥抑制肿瘤细胞增殖的作用,但与卡铂及顺铂无交叉耐药性,临床使用安全、方便[10]。基于上述考虑,本文选用奈达铂与紫杉醇、吉西他滨及多西他赛进行配伍。研究表明,紫杉醇组生活质量改善率优于吉西他滨组及多西他赛组(P<0.05),与紫杉醇组对疾病进展的控制效果有关。同时,本组资料研究还发现,不良反应中,紫杉醇组神经毒性大于其他二组,差异有统计学意义(P<0.05),与文献[11]报道基本一致。导致出现此种现象的主要原因与紫杉醇的作用机制有关,一方面紫杉醇的微管蛋白凝聚可对微管形成造成干扰,进而影响神经轴突内的电信号输送,最终造成外周神经病变。而吉西他滨及多西他赛虽同为抗微管类化疗药物,但其二者的神经毒性较低,且患者可自行恢复。另一方面,紫杉醇具有较高的生物利用度,更高的细胞内浓度,也是导致神经毒性反应的原因之一[10, 11]。
综上所述,紫杉醇、吉西他滨及多西他赛联合奈达铂对晚期NSCLC的化疗效果相近,但紫杉醇组可更好的改善患者的生活质量、控制疾病进展,值得临床深入研究。
| [1] |
吴国明, 范晔. 晚期非小细胞肺癌靶向治疗研究进展及思考[J].
西部医学, 2012, 24 (1): 1-4, 8.
Wu GM, Fan Y. Research progress and new thoughts on non-small cell lung cancer of late stage[J]. Medical Journal of West China, 2012, 24(1): 1-4, 8. |
| [2] |
迟德财. 老年晚期非小细胞肺癌化疗进展[J].
实用肿瘤学杂志, 2012, 26 (1): 86-91.
Chi DC. Progress in chemotherapy for elderly advanced non-small cell lung cancer[J]. Practical Oncology Journal, 2012, 26(1): 86-91. |
| [3] | Yin Z, Zhang Y, Li Y, et al. Prognostic significance of STAT3 expression and its correlation with chemoresistance of non-small cell lung cancer cells[J]. Acta Histochemica, 2012, 114(2): 151-158. DOI: 10.1016/j.acthis.2011.04.002. |
| [4] | Esterbrook G, Anathhanam S, Plant PK, et al. Adequacy of endobronchial ultrasound transbronchial needle aspiration samples in the subtyping of non-small cell lung cancer[J]. Lung cancer, 2013, 80(1): 30-34. DOI: 10.1016/j.lungcan.2012.12.017. |
| [5] | Fu HY, Li C, Yang W, et al. FOXP3 and TLR4 protein expression are correlated in non-small cell lung cancer: Implications for tumor progression and escape[J]. Acta Histochemica, 2013, 115(2): 151-157. DOI: 10.1016/j.acthis.2012.06.002. |
| [6] | Kosmidis PA, Fountzilas G, Eleftheraki AG, et al. Paclitaxel and gemcitabine versus paclitaxel and vinorelbine in patients with advanced non-small-cell lung cancer. A phase III study of the Hellenic Cooperative Oncology Group (HeCOG)[J]. Annals of oncology, 2011, 22(4): 827-834. DOI: 10.1093/annonc/mdq445. |
| [7] | Ansari RH, Socinski MA, Edelman MJ, et al. A retrospective analysis of outcomes by age in a three-arm phase III trial of gemcitabine in combination with carboplatin or paclitaxel vs. paclitaxel plus carboplatin for advanced non-small cell lung cancer[J]. Critical reviews in oncology/hematology, 2011, 78(2): 162-171. DOI: 10.1016/j.critrevonc.2010.03.003. |
| [8] | Liu Y, Wu X, Sun Y, et al. Silencing of X-linked inhibitor of apoptosis decreases resistance to cisplatin and paclitaxel but not gemcitabine in non-small cell lung cancer[J]. The Journal of International Medical Research, 2011, 39(5): 1682-1692. DOI: 10.1177/147323001103900510. |
| [9] |
赵玲娣, 张湘茹, 李峻岭, 等. 不同三代新药与铂联合一线双药方案对晚期非小细胞肺癌的疗效分析[J].
中华医学杂志, 2012, 92 (22): 1527-1531.
Zhao LD, Zhang XR, Li JL, et al. Efficacy analysis of third-generation plus platinum doublets in the first-line chemotherapy of advanced non-small cell lung cancer[J]. National Medical Journal of China, 2012, 92(22): 1527-1531. |
| [10] |
黄志荣, 曹齐生, 杜成荣, 等. 吉西他滨联合紫杉醇治疗晚期非小细胞肺癌的临床研究[J].
实用临床医药杂志, 2012, 16 (21): 70-72.
Huang ZR, Cao QS, Du CR, et al. Clinical study of gemcitabine plus paclitaxel in the treatment of advanced non-small cell lung cancer[J]. Journal of Clinical Medicine in Practice, 2012, 16(21): 70-72. |
| [11] |
罗虎, 杨静翔, 宫亮, 等. 紫杉醇脂质体联合顺铂对比吉西他滨联合顺铂一线治疗伴有区域淋巴结转移的晚期非小细胞肺癌的临床研究[J].
中国癌症杂志, 2013, 12 (12): 995-1000.
Luo H, Yang JX, Gong L, et al. Liposomal paclitaxel in combination with cisplatin as a first line of chemotherapy in treatment of advanced NSCLC with regional lymph node metastasis:A randomized controlled trial[J]. China Oncology, 2013, 12(12): 995-1000. |
 2016, Vol. 37
2016, Vol. 37
