2. 武汉科技大学信息科学与工程学院 湖北 武汉 430065;
3. 华中科技大学同济医学院附属同济医院心内科 湖北 武汉 430030
2. School of Information Science and Engineering, Wuhan University of Science and Technology, Wuhan 430065, China;
3. Dept. of Cardiology, Tongji Hospital, Tongji Medical College of Huazhong University of Science and Technology, Wuhan 430030, China
花生四烯酸(AA)是人体内最丰富的物质之一,可通过环氧化酶,脂质氧化酶和细胞色素P450表氧化酶三条途径代谢。其中AA经细胞色素P450表氧化酶途径代谢生成4种不同的环氧二十碳三烯酸(epoxyeicosatrienoic acids,EETs),即5, 6-EET, 8, 9-EET, 11, 12-EET和14, 15-EET[1]。许多研究表明EETs在心血管系统的稳态中发挥重要作用,首先EETs具有强大的舒张血管的功能,其机制是通过激活平滑肌细胞中钙离子敏感的钾通道引起血管平滑肌细胞超级化进而导致血管舒张。EETs可通过激活丝裂原活化的蛋白激酶(nitrogen-activated protein kinase,MAPK)及磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase, PI3K)/蛋白激酶B (protein kinase B,PKB/AKT)信号通路促进内皮细胞增殖与新生血管形成[2]。通过CYP表氧化酶过表达增加内源性EETs的合成,可显著抑制TNF-α诱导的内皮细胞凋亡,其机制也被证明可能与抑制MAPK的去磷酸化,以及激活PI3K/AKT信号通路密切相关[3]。体外实验证明,饱和脂肪酸棕榈酸盐(Palmitate)可诱导包括心肌细胞在内的多种不同种类的细胞凋亡[4]。饱和脂肪酸在心肌细胞中蓄积,并诱导心肌细胞凋亡的作用,即所谓的“脂毒性”可使心脏功能失调,严重时可导致心力衰竭[5, 6]。本研究对体外培养的大鼠心肌细胞H9c2,在给予Palmitate处理的同时予以14,15-EET干预,观察14,15-EET对Palmitate诱导的H9c2心肌细胞凋亡的影响及其机制。
1 材料与方法 1.1 细胞培养与分组H9c2细胞(购自武汉大学细胞典型培养物保藏中心)培养于含10%胎牛血清、抗生素(50 μ/ml青霉素+50 μg/ml链霉素)的DMEM培养液中,放置在37 ℃、5%CO2、饱和湿度的培养箱中静置孵育。0.25% EDTA-胰酶消化、1:3传代培养。待细胞融合达70%-80%时,改用无血清培养基培养24 h使其同步化。取对数生长期H9c2细胞随机分为4组:①正常组,②溶媒组(使用与③组同体积的乙醇干预细胞),③ Palmitate组(Palmitate粉剂购自上海阿拉丁生化科技股份公司,使用乙醇溶解后稀释成不同浓度),④ Palmitate+14,15-EET组;4组均培养24 h后进行各项指标测定。
1.2 MTT细胞活力检测按上述分组加入处理因素培养24 h,培养结束前4 h,培养板所有孔中加入20 μl浓度为5 mg/ml的新鲜配制的MTT溶液,继续培养4 h,使MTT还原为甲瓒。小心地吸除上清液,每孔加DMSO (二甲基亚砜)150 μl,用摇床摇匀。使用酶标仪测定570 nm光吸收值(OD值)。
1.3 流式细胞仪测细胞凋亡按上述分组加入处理因素培养24 h,取1 ml胰酶消化细胞,1 500 r/min离心5 min,弃上清。加入3 ml 4 ℃预冷的PBS完全重悬细胞,1 500 r/min离心5 min,弃上清。沉淀用300 μl的Binding Buffer重悬,加入5 μl Annexin V-FITC和5 μl Propidium Iodide混匀,室温下避光反应5-15 min。流式细胞仪检测细胞凋亡率。
1.4 Western blot检测Bax和Bcl-2表达按上述分组加入处理因素培养24 h后,吸出培养基,预冷的磷酸盐缓冲液(PBS)冲洗后加入细胞裂解液,充分晃动使试剂与细胞充分接触后用细胞刮刀将细胞及试剂刮下,收集到1.5 ml离心管中。冰浴30 min期间反复吹打保证细胞完全裂解。12 000 g离心5 min,收集上清至新离心管。BCA法测蛋白浓度。SDS聚丙烯酰胺凝胶(分离胶8%,浓缩胶5%)垂直电泳分离,电转至PVDF膜上(4 ℃转膜过夜),转好的膜室温下用含5%的脱脂牛奶(0.5%TBST配),封闭1 h。加入一抗(1:500稀释)4 ℃孵育过夜,用TBST在室温下摇床上洗膜3次,每次5 min。加入二抗(1:3 000稀释),室温下孵育30 min后,用TBST在室温下摇床上洗3次,每次5 min。增强的化学发光试剂显色曝光。
1.5 统计学处理所有检测值均以均数±标准差(x±s)表示,应用SPSS 16.0软件进行统计处理,两样本均数比较采用t检验,多组间数据比较采用单因素方差分析,组间两两比较q检验,当P < 0.05为差异有统计学意义。
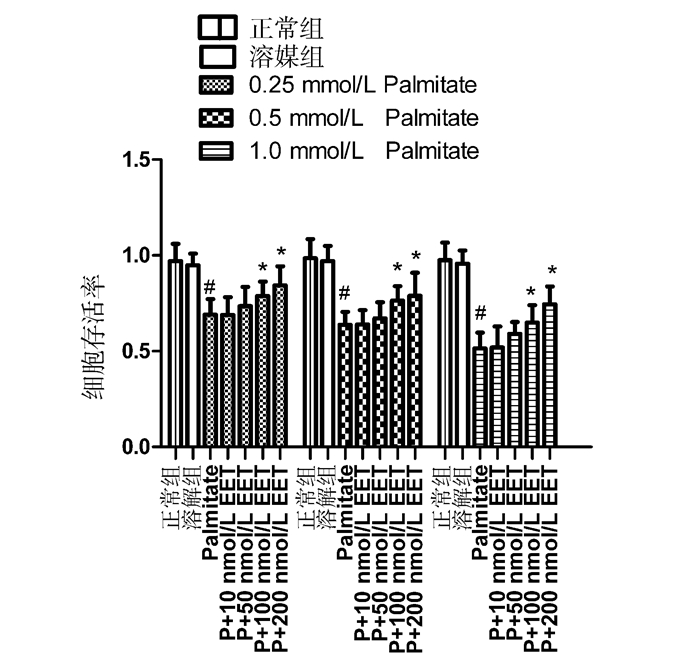
2 结果 2.1 14,15-EET对Palmitate诱导的H9c2细胞存活率的影响使用不同终浓度(0.25,0.5,1.0 mmol/L)的Palmitate分别作用于H9c2细胞,24 h后行MTT检测细胞存活率。结果如表 1所示,与正常组(Control)相比,溶媒组(Vehicle) H9c2细胞存活率无明显改变,Palmitate呈剂量依赖性显著降低H9c2细胞存活率(P < 0.05)。为了明确14,15-EET对Palmitate诱导的H9c2细胞存活率的影响,将不同终浓度的14,15-EET (10,50,100,200 nmol/L)分别与不同浓度(0.25,0.5,1.0 mmol/L)的Palmitate共同作用于H9c2心肌细胞24 h。结果如图 1所示,50 nmol/L的14,15-EET (50 nmol/L EET)作用即可提高Palmitate诱导后H9c2细胞的存活率,100 nmol/L的14,15-EET (100 nmol/L EET)可显著提高H9c2细胞的存活率(P < 0.05),随着14,15-EET浓度的增加,提高H9c2细胞存活率的作用逐渐增强。提示14,15-EET呈浓度依赖性改善不同浓度Palmitate刺激后H9c2细胞存活率。
| 表 1 MTT吸光度值计算Palmitate诱导后各组H9c2细胞存活率(n=4,x±s) |
|
图 1 各组H9c2细胞MTT吸光度值计算细胞存活率(n=4,x±s) 与正常组比较,#P < 0.05;与Palmitate组比较,*P < 0.05 |
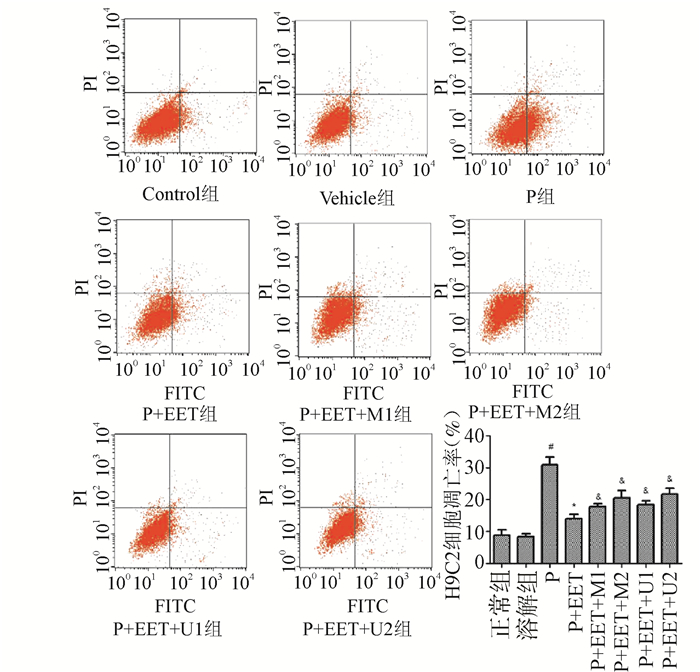
应用0.25 mmol/L的Palmitate诱导H9c2细胞发生凋亡,同时加用终浓度为200 nmol/L 14,15-EET刺激H9c2细胞24 h,收集细胞流式细胞仪检测凋亡。正常组和溶媒组H9c2细胞凋亡的比例分别为(8.84±1.6)%和(8.36±0.9)%,0.25 mmol/L Palmitate组(P组)为(30.88±2.5)%,0.25 mmol/L Palmitate+200 nmol/L 14,15-EET组(P+EET组)为(14.00±1.42)%。结果如图 2所示,与正常组相比较,溶媒组H9c2细胞凋亡比例无明显改变,提示溶媒对H9c2细胞凋亡无显著影响;与正常组相比较,Palmitate组凋亡细胞比例显著增加(P < 0.05),提示Palmitate可成功诱导H9c2细胞凋亡;14,15-EET处理后凋亡细胞的比例显著减少(P < 0.05),提示14,15-EET对Palmitate诱导的H9c2细胞凋亡有保护作用。
|
图 2 各组H9c2细胞流式细胞仪测凋亡 与正常组比较,#P < 0.05;与P组比较,*P < 0.05;与P+EET比较,&P < 0.05 |
应用0.25 mmol/L的Palmitate诱导H9c2细胞发生凋亡,同时加用终浓度为200 nmol/L的14, 15-EET刺激,合用终浓度为50,100 nmol/L的AKT抑制剂MK2206,共同孵育24 h后,收集细胞应用流式细胞仪检测H9c2细胞的凋亡情况。0.25 mmol/L Palmitate+14,15-EET+50 nmol/L MK2206组(P+EET+M1),0.25 mmol/L Palmitate+14,15-EET+100 nmol/L MK2206组(P+EET+M2)凋亡细胞比例分别为(17.83±0.95)%和(20.52±2.3)%,结果如图 2所示,与0.25 mmol/L Palmitate+14,15-EET组相比较,0.25 mmol/L Palmitate+14,15-EET+MK2206组H9c2细胞中凋亡细胞比例显著增加(P < 0.05),提示AKT抑制剂显著抑制了14,15-EET抑制Palmitate诱导的H9c2细胞的凋亡作用。这些数据说明,14,15-EET经AKT信号传导通路抑制Palmitate诱导的H9c2细胞的凋亡。
2.4 ERK1/2抑制剂对14, 15-EET抑制Palmitate诱导的H9c2细胞凋亡的影响应用0.25 mmol/L的Palmitate诱导H9c2细胞发生凋亡,同时加用终浓度为200 nmol/L的14, 15-EET刺激,合用终浓度为5,10 μmol/L的ERK1/2抑制剂U0126,共同孵育24 h后,收集细胞应用流式细胞仪检测H9c2细胞的凋亡情况。0.25 mmol/L Palmitate+14,15-EET+5 μmol/L U0126组(P+EET+U1),0.25 mmol/L Palmitate+14,15-EET+10 μmol/L U0126(P+EET+U2)的凋亡细胞比例分别为(18.38±1.32)%和(21.8±1.75)%。结果如图 2所示,与0.25 mmol/L Palmitate+14,15-EET组相比较,0.25 mmol/L Palmitate+14,15-EET+U0126组凋亡细胞比例显著增加(P < 0.05),提示ERK1/2抑制剂显著抑制了14,15-EET抑制Palmitate诱导的H9c2细胞凋亡的作用。这些数据说明,14,15-EET经ERK1/2信号传导通路抑制Palmitate诱导的H9c2细胞的凋亡。
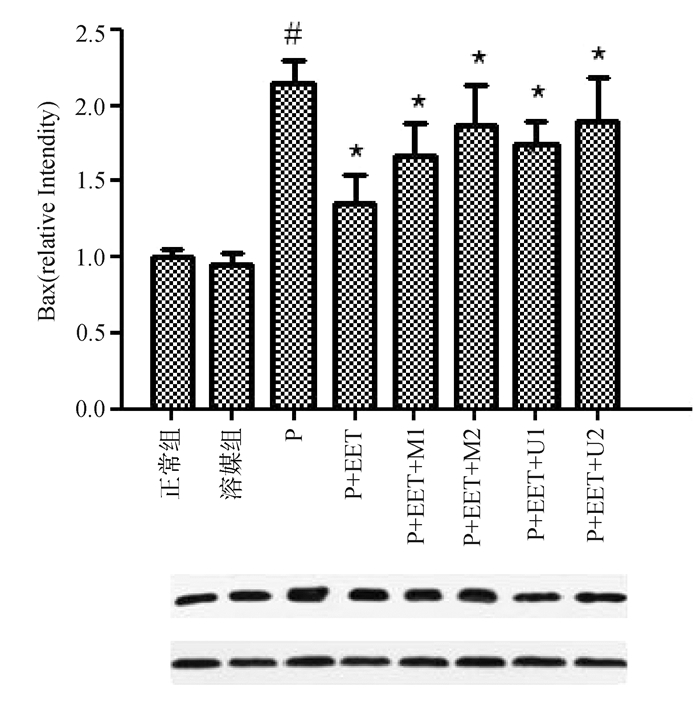
2.5 AKT与ERK1/2的抑制剂对H9c2细胞Bax表达的影响应用0.25 mmol/L Palmitate诱导H9c2细胞发生凋亡,同时加用终浓度为200 nmol/L的14,15-EET刺激H9c2细胞,分别合用终浓度为50,100 nmol/L的AKT抑制剂MK2206与终浓度为5,10 μmol/L的ERK1/2抑制剂U0126,共同孵育24 h后,收集细胞,提取H9c2细胞的蛋白质,应用Western blot的方法检测H9c2细胞中Bax表达。实验结果如图 3所示,与0.25 mmol/L Palmitate+200 nmol/L 14,15-EET组(P+EET组)相比较,0.25 mmol/L Palmitate+200 nmol/L 14,15-EET+50 nmol/L MK2206组(P+EET+M1组),0.25 mmol/L Palmitate +200 nmol/L 14,15-EET+100 nmol/L MK2206组(P+EET+M2组),0.25 mmol/L Palmitate+200 nmol/L 14,15-EET+5 μmol/L U0126组(P+EET+U1组),0.25 mmol/L Palmitate+14,15-EET+ 10 μmol/L U0126组(P+EET+U2组)的Bax表达水平显著增加(P < 0.05)。这些结果说明,AKT与ERK1/2抑制剂抑制了14,15-EET对H9c2细胞Bax表达水平的下调的作用。提示14,15-EET抑制Palmitate诱导的H9c2细胞的凋亡依赖于AKT与ERK1/2信号通路。
|
图 3 Western blot检测各组H9c2细胞Bax表达 与正常组比较,#P < 0.05;与P组比较,*P < 0.05 |
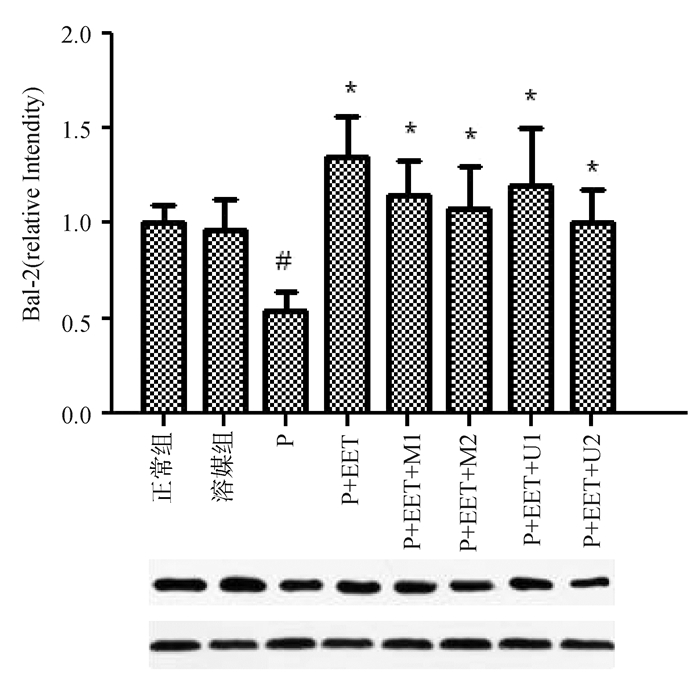
应用0.25 mmol/L Palmitate诱导H9c2细胞发生凋亡,同时加用终浓度为200 nmol/L的14,15-EET刺激H9c2细胞,分别合用终浓度为50,100 nmol/L的AKT抑制剂MK2206与终浓度为5,10 μmol/L的ERK1/2抑制剂U0126,共同孵育24 h后,收集细胞,提取H9c2细胞的蛋白质,应用Western blot的方法检测H9c2细胞中Bcl-2的表达。实验结果如图 4所示,与0.25 mmol/L Palmitate+200 nmol/L 14,15-EET组(P+EET组)相比较,0.25 mmol/L Palmitate+200 nmol/L 14,15-EET+50 nmol/L MK2206组(P+EET+M1组),0.25 mmol/L Palmitate +200 nmol/L 14,15-EET+100 nmol/L MK2206组(P+EET+M2组),0.25 mmol/L Palmitate+200 nmol/L 14,15-EET+5 μmol/L U0126组(P+EET+U1组),0.25 mmol/L Palmitate+14,15-EET+ 10 μmol/L U0126组(P+EET+U2组)的Bcl-2的表达水平显著降低(P < 0.05)。这些结果说明,AKT与ERK1/2抑制剂抑制了14,15-EET对H9c2细胞Bcl-2表达水平的上调作用。进一步提示14,15-EET抑制Palmitate诱导的H9c2细胞的凋亡依赖于AKT与ERK1/2信号通路。
|
图 4 Western blot检测各组H9c2细胞Bcl-2表达 与正常组比较,#P < 0.05;与P组比较,*P < 0.05 |
脂毒性是指游离脂肪酸的摄入和利用的不平衡,引起脂质聚集在心脏,导致心肌功能障碍或心肌肥厚。游离脂肪酸中的饱和脂肪酸已经被各类实验证实是脂毒性的主要贡献者,而棕榈酸盐(Palmitate)是饱和脂肪酸中最重要的一种,脂毒性心肌病的发病机制被认为是大量脂质聚集在心脏诱导心肌细胞凋亡或激活相关传导途径进而导致心肌损伤,心肌凋亡和损伤都是心功能下降的主要原因[7]。
凋亡细胞内的信号通路主要是Bcl-2家族的抗凋亡分子与促凋亡分子之间的平衡所控制的。抗凋亡蛋白Bcl-2过表达或促凋亡蛋白Bax沉默都可抑制死亡受体通路介导的心肌细胞凋亡[8, 9]。研究表明PI3K/AKT信号通路的活化在体外培养的心肌细胞和动物心肌梗塞模型中均可抑制caspase依赖的细胞凋亡[10]。进一步的实验证明,EETs在不同类型的细胞中可通过激活AKT信号通路发挥其促进细胞增殖和抗凋亡的作用[11],但是EET的抗细胞凋亡机制仍有待研究。本实验提示14,15-EET能通过上调抗凋亡蛋白Bcl-2,以及下调促凋亡蛋白Bax的表达抑制Palmitate诱导的H9c2细胞的凋亡,这些作用在AKT特异性抑制剂MK2206作用下被阻断,提示AKT信号通路在14,15-EET抑制Palmitate诱导的H9c2细胞凋亡作用中发挥重要作用。
MAPK家族通过级联反应激活转录因子,调节基因表达及细胞的增殖、分化和凋亡。ERK1/2通路是MAPK家族主要通路之一,在包括心肌细胞在内的多种类型细胞的凋亡过程中均发挥重要作用[12]。研究表明,ERK1/2信号通路的活化可以抑制硫化氢的抗高糖诱导的心肌细胞凋亡作用[13];丹参素可以通过ERK1/2信号通路的激活发挥抗大鼠缺血再灌注模型对心肌的损伤及抑制H9c2心肌细胞的凋亡作用[14]。与MK2206一样,本实验中14,15-EET的抗凋亡作用同样可以被ERK1/2特异性抑制剂U0126所阻断,提示ERK1/2信号通路在14,15-EET抑制Palmitate诱导的H9c2细胞凋亡作用中发挥重要作用。
综上所述,本实验对AKT及ERK1/2信号通路在14,15-EET的抗Palmitate诱导H9c2心肌细胞凋亡的作用进行了初步探讨,结果表明,AKT和ERK1/2信号通路与14,15-EET抑制Palmitate诱导H9c2心肌细胞凋亡有相关性,表现为AKT和ERK1/2通路抑制了14,15-EET对Palmitate诱导H9c2心肌细胞凋亡的抑制作用。其机制可能与Pamitate诱导H9c2心肌细胞后,14,15-EET通过激活AKT和ERK1/2信号通路,进而调节抗凋亡蛋白Bcl-2和促凋亡蛋白Bax的表达,从而发挥抗心肌细胞凋亡的作用有关,或AKT及ERK1/2信号通路的相互作用调节了心肌细胞的凋亡。本研究的不足之处在于没有对磷酸化ERK1/2和磷酸化AKT水平进行检测,因此只能对PI3K/AKT和ERK信号通路在14,15-EET抑制Palmitate诱导心肌细胞凋亡作用中的关系进行推测,要明确三者之间的关系有待进一步的研究。
| [1] | Zhao G, Wang J, Xu X, et al. Epoxyeicosatrienoic acids protect rat hearts against tumor necrosis factor-alpha-induced injury[J]. J Lipid Res,2012, 53 (3) : 456-466. DOI: 10.1194/jlr.M017319. |
| [2] | Wang Y, Wei X, Xiao X, et al. Arachidonic acid epoxygenase metabolites stimulate endothelial cell growth and angiogenesis via mitogen-activated protein kinase and phosphatidylinositol 3-kinase/Akt signaling pathways[J]. J Pharmacol Exp Ther,2005, 314 (2) : 522-532. DOI: 10.1124/jpet.105.083477. |
| [3] | Liu L, Chen C, Gong W, et al. Epoxyeicosatrienoic acids attenuate reactive oxygen species level, mitochondrial dysfunction, caspase activation, and apoptosis in carcinoma cells treated with arsenic trioxide[J]. J Pharmacol Exp Ther,2011, 339 (2) : 451-463. DOI: 10.1124/jpet.111.180505. |
| [4] | Xu S, Nam SM, Kim JH, et al. Palmitate induces ER calcium depletion and apoptosis in mouse podocytes subsequent to mitochondrial oxidative stress[J]. Cell Death Dis,2015, 6 (2) : 196-197. |
| [5] | van de Weijer T, Schrauwen-Hinderling VB, Schrauwen P. Lipotoxicity in type 2 diabetic cardiomyopathy[J]. Cardiovasc Res,2011, 92 (1) : 10-18. DOI: 10.1093/cvr/cvr212. |
| [6] | Falcao-Pires I, Leite-Moreira AF. Diabetic cardiomyopathy: understanding the molecular and cellular basis to progress in diagnosis and treatment[J]. Heart Fail Rev,2012, 17 (30) : 325-344. |
| [7] | Kerner J, Minkler PE, Lesnefsky EJ, et al. Fatty acid chain elongation in palmitate-perfused working rat heart: mitochondrial acetyl-CoA is the source of two-carbon units for chain elongation[J]. J Biol Chem,2014, 289 (14) : 10 223-10 234. DOI: 10.1074/jbc.M113.524314. |
| [8] | Zhai C, Tang G, Peng L, et al. Inhibition of microRNA-1 attenuates hypoxia/re-oxygenation-induced apoptosis of cardiomyocytes by directly targeting Bcl-2 but not GADD45Beta[J]. Am J Transl Res,2015, 7 (10) : 1 952-1 962. |
| [9] | Yang Y, Duan W, Lin Y, et al. SIRT1 activation by curcumin pretreatment attenuates mitochondrial oxidative damage induced by myocardial ischemia reperfusion injury[J]. Free Radic Biol Med,2013, 65 (9) : 667-679. |
| [10] | Jian J, Xuan F, Qin F, et al. Bauhinia championii flavone inhibits apoptosis and autophagy via the PI3K/Akt pathway in myocardial ischemia/reperfusion injury in rats[J]. Drug Des Devel Ther,2015, 9 (7) : 5 933-5 945. |
| [11] | Feng W, Xu X, Zhao G, et al. EETs and CYP2J2 inhibit TNF-alpha-induced apoptosis in pulmonary artery endothelial cells and TGF-beta1-induced migration in pulmonary artery smooth muscle cells[J]. Int J Mol Med,2013, 32 (3) : 685-693. |
| [12] | Luke JJ, Ott PA, Shapiro GI. The biology and clinical development of MEK inhibitors for cancer[J]. Drugs,2014, 7 (4) : 2 111-2 128. |
| [13] | Xu W, Wu W, Chen J, et al. Exogenous hydrogen sulfide protects H9c2 cardiac cells against high glucose-induced injury by inhibiting the activities of the p38 MAPK and ERK1/2 pathways[J]. Int J Mol Med,2013, 32 (4) : 917-925. |
| [14] | Yin Y, Guan Y, Duan J, et al. Cardioprotective effect of Danshensu against myocardial ischemia/ reperfusion injury and inhibits apoptosis of H9c2 cardiomyocytes via Akt and ERK1/2 phosphorylation[J]. Eur J Pharmacol,2013, 699 (13) : 219-226. |
 2016, Vol. 37
2016, Vol. 37

 ,
,