复发性流产(recurrent spontaneous abortion,RSA)是人类妊娠中常见的合并症,研究数据提示近年复发性流产的发病率为2%-5%,且发病率逐年上升[1]。目前关于复发性流产的病因尚不完全清楚,高达60%-70%的流产原因不明[2]。近年来母胎界面免疫功能异常在复发性流产研究机制中备受关注。研究显示早孕蜕膜可以合成多种肽类细胞因子,如转化生长因子β1 (transforming growth factor-β1,TGF-β1)、表皮生长因子等,其中TGF-β1具有免疫抑制、促进细胞分化、防止母体对胎儿的免疫免疫排斥功能,在妊娠维持中发挥重要作用[3]。本研究通过比较正常早期妊娠和复发性流产患者蜕膜组织中TGF-β1的表达,初步探讨TGF-β1的表达差异与复发性流产发病的相关性,为研究复发性流产的发病的机制提供理论依据。
1 材料与方法 1.1 研究对象选取2014年3月-2016年3月我院收治的复发性流产患者30例(复发流产组),自然流产次数≥3次,孕龄5-10(8.1±1.6) 周,年龄25-40岁,平均31.5岁。B超提示宫内妊娠,无胚芽和/或无原始心管搏动,选取同时期人工流产的健康早孕妇女32例(正常妊娠组)作为对照,孕龄5-10(7.9±2.1) 周,年龄23-38岁,平均33岁; B超提示宫内妊娠,有胚胎原始心管搏动,无自然流产史。两组受试者均排除染色体异常、全身性或感染性等相关疾病,年龄、孕周间差异无统计学意义(P>0.05)。
1.2 实验材料与仪器蜕膜组织均通过负压吸引术获得,于液氮中浸泡,-80 ℃冰箱保存使用; RNA抽提试剂Trizol和逆转录试剂盒购自Invitrogen公司;鼠抗人TGF-β1单克隆抗体购自美国Abcam公司; 羊抗鼠二抗购自Santa公司; 免疫组化SP试剂盒、DAB显色剂和苏木精购自北京中杉生物技术有限公司; OLYMPUS BX5l显微镜购自日本奥林巴斯。
1.3 标本的收集和处理复发性流产妇女孕囊自行排出者在常规消毒下刮取蜕膜组织,未排出者行负压吸引将蜕膜组织取出并分离。人工流产的健康早孕妇女在负压下吸取蜕膜组织。所有的标本均经生理盐水反复冲洗后,4%多聚甲醛固定。同时取两组的蜕膜组织,分别于液氮中冷冻浸泡,快速冻存于-80 ℃冰箱内。
1.4 免疫组织化学检测TGF-β1的表达分别取多聚甲醛固定的复发性流产组和正常妊娠组蜕膜组织约1 cm×1 cm,石蜡包埋,每个标本均做5 μm厚的连续切片。严格按照链霉菌抗生物素蛋白-过氧化物酶链接(SP)免疫组织化学试剂盒流程进行操作。常规二甲苯脱蜡,梯度乙醇脱水,枸橼酸盐缓冲液97.5 ℃烤箱内热修复30 min, 取出后冷却至室温,3%双氧水封闭过氧化物酶活性,37 ℃孵育10 min,磷酸盐缓冲液(PBS)冲洗,3 min×3次; 2%的山羊血清室温孵育30 min,封闭非特异性染色;滴加一抗1:100,4 ℃冰箱过夜,PBS冲洗3 min×3次,滴加二抗,37 ℃孵育30 min, PBS冲洗3 min×3次;DAB显色2-10 min,苏木精复染,常规脱水,透明,树胶封片。同时设立阳性和阴性对照。阳性结果判定:阳性部位为黄棕色颗粒;阴性对照:用1%BSA代替一抗。显微镜下随机观察10个视野,采用图像采集系统采集图像,运用Image Pro-plus Version 6.0图像分析软件进行图像积分密度(Integrated optical density,IOD)测量,测定每张切片的阳性值,阳性值与积分光密度成正比。
1.5 实时荧光定量PCR(RT-PCR)检测TGF-β1的mRNA表达水平 1.5.1 总RNA提取从-80 ℃冰箱内取出各组蜕膜组织,按照Trizol试剂说明书抽提各蜕膜组织总RNA,-80 ℃保存备用,采用紫外分光光度计和1%的琼脂糖凝胶测定其纯度、浓度和完整性。
1.5.2 cDNA的合成选取鉴定合格的RNA定量后,取总RNA 1 μl进行逆转录,按照反转录试剂盒说明书进行操作,将RNA反转录为cDNA,作为RT-PCR的模板,所得cDNA-20 ℃保存备用。
1.5.3 引物合成和设计TGF-β1和内参3-磷酸甘油醛脱氢酶(GAPDH)引物均由上海Sangon公司合成,引物序列如表 1所示。
| 表 1 TGF-β1和GAPDH的引物及序列 |
PCR反应体系为:总体积20 μl,上游引物和下游引物各0. 5 μl模板DNA 1 μl,20 × SYBR solution 1 μl,2. 5×Real Master Mix 8 μl用双蒸水补足至20 ml。实时荧光定量PCR仪反应条件为: 94 ℃预变性3 min后,94 ℃变性30 s,60 ℃退火30 s,72 ℃延伸1 min,共40个循环,最后72 ℃延伸5 min,一个循环。制备2%的琼脂糖凝胶,PCR产物8 μl,5 V/cm电压电泳,凝胶扫描成像系统分析电泳条带。目的基因/GAPDH的灰度比值表示其mRNA的表达水平。
1.6 Western Blot法检测TGF-β1蛋白表达取适量复发流产组和正常妊娠组的蜕膜组织,用裂解液裂解组织,4 ℃离心机离心去除沉淀,取上清液加入96孔板内用BCA法定量后,进行SDS-聚丙烯酰胺凝胶电泳,转膜。转膜结束后,用含5%脱脂奶粉的TBST封闭液室温封闭1 h。一抗4 ℃孵育过夜(一抗TGF-β1按1:1 000稀释),次日用PBS浸洗3次后,加入辣根过氧化物酶(HRP)标记的羊抗兔二抗(稀释1:300),37 ℃恒温箱孵育1 h,PBS洗3次,最后X线片曝光、显影和定影后观察结果。以β-actin作为内参,目的蛋白的相对表达水平=目的蛋白的灰度值/β-actin蛋白的灰度值,实验重复3次。
1.7 统计学分析检测数据均用均数±标准差(x±s)表示,两组间均数比较采用t检验。P<0.05为差异具有统计学意义。所有数据采用SPSS 13.0(SPSS, Chicago, IL, USA)软件包进行统计处理。
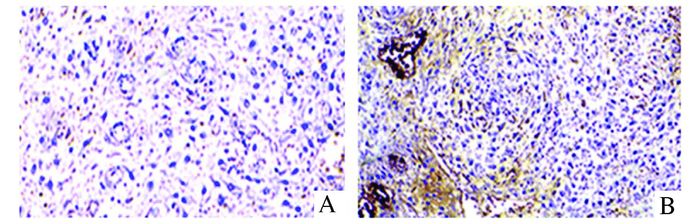
2 结果 2.1 免疫组化实验结果免疫组化结果图片如图 1所示,显微镜下观察到棕黄色颗粒为TGF-β1阳性表达,TGF-β1阳性颗粒主要表达于蜕膜组织的腺体细胞和间质细胞中。复发流产组和正常妊娠组TGF-β1免疫组化积分光密度(IOD)值检测结果如表 2所示:与正常妊娠组相比,复发流产组TGF-β1明显降低(P<0.05), 表明TGF-β1可能在正常妊娠维持中发挥重要作用。
|
图 1 TGF-β1在两组蜕膜组织中表达的免疫组化图片结果(×400) A:正常妊娠组,B:复发流产组 |
| 表 2 复发流产组和正常妊娠组TGF-β1蛋白免疫组化(IOD)分析结果(x±s) |
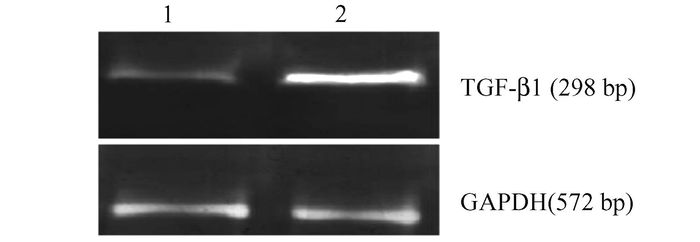
从两组蜕膜组织中提取的RNA经紫外线分析,OD260/OD280为1.9-2.0,说明RNA纯度较高,未受到DNA和蛋白质污染。RT-PCR结果表明:复发流产组蜕膜组织中TGF-β1 mRNA表达水平较正常妊娠组下降,差异有统计学意义(P<0.05),如图 2和表 3所示。
|
图 2 PCR检测复发流产及正常妊娠组中TGF-β1 mRNA的表达 1:复发流产组,2:正常妊娠组 |
| 表 3 复发流产组和正常妊娠组蜕膜组织中TGF-β1 mRNA表达水平 |
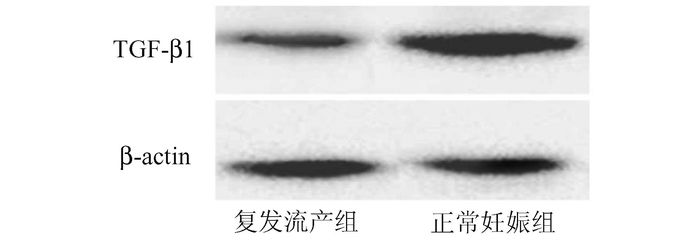
复发性流产组和正常妊娠组蜕膜组织中TGF-β1蛋白表达的Western Blot结果见表 4和图 3所示,与免疫组化和RT-PCR结果一致,复发性流产组的TGF-β1蛋白表达水平较正常妊娠组降低,差异具有统计学意义(P<0.05),提示蜕膜组织中TGF-β1水平降低可能是导致流产的重要因素。
|
图 3 Western Blot检测复发流产组和正常妊娠组中TGF-β1蛋白表达量 |
| 表 4 复发流产组和正常妊娠组蜕膜组织中TGF-β1蛋白Western Blot结果 |
复发性流产定义为妊娠在20周前自行终止,胎儿体重低于1 kg,并且连续发生3次或3次以上的病理性妊娠[4]。遗憾的是,目前临床对此尚无明确有效的方法来改善妊娠结局。复发性流产的发病机制非常复杂,包括染色体异常、免疫功能异常、生殖道感染、内分泌失调等。在生殖免疫学中,妊娠过程被认为是半同种移植,在正常妊娠过程中母胎界面形成免疫耐受,从而保护胚胎不受母体排斥[5]。然而,如果这种免疫耐受性受到损害将导致病理妊娠、自然流产的发生。近年来对TGF-β1与病理妊娠的相关性研究比较多。因此,本研究探讨了TGF-β1与复发性流产之间的关系,旨在为临床诊断复发性流产提供一定的参考价值。
TGF-β1是一种多功能细胞因子,由多种类型细胞分泌,包括外周血单个核细胞和调节性T淋巴细胞,亦可以表达于子宫内膜和早期妊娠蜕膜内,在细胞的生长、分化、免疫调节和细胞外基质形成中发挥着重要作用[6]。Jones等[7]研究也发现,TGF-β1定位于妊娠早、中晚期绒毛滋养细胞以及绒毛附近区域。母胎界面Th1/Th2细胞因子网络参与免疫调控,在胎儿的正常生长和发育发挥重要作用,Th2型细胞因子通过抑制Th1型细胞因子的免疫应答,维持正常妊娠顺利进行[8]。研究发现在母体血液循环中,TGF-β1的主要功能是限制免疫反应,介导Th2型细胞反应,诱导Th2型免疫偏倚,使妊娠得以成功进行[9]。TGF-β1在胚胎着床过程中起到负向免疫调节作用,提高子宫内膜的容受性,其可促进滋养细胞黏附并侵入子宫内膜,TGF-β1在子宫内膜的低表达是胚胎着床失败的重要原因[10]。TGF-β1也可通过刺激纤维和血管内皮生长因子的生长在胚胎种植过程中发挥重要作用[11]。亦有研究表明,TGF-β1可通过刺激子宫内膜中的基质细胞分泌细胞外基质蛋白,促进内膜的蜕膜化,从而有利于孕卵的着床[12]。研究发现由蜕膜细胞分泌的TGF-β1, 能降低蜕膜组织中NK细胞的活性, 抑制白细胞介素-1(IL-1) 的免疫刺激性, 控制滋养细胞的产生及分化等[3]。正常妊娠过程中妊娠期高水平的孕激素可以诱发妊娠期外周血单个核细胞表达TGF-β1的上调,提示高水平表达的TGF-β1参与维持正常妊娠,并在着床期间受激素水平的调控[14]。
值得注意的是,TGF-β1以自分泌或旁分泌方式对多种组织产生生物学效应,因此,检测TGF-β1在原位组织的表达比血浆水平分析更具相关性。本研究采用免疫组织化学法分析蜕膜组织中TGF-β1的表达情况,结果发现TGF-β1主要表达于蜕膜腺体和间质细胞中,与正常妊娠组相比,复发性流产组蜕膜组织TGF-β1的表达明显降低。Western Blot在TGF-β1蛋白水平检测结果和RT-PCR在mRNA水平结果相一致,发现复发流产组蜕膜组织TGF-β1的表达低于正常妊娠组,提示TGF-β1的表达下降可能与复发性流产的发生有关,与上述理论基本一致。TGF-β1在胚胎着床过程中起到负向免疫调节作用,主要功能是限制免疫反应,介导Th2型细胞反应,诱导Th2型免疫偏倚,使妊娠得以成功进行。本研究结果发现TGF-β1在复发流产蜕膜组织中的表达明显降低,因此我们推测,TGF-β1的表达下降可能是通过破坏上述妊娠机制,影响胚胎的着床,最终导致流产发生,其可能在复发性流产的诊断中具有较好的预测性。
总之,本研究发现,复发性流产患者蜕膜组织中TGF-β1的表达较正常妊娠组织下降,提示早期流产的发生与蜕膜组织中细胞因子的失衡有关。TGF-β1表达异常与复发性流产的发生密切相关,但由于复发性流产的病因和发病机制的复杂性,若想阐明TGF-β1和复发性流产间具体的分子机制仍需更多深入研究。
| [1] | Branch DW, Gibson M, Silver RM. Clinical practice. Recurrent miscarriage[J]. N Engl J Med, 2010, 363(18): 1740-1747. DOI: 10.1056/NEJMcp1005330. |
| [2] | Christiansen OB, Larsen EC, Egerup P, et al. Intravenous immunoglobulin treatment for secondary recurrent miscarriage: a randomised, double-blind, placebo-controlled trial[J]. BJOG, 2015, 122(4): 500-508. DOI: 10.1111/bjo.2015.122.issue-4. |
| [3] | Sun J, Yang M, Ban Y, et al. Tim-3 Is Upregulated in NK cells during early pregnancy and Inhibits NK cytotoxicity toward trophoblast in galectin-9 dependent pathway[J]. PLoS One, 2016, 11(1): e0147186. DOI: 10.1371/journal.pone.0147186. |
| [4] | Jauniaux E, Farquharson RG, Christiansen OB, et al. Evidence-based guidelines for the investigation and medical treatment of recurrent miscarriage[J]. Hum Reprod, 2006, 21(9): 2216-2222. DOI: 10.1093/humrep/del150. |
| [5] | Wang WJ, Liu FJ, Xin L, et al. Adoptive transfer of pregnancy-induced CD4+CD25+ regulatory T cells reverses the increase in abortion rate caused by interleukin 17 in the CBA/JxBALB/c mouse model[J]. Hum Reprod, 2014, 29(5): 946-952. DOI: 10.1093/humrep/deu014. |
| [6] | Khani M, Amani D, Taheripanah R, et al. Transforming growth factor beta-1 (TGF-beta1) gene single nucleotide polymorphisms (SNPs) and susceptibility to pre-eclampsia in Iranian women: A case-control study[J]. Pregnancy Hypertens, 2015, 5(4): 267-272. |
| [7] | Jones RL, Stoikos C, Findlay JK, et al. TGF-beta superfamily expression and actions in the endometrium and placenta[J]. Reproduction, 2006, 132(2): 217-232. DOI: 10.1530/rep.1.01076. |
| [8] | Wang S, Cao C, Piao H, et al. Tim-3 protects decidual stromal cells from toll-like receptor-mediated apoptosis and inflammatory reactions and promotes Th2 bias at the maternal-fetal interface[J]. Sci Rep, 2015, 5: 9013. DOI: 10.1038/srep09013. |
| [9] |
罗珊, 尹海宁, 李尚为. TGF-β1改善体外培养小鼠胚胎种植率及其作用机制的研究[J].
四川大学学报:医学版, 2010, 41(2): 265-268.
Luo S, Yin HN, Li SW. Effect of TGF-beta1 on embryo implantation and development in mice in vitro[J]. Journal of Sichuan University (Medical Science Edition), 2010, 41(2): 265-268. |
| [10] | Singh M, Chaudhry P, Asselin E. Bridging endometrial receptivity and implantation: network of hormones, cytokines, and growth factors[J]. J Endocrinol, 2011, 210(1): 5-14. DOI: 10.1530/JOE-10-0461. |
| [11] | Boussat S, Eddahibi S, Coste A, et al. Expression and regulation of vascular endothelial growth factor in human pulmonary epithelial cells[J]. Am J Physiol Lung Cell Mol Physiol, 2000, 279(2): L371-L378. |
| [12] | Kane NM, Jones M, Brosens JJ, et al. TGFbeta1 attenuates expression of prolactin and IGFBP-1 in decidualized endometrial stromal cells by both SMAD-dependent and SMAD-independent pathways[J]. PLoS One, 2010, 5(9): e12970. DOI: 10.1371/journal.pone.0012970. |
| [14] | Maurya VK, Jha RK, Kumar V, et al. Transforming growth factor-beta 1 (TGF-B1) liberation from its latent complex during embryo implantation and its regulation by estradiol in mouse[J]. Biol Reprod, 2013, 89(4): 84. |
 2017, Vol. 38
2017, Vol. 38

