2. 中南大学湘雅三医院/卫生部移植医学工程技术研究中心 湖南 长沙 410013
2. The 3rd Xiangya Hospital of Central South University & Research Center of National Health Ministry on Transplantation Medicine Engineering and Technology, Changsha 410013, China
肺移植是治疗多种终末期肺病唯一有效的方法,可以明显改善患者的生活质量,延长生存时间[1],但肺移植供体的短缺制约了其发展。脑死亡后捐献(donor after death, DBD)的出现有效缓解了供肺短缺的问题。然而,脑死亡会引起机体血流动力学、内分泌和免疫功能的改变,由此导致的肺损伤将明显降低供肺的质量,使其不适于移植[2]。细胞凋亡作为一种受基因调控的程序性死亡过程,涉及多种细胞因子的信号传递,可能参与脑死亡状态致肺脏损伤的免疫过程。本研究中我们利用家兔脑死亡模型,研究脑死亡状态下不同时间点肺组织的细胞凋亡和相关基因的表达变化,揭示脑死亡致肺损伤过程中细胞凋亡的作用,以期为脑死亡供体器官保护提供实验依据。
1 材料与方法 1.1 实验仪器及试剂BL-420生物机能实验系统、JR-1/2智能恒温控制仪和HX-100E动物呼吸机均购自成都泰盟科技有限公司。Foley 3F气囊导管、多功能心电监护仪、动物手术台及常规手术器械。RevertAidTM反转录试剂盒购自美国Fermentas公司。Caspase 3兔一抗购自武汉博士德生物工程有限公司。TUNEL试剂盒美国购自美国Roche公司。戊巴比妥(500 mg/kg)、0.3%肝素生理盐水注射液。
1.2 实验动物与分组健康家兔40只,清洁级,体质量(3.0±0.3) kg,购自武汉万千佳禾实验动物养殖中心,动物许可证号:SCXK(鄂)2007-0006。所有家兔饲养于标准实验条件(温度20-25 ℃,湿度50%-70%),均自由饮水,术前禁食12 h。采用随机数字表法将40只健康家兔分为假手术组(n=20):行气管插管、股动脉插管及钻孔开颅手术,置入Foley 3F气囊导管后不加压;脑死亡组(n=20):成功建立兔脑死亡模型。
1.3 兔脑死亡模型的建立采用改进的缓慢间断颅内加压法建立脑死亡模型[4]。将兔固定于动物手术台,经耳缘静脉注射戊巴比妥(500 mg/kg)进行全身麻醉后,于左腹股沟部手术暴露股动脉、静脉并插管,分别接生物机能实验系统和充满0.3%肝素生理盐水注射液的导管。颈部行气管插管术,备连接呼吸机。连接剑突,检测呼吸波。额、顶和枕极颅骨骨膜下埋置脑电图银针电极,两前肢及右后肢连接心电图导联,智能恒温控制仪维持深部体温38 ℃。完成上述步骤后,颅骨钻开颅,于硬脑膜外腔置入Foley 3F气囊导管,向导管内定时灌注生理盐水,0.2 ml/次,观察脑电图、心率、血压变化,保证维持在正常范围,直至自主呼吸停止,脑电图波动消失后,停止灌注,气管插管接呼吸机(呼吸频率35次/min,潮气量15 ml/kg,吸呼比5:4,氧浓度50%)。
1.4 脑死亡模型判定标准判定脑死亡的标准参照美国神经医学学会制定的《成人脑死亡诊断指南》及我国的《脑死亡判定标准与技术规范》[4, 5]。本实验脑死亡标准为:① 深昏迷,排除麻醉、低体温等可逆性昏迷的原因;② 瞳孔对光反射消失(反复2次),角膜反射消失;③ 自主呼吸停止;④ 脑电图波动消失。
1.5 参数监测多功能心电监测仪监测家兔脑死亡前及脑死亡后2, 6, 8 h的平均动脉压(mean arterial pressure, MAP)和心率(heart rate, HR)变化。
1.6 RT-PCR检测Bax的mRNA表达DEPC水灭菌且180 ℃高温烘烤的研钵中进行肺组织匀浆,采用Trizol试剂提取总mRNA,试剂盒反转录成cDNA后,PCR扩增Bax及GAPDH。其中,Bax前引物为:5′-TCAGGGTTTCATCCAGGACC-3′,后引物为:5′-TGATGAGCTCAGGCACCTTG-3′;GAPDH前引物为:5′-TCTGGCAAAGTGGATGTTGTC-3′,后引物为:5′-TCACGCCCATCACAAACAT-3′,由上海英骏生物公司合成。产物用2%的琼脂糖凝胶电泳检测,用Image J软件对目的条带进行灰度扫描,计算灰度值。mRNA的相对表达量=mRNA灰度值/同一标本GAPDH灰度值,对比值进行统计学分析。
1.7 免疫组织化学法检测肺组织caspase 3的表达取各时间点家兔肺组织,用聚赖氨酸浸泡5 min,依次采用二甲苯洗脱蜡、梯度酒精及水清洗2 min。3%的H2O2孵育10 min灭活内源性酶,蒸馏水洗3次。浸入枸橼酸盐缓冲液,重复2次,磷酸盐缓冲液(PBS)洗2次。5%牛血清白蛋白(BSA)在室温下封闭20 min,加入caspase 3兔一抗,37 ℃下孵育2 h,加入羊抗兔二抗,37 ℃下孵育20 min,PBS洗4次,5 min/次。DAB显色10 min,滴加Harris苏木精复染10 min,自来水冲洗5 min。依次加入梯度酒精、二甲苯石碳酸、二甲苯、二甲苯洗1 min,中性树脂封固,镜下观察。
1.8 TUNEL法检测肺脏细胞的凋亡TUNEL染色肺脏凋亡细胞的胞核呈黄褐色,非凋亡细胞的胞核呈蓝紫色,400倍光镜下观察,随机计数6个视野,计算凋亡指数(每100个细胞中凋亡细胞所占比例)。
1.9 统计学处理采用SPSS 19.0统计学软件。计量资料以均数±标准差(x±s)表示。经正态性检验,数据均符合正态分布。组间分析采用单因素方差分析,组内分析采用重复测量设计的方差分析,P<0.05为差异有统计学意义。
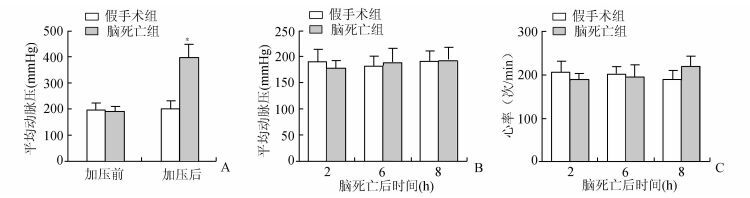
2 结果 2.1 脑死亡前及脑死亡后各时间点平均动脉压和心率变化脑死亡组和假手术组加压前MAP无明显差异(P>0.05)。开始颅内加压后,脑死亡组MAP峰值达(397.5±52.4) mmHg,明显高于加压前(P<0.01, 图 1A)。脑死亡状态时(停止加压后),气管插管接呼吸机,同时多巴胺2 μg/(kg·min)静脉滴入维持血压。检测停止加压后2, 6, 8 h MAP和HR,脑死亡组各时间点MAP、HR的差异及与假手术组各时间点MAP、HR的差异均无统计学意义(P>0.05, 图 1B、1C)。结果提示,在去神经支配的情况下,给予多巴胺等升压药物和呼吸机辅助呼吸支持,脑死亡后一段时间内家兔血压和心率可以维持在一定水平,生命体征相对稳定。
|
图 1 脑死亡前及脑死亡后各时间点动脉血压和心率变化 与同组加压前比较,*P<0.01;A.家兔颅内加压前后平均动脉压;B.家兔脑死亡后2, 6, 8 h平均动脉压;C.家兔脑死亡后2, 6, 8 h心率 |
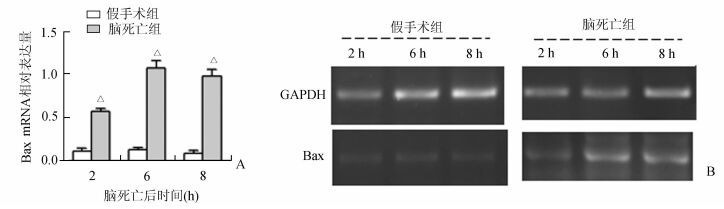
RT-PCR结果显示,假手术组各时间点Bax表达水平很低。脑死亡组各时间点Bax的mRNA水平较假手术组均升高,术后6, 8 h最为明显(图 2A, P<0.01)。
|
图 2 两组家兔肺组织Bax mRNA的表达 △与假手术组比较,P<0.01;A.Bax mRNA在两组中的相对表达量;B.两组Bax mRNA电泳结果(GAPDH为内参基因) |
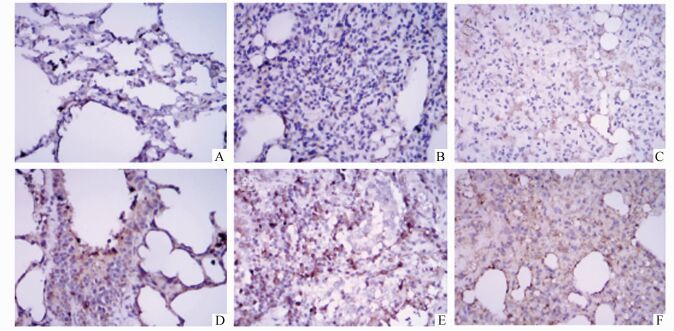
免疫组化检测caspase 3的蛋白表达,与假手术组相比,各时间点脑死亡组中caspase 3表达均明显升高。术后8 h,脑死亡组caspase 3蛋白阳性细胞比例接近100%(图 3)。
|
图 3 两组家兔肺脏caspase 3蛋白表达情况(免疫组化×200) 胞质中都可见caspase 3阳性表达,呈棕黄色;A-C.假手术组在术后2, 6, 8 h;D-F.脑死亡组组脑死亡后2, 6, 8 h |
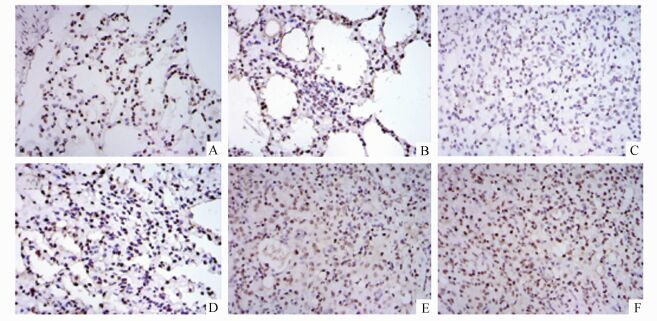
见图 4。各组肺脏TUNEL染色的凋亡指数值分别如下:假手术组2 h为(13.13±1.78)%,6 h为(15.52±3.91)%,8 h为(12.26±2.34)%;脑死亡组2 h为(31.24±6.67)%,6 h为(86.26±14.47)%,8 h为(92.75±9.83)%。两组各时段比较均有显著性差异。
|
图 4 两组家兔肺脏细胞凋亡的情况(免疫组化×200) TUNEL染色肺脏凋亡细胞的胞核呈黄褐色,非凋亡细胞的胞核呈蓝紫色;A-C.假手术组在术后2, 6, 8 h;D-F.脑死亡组组脑死亡后2, 6, 8 h |
脑死亡作为一种全脑功能不可逆性和永久性丧失的状态,常伴有机体明显的血流动力学、内分泌和免疫功能的改变,可能引起肺水肿、血管通透性增高及肺泡内出血,由此导致的供肺质量的下降将使其不适于移植。近期研究也发现,脑死亡供肺移植在排斥反应发生率等方面均明显高于活体供肺移植甚至心脏死亡供肺移植[6, 7]。因此,对脑死亡后肺移植供体的器官保护是目前亟待研究的课题。有文献报道,DBD的肺脏存在细胞的凋亡,并且会影响到供体的质量和移植后功能的恢复[8, 9]。本研究中我们利用家兔脑死亡模型,研究脑死亡状态下不同时间点肺组织的凋亡指数和相关基因的变化规律,揭示细胞凋亡对脑死亡致肺损伤过程的影响及相关基因在其发生机制中的作用,以期为脑死亡供肺器官的保护和移植后肺功能的改善提供实验依据。
本实验利用颅内缓慢气囊注水的方法建立家兔脑死亡模型,对家兔脑死亡前和脑死亡后若干个时间点的血压、心率、肺脏细胞凋亡、促凋亡基因Bax和蛋白酶caspase 3的表达等多个指标进行了检测。停止加压后2,6,8 h脑死亡组MAP、HR的差异及假手术组MAP、HR的差异均无统计学意义,表明脑死亡状态建立后,给予多巴胺等升压药物和呼吸机辅助呼吸支持,一段时间内心脏搏动功能和呼吸功能均无明显受损,进一步证实缓慢颅内加压法辅以呼吸循环支持是建立稳定的家兔脑死亡模型的有效方法。
各时间点TUNEL染色情况显示,脑死亡组和假手术组均检测到凋亡现象的发生。假手术组术后2 h肺泡壁可见肺上皮细胞凋亡;4 h,肺泡壁中开始出现炎症细胞浸润,上皮细胞凋亡加重;8 h,炎症细胞进一步浸润,凋亡指数无明显改变。对于脑死亡组,术后2 h即可见肺泡完整性丧失,存在明显炎症细胞浸润,凋亡指数(31.24%±6.67%)高于假手术组(13.13%±1.78%)(P<0.05);术后6, 8 h,视野中存在大量凋亡细胞,凋亡指数达80%以上。提示家兔肺脏细胞凋亡存在进行性发展,随着脑死亡时间延长逐渐加重。
Bax属于Bcl-2家族中的促凋亡基因,表达产物定位于细胞质。受凋亡信号刺激后,Bax会移位到线粒体外膜上,与抗凋亡蛋白如Bcl-2形成异源二聚体,并在外膜上形成通透性PT孔道,引起细胞色素C和促凋亡因子的释放,最终导致细胞凋亡[10]。RT-PCR结果显示,Bax在假手术组兔肺组织中低表达,而脑死亡组各时间点Bax的mRNA水平均高于假手术组,术后6,8 h差异最为明显。这与2 h到8 h肺组织中细胞凋亡逐渐加重的趋势一致,提示Bax可能参与介导脑死亡后细胞凋亡,引起肺脏损伤。研究也表明,Bax/Bcl-2的平衡对细胞凋亡起重要的调节作用,并决定了肺脏、心脏、肾脏等多种器官的存活状态,在器官移植后功能恢复中发挥重要作用[11]。
caspase 3是caspase家族中执行细胞凋亡效应的蛋白酶,它对特定蛋白底物进行水解,引起细胞死亡。Bax破坏线粒体外膜完整性后,释放细胞色素C,在dATP存在下细胞色素C通过半胱氨酸蛋白酶作用域与凋亡蛋白酶激活因子1(apoptotic protease-activating factor 1, Apaf-1) 结合形成凋亡体,并招募procaspase-9在其上寡聚,进而激活caspase-3,启动caspase凋亡级联反应[12]。因此,caspase3作为级联反应的下游因子, 与Bax互为关联,共同参与脑死亡后细胞凋亡的效应。免疫组化结果也显示,随着脑死亡时间延长,caspase 3表达逐渐升高,且与假手术组相比均有明显差异。
综合上述,我们认为由Bax、caspase 3在脑死亡状态致供体肺损伤的细胞凋亡过程中发挥着重要作用。如果能从这些凋亡相关基因入手,通过研究细胞凋亡与免疫过程的关系来研究其对脑死亡供体的影响,将为脑死亡供肺器官的存活、功能恢复指明一条新道路。
| [1] | Barnard JB, Davies O, Curry P, et al. Size matching in lung transplantation: an evidence-based review[J]. J Heart Lung Transplant, 2013, 32(9): 849-860. DOI: 10.1016/j.healun.2013.07.002. |
| [2] | Avlonitis VS, Wigfield CH, Kirby JA, et al. The hemodynamic mechanisms of lung injury and systemic inflammatory response following brain death in the transplant donor[J]. Am J Transplant, 2005, 5(4 Pt 1): 684-693. |
| [3] | Pratschke J, Wilhelm MJ, Laskowski I, et al. Influence of donor brain death on chronic rejection of renal transplants in rats[J]. J Am Soc Nephrol, 2001, 12(11): 2474-2481. |
| [4] | Wijdicks EF, Varelas PN, Gronseth GS, et al. Evidence-based guideline update: determining brain death in adults: report of the Quality Standards Subcommittee of the American Academy of Neurology[J]. Neurology, 2010, 74(23): 1911-1918. DOI: 10.1212/WNL.0b013e3181e242a8. |
| [5] |
宿英英, 张艳, 叶红, 等. 脑死亡判定标准与技术规范(成人质控版)[J].
中华移植杂志(电子版), 2015, 9(1): 13-17.
Su YY, Zhang Y, Ye H, et al. Criteria and practical guidance for determination of brain death in adults(BQCC version)[J]. Chin J Transplant: Electronic Edition), 2015, 9(1): 13-17. |
| [6] | Floerchinger B, Oberhuber R, Tullius SG, et al. Effects of brain death on organ quality and transplant outcome[J]. Transplant Rev (Orlando), 2012, 26(2): 54-59. DOI: 10.1016/j.trre.2011.10.001. |
| [7] | Kang CH, Anraku M, Cypel M, et al. Transcriptional signatures in donor lungs from donation after cardiac death vs after brain death: a functional pathway analysis[J]. J Heart Lung Transplant, 2011, 30(3): 289-298. DOI: 10.1016/j.healun.2010.09.004. |
| [8] | Zhou H, Fu Z, Wei Y, et al. Hydrogen inhalation decreases lung graft injury in brain-dead donor rats[J]. J Heart Lung Transplant, 2013, 32(2): 251-258. DOI: 10.1016/j.healun.2012.11.007. |
| [9] | Zhou H, Ding W, Cui X, et al. Carbon monoxide inhalation ameliorates conditions of lung grafts from rat brain death donors[J]. Chin Med J (Engl), 2008, 121(15): 1411-1419. |
| [10] | Husain MA, Ishqi HM, Sarwar T, et al. Identification andexpression analysis of alternatively spliced new transcript isoform of Bax gene in mouse[J]. Gene, 2017, 621: 21-31. DOI: 10.1016/j.gene.2017.04.020. |
| [11] | Guo W, Zhang Y, Ling Z, et al. Caspase-3 feedback loop enhances Bid-induced AIF/endoG and Bak activation in Bax and p53-independent manner[J]. Cell Death Dis, 2015, 6: e1919. DOI: 10.1038/cddis.2015.276. |
| [12] | Zhokhov SS, Desfeux A, Aubert N, et al. Bax siRNA promotes survival of cultured and allografted granule cell precursors through blockade of caspase-3 cleavage[J]. Cell Death Differ, 2008, 15(6): 1042-1053. DOI: 10.1038/cdd.2008.29. |
 2017, Vol. 38
2017, Vol. 38


