2. 武汉市中心医院检验科 湖北 武汉 430014;
3. 宜春学院医学院微生物与免疫学教古代室 江西 宜春 336000
2. Clinical Laboratory, Wuhan Central Hospital, Wuhan 430014, China;
3. Dept. of Microbiology and Immunology, Medical College of Yichun University, Yichun 336000, Jiangxi, China
最近研究表明,血管生成素-2(angiopoietin-2, ang-2) 具有早期促血管退化,又有启动新生血管形成的双重作用,是肿瘤形成的早期标志物之一。Ang-2的表达水平与肿瘤血管的数量、肿瘤的临床分期以及疾病预后有着一定的关系。因此,如何通过抑制ang-2在肿瘤血管形成中的作用,达到抑制肿瘤生长的目的,成为当前肿瘤治疗的一个新热点。
当前,RNA干扰技术已被广泛用于探索基因功能和传染性疾病及恶性肿瘤的治疗领域。该技术通过一些短片段的、高度保守的双链RNA诱导同源的特定基因的mRNA高效降解,特异性阻断体内特定基因表达,进而发挥抗感染、抗肿瘤等功能。
本实验旨在通过构建Ang-2基因沉默载体并转染hepG2细胞株,为进一步研究针对Ang-2为靶点治疗肝癌提供依据。
1 材料与方法 1.1 材料 1.1.1 细胞293T、hepG2细胞株由武汉巴菲尔生物技术服务有限公司提供。
1.1.2 主要实验试剂慢病毒干扰载体质粒pLVX-shRNA2(氨苄青霉素抗性,Amp+)购自SBI公司;SacⅠ、DL2000、T4 DNA Ligase均购自日本TaKaRa公司;BSAⅠ购自美国BioLabs公司;普通质粒小提试剂盒购自QIAGEN Plasmid Mini Kit公司;HET高效转染试剂盒购自深圳百恩维生物科技有限公司。
1.2 方法 1.2.1 shRNA片段的设计与合成根据ang2基因序列设计shRNA,3′端引入一个XhoⅠ位点。从金斯瑞公司合成shRNA片段,合成序列如下:
ang2-2-F:
5′-
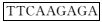

ang2-2-R:
5′-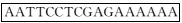
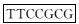
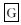
pLVX-shRNA2用限制性内切酶BamHⅠ过夜酶切,然后用EcoRⅠ第二次酶切。琼脂糖凝胶回收酶切大片段。
1.2.3 质粒pLVX-shRNA回收大片段与shRNA-ang-2的稀释退火产物,按照下列反应体系进行连接:pLVX-ShRNA2大片段1 μl,ShRNA退火产物1 μl,10×DNA Ligase Buffer 1 μl,T4 DNA Ligase 1 μl,ddH2O 6 μl,22 ℃水浴反应过夜。
1.2.4 各取10 μl过夜连接产物转化100 μl DH5α感受态细胞,均匀涂布于含Amp+的LB平板上,37 ℃恒温培养过夜。分别挑取4个单菌落接种于含Amp+的LB培养液中,37 ℃恒温摇床培养过夜,用小量质粒抽提试剂盒抽提质粒,并分别用XhoⅠ做酶切鉴定。阳性克隆可切出1 320 bp的条带。挑取酶切鉴定正确的菌液去测序,测序引物为U6-F:5′-GCTTCCTTAGCTCCTGAAA-3′。
1.2.5 细胞转染及病毒回收在转染前1 d按照每10 cm细胞培养皿接种6×106-8×106cells到10 cm细胞培养皿中对293T细胞换液培养。按照HET高效转染试剂盒说明进行配液,将所配液体包含HET Buffer 500 μl,Vector 10 μl,Lentiviral packaging mixture 15 μl, HET Buffer B 50 μl, ddH2O 425 μl。将上述混合液均匀加入至培养皿中,轻微混匀,置于培养箱中培养。12-16 h后用10 ml新鲜的完全培养基换液。分别于换液后24 h、48 h收获病毒上清,置于-80 ℃冰箱保存。再通过转染HEK293T细胞进行滴度测定,病毒滴度=(N×10 m+3) TU/ml(10 m为稀释倍数,N为带荧光的细胞数)。
1.2.6 hepG2细胞转染实验分组:pLVX-shRNA-ang-2组:以pLVX-shRNA-ang-2转染hepG2细胞;pLVX-s ang-2组:以pLVX-s ang-2转染hepG2细胞;对照组:未转染的hepG2细胞。转染后荧光镜下照像,并收集细胞作Western Blot。
1.2.7 Western Blot分析按文献提取hepG2细胞蛋白[2],进行SDS-PAGE, 转膜及随后的免疫反应等Western Blot操作过程。实验分3组:干扰质粒组、阴性质粒组分别予以LV-ang-2-shRNA、予LV-GFP进行转染,正常细胞组以单纯培养液培养。β-actin用于等量上样对照。
1.2.8 MTT法检测不同组hepG2细胞的增殖率按照上述分组方法对细胞进行干预,采用MTT法检测各组hepG2细胞的增殖率。
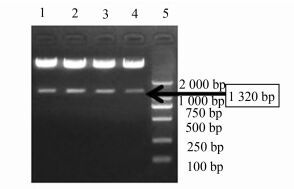
2 结果 2.1 酶切鉴定结果pLVX-shRNA2-ang-2的4个单菌落用XhoⅠ做酶切鉴定,鉴定图如图 1所示,4个克隆均可酶切到1 320 bp的条带,为阳性克隆。
|
图 1 pLVX-shRNA-ang-2的酶切鉴定 |
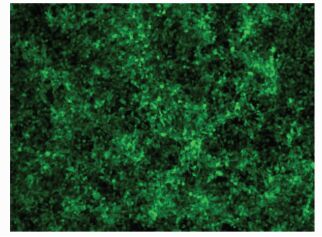
通过转染293T细胞获得了表达ang-2的慢病毒。再感染HEK293T细胞,倒置显微镜下显示绿色荧光(图 2),然后进行慢病毒滴度测定,测得慢病毒PLVX-ang-2滴度为:1×108 TU/ml。
|
图 2 慢病毒转染HEK293(48孔)48 h后绿色荧光 |
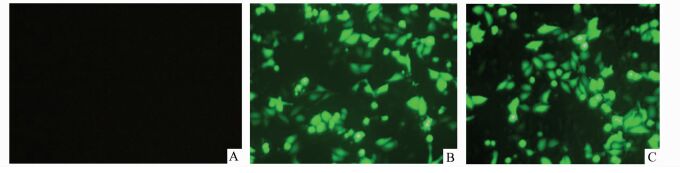
细胞转染后,在倒置荧光显微镜下观察,pLVX-shRNA-ang-2及pLVX-ang-2镜下可见大量绿色荧光表达,而未转染组镜下无荧光表达(图 3),表示慢病毒载体成功感染hepG2细胞,为后续Western Blot和MTT检测奠定基础。
|
图 3 慢病毒感染hepG2细胞后绿色荧光 A:未转染组;B:pLVX-shRNA-ang-2; C:pLVX-ang-2 |
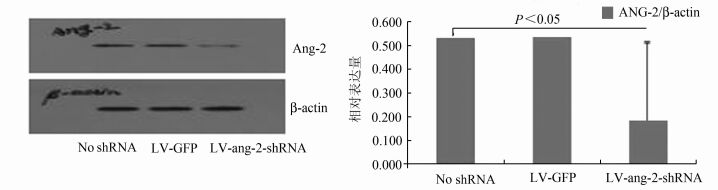
与单纯培养液及未转导shRNA组比较,经转导了shRNA-ang-2基因的hepG2细胞的ang-2基因及蛋白表达水平明显下降(P<0.05)(图 4)。
|
图 4 慢病毒pLVX-ang-2对hepG2细胞ang-2蛋白表达的影响 |
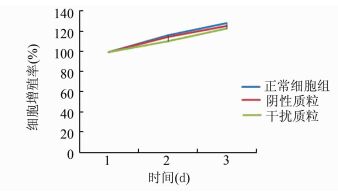
与单纯培养液及未转到shRNA组比较,经转导了shR-NA-ang-2基因的hepG2细胞增殖率无明显差异(P>0.05)(图 5)。
|
图 5 慢病毒pLVX-ang-2对hepG2细胞增殖率的影响 |
本实验采用RNA干扰技术,合成的pLVX-shRNA-ang-2经测序后,与设计序列ang-2一致,表明ang-2基因沉默载体构建成功。该载体质粒还带有GFP荧光蛋白,可用于病毒包装时转染率的测定及对靶细胞hepG2感染效率的判断。
我们通过获得的病毒颗粒感染靶细胞hepG2,感染96 h后,在倒置荧光显微镜下观察发现,LV-Ang-2-shRNA及LV-GFP进行转染组靶细胞内均可见大量绿色荧光,初步判定感染靶细胞成功。接下来,我们进一步通过Western Blot检测ang-2的沉默效率。从实验结果中可以看出,与单纯培养液及未转导shRNA组比较,LV-ang-2-shRNA感染hepG2细胞后,其ang-2蛋白表达水平明显下降(P<0.05),证明我们构建的ang-2基因沉默载体是成功的。
此外,国内外关于ang-2与细胞增殖凋亡的关系,研究较少,ang-2促进还是抑制细胞凋亡尚存在争论[14, 15]。从我们的实验结果可以看出,LV-ang-2-shRNA在抑制hepG2细胞增殖的作用上与其他两组相比,没有统计学差异。因而,从另一个角度说明了ang-2对肿瘤生长的促进作用,并非是促进肿瘤细胞本身生长,而是通过其他机制完成的,同时说明了我们设计的靶向ang-2的shRNA的有效性和特异性,再次证明我们构建的载体是成功的。
本研究结果为我们进一步开展实验奠定了基础,也为今后临床开展以ang-2为靶点的肿瘤血管生成疗法治疗肝癌提供了依据。
| [1] | Chung AS, Lee J, Ferrara N. Targeting the tumour vasculature: insights from physiological angiogenesis[J]. Nat Rev Cancer, 2010, 10(7): 505-514. DOI: 10.1038/nrc2868. |
| [2] | Lin J, Tang Y, Kang Q, et al. Curcumin inhibits gene expression of receptor for advanced glycation end-products (RAGE) in hepatic stellate cells in vitro by elevating PPARγ activity and attenuating oxidative stress[J]. Br J Pharmacol, 2012, 166(8): 2212-2227. DOI: 10.1111/j.1476-5381.2012.01910.x. |
| [3] | Lewis CE, Ferrara N. Multiple effects of angiopoietin-2 blockade on tumors[J]. Cancer Cell, 2011, 19(4): 431-433. DOI: 10.1016/j.ccr.2011.03.016. |
| [4] | Eklund L, Saharinen P. Angiopoietin signaling in the vasculature[J]. Exp Cell Res, 2013, 319(9): 1271-1280. DOI: 10.1016/j.yexcr.2013.03.011. |
| [5] | Daly C, Eichten A, Castanaro C, et al. Angiopoietin-2 functions as a Tie2 agonist in tumor models, where it limits the effects of VEGF inhibition[J]. Cancer Res, 2013, 73(1): 108-118. DOI: 10.1158/0008-5472.CAN-12-2064. |
| [6] | Lee HS, Oh SJ, Lee KH, et al. Gln-362 of angiopoietin-2 mediates migration of tumor and endothelial cells through association with α5β1 integrin[J]. J Biol Chem, 2014, 289(45): 31330-31340. DOI: 10.1074/jbc.M114.572594. |
| [7] | Mohr SE, Perrimon N. RNAi screening: new approaches, understandings and organisms[J]. Wiley Interdiscip Rev RNA, 2012, 3(2): 145-158. DOI: 10.1002/wrna.v3.2. |
| [8] | Mohr SE, Smith JA, Shamu CE, et al. RNAi screening comes of age: improved techniques and complementary approaches[J]. Nat Rev Mol Cell Biol, 2014, 15(9): 591-600. DOI: 10.1038/nrm3860. |
| [9] | Melen-Mucha G, Niedziela A, Mucha S, et al. Elevated peripheral blood plasma concentrations of tie-2 and angiopoietin 2 in patients with neuroendocrine tumors[J]. Int J Mol Sci, 2012, 13(2): 1444-1460. |
| [10] | Volkova E, Willis JA, Wells JE, et al. Association of angiopoietin-2, C-reactive protein and markers of obesity and insulin resistance with survival outcome in colorectalcancer[J]. Br J Cancer, 2011, 104(1): 51-59. DOI: 10.1038/sj.bjc.6606005. |
| [11] | Miyahara K, Nouso K, Morimoto Y, et al. Pro-angiogenic cytokines for prediction of outcomes in patients with advanced hepatocellular carcinoma[J]. Br J Cancer, 2013, 109(8): 2072-2078. DOI: 10.1038/bjc.2013.554. |
| [12] | Li P, He QY, Luo CQ, et al. Diagnostic and prognostic potential of serum angiopoietin-2 expression in human breast cancer[J]. Int J Clin Exp Pathol, 2015, 8(1): 660-664. |
| [13] | Lin ZJ, Liu Y, Sun YH, et al. Expression of Ets-1, Ang-2 and maspin in ovarian cancer and their role in tumor angiogenesis[J]. J Exp Clin Cancer Res, 2011, 30(1): 31. DOI: 10.1186/1756-9966-30-31. |
| [14] | Moritz F, Robert L, Alexander S, et al. Angiopoietin-2 differentially regulates angiogenesis through TIE2 and integrin signaling[J]. J Clin Invest, 2012, 122(6): 1991-2005. DOI: 10.1172/JCI58832. |
| [15] | Daly C, Pasnikowski E, Burova E, et al. Angiopoietin-2 functions as an autocrine protective factor in stressed endothelial cells[J]. Proc Natl Acad Sci U S A, 2006, 103(42): 15491-15496. DOI: 10.1073/pnas.0607538103. |
 2017, Vol. 38
2017, Vol. 38

 ,
,