2. 湖北省中医院/湖北省中医药研究院 湖北 武汉 430061
2. Hubei Provincial Hospital of TCM/Hubei Academy of Traditional Chinese
在青光眼、翼状胬肉、增生性视网膜病变等纤维增生性疾病中,病理过程的重要细胞学基础是成纤维细胞。成纤维细胞异常增殖往往是病理性瘢痕形成的主要原因[1, 2],尤其是青光眼滤过术后术区滤过通道的瘢痕形成,导致滤过通道堵塞,成为青光眼滤过性手术失败的重要原因[3]。当前,为抑制滤过道瘢痕形成,临床常使用5-氟尿嘧啶和丝裂霉素,但是会引起严重并发症。因此,寻找安全、有效的抗青光眼术后滤过泡瘢痕化药物是临床青光眼治疗亟待解决的难题。
原代细胞是体外开展细胞学研究的重要基础,尤其是眼疾特异性原代细胞,不仅在治疗方法研究中发挥重要作用,而且在体外诊断、药物检测、新药及其毒性筛选方法的建立中也起着关键作用,是眼疾药物体外研究的首选系统[4, 5]。原代Tenon’s囊成纤维细胞是阐明眼睛重要生理或病理过程所必需的,包括伤口愈合、药物释放、特异生长因子等[6-8]。目前,已有文献对培养人Tenon’s囊原代成纤维细胞进行研究,但组织块取自青光眼、白内障、翼状胬肉或斜视手术患者的Tenon’s囊[7, 9-12],限制了实验研究的开展。本研究对已有的原代成纤维细胞分离培养鉴定方法加以改良、补充,建立了一种简便、经济的方法,为后续青光眼术后滤过泡抗瘢痕化的药物研究提供成熟的原代成纤维细胞。
1 材料与方法 1.1 主要试剂与仪器DMEM培养基(Gibco),胎牛血清(Hycolon),0.25%胰酶(Gibco),青霉素-链霉素双抗溶液(中国杭州吉诺生物医药技术有限公司),Hoechst33342(北京索莱宝科技有限公司),角蛋白(KRT)单克隆抗体、波形蛋白(VIM)单克隆抗体(美国Abcam公司),反转录试剂盒(cDNA Synthesis Kit,北京安赞诺生物有限公司),荧光定量用预混液FastStart Essential DNA Green Master(德国罗氏公司),二氧化碳培养箱(上海一恒科学仪器有限公司),普通倒置显微镜(日本Olympus,CK2型),荧光倒置显微镜及照相系统(日本Olympus,IX81型),实时荧光定量PCR仪(美国伯乐公司,CFX96型),低温离心机(美国贝克曼Microfuge20R型)。
1.2 标本取材本研究经湖北省中医院伦理委员会审核批准,取材用健康成年新西兰白兔,无眼部疾患,体重(1.5±0.2) kg,由湖北省实验动物研究中心提供[许可证号SCXK(鄂)2015-0018]。将兔仰卧位固定于兔台上,耳缘静脉注射麻醉药,参照文献[12]方法,在无菌条件下,摘取Tenon’s囊组织,浸泡于无菌PBS液中(含青霉素300 U/ml,链霉素300 U/ml),冰盒中保存。
1.3 兔Tenon’s囊成纤维细胞的分离、培养将上步所摘取的Tenon’s囊组织标本,在超净台中用无菌PBS液(含青霉素100 U/ml,链霉素100 μg/ml)洗涤3次,滴加少量DMEM完全培养液(含10%胎牛血清,青霉素100 U/ml,链霉素100 μg/ml),无菌角膜剪将其剪成约0.5-1 mm2大小的微小组织块,另加入少量DMEM完全培养液,充分混匀,用无菌滴管将组织块混悬液均匀接种于灭菌90 mm玻璃培养皿中,每滴间隔1 cm左右。培养皿静置于37 ℃,5%CO2培养箱中,培养24 h后,组织块贴附,向培养皿中加入7 ml含DMEM完全培养液,于37 ℃、5%CO2培养箱中继续培养,普通倒置显微镜下观察,每3-4 d更换培养液1次。
当培养皿中细胞达70%-80%满度时,进行传代培养。吸弃培养皿中原培养液,无菌PBS洗涤1次,加入0.25%胰蛋白酶溶液,于37 ℃培养箱中静置2-3 min,显微镜下见细胞间隙增大、细胞变圆时,吸弃尽培养皿中胰蛋白酶溶液,加入DMEM完全培养液终止消化,反复吹打培养皿底,充分吹打均匀脱落细胞,以1:4或1:5比例传代,接种于培养瓶或培养孔板中,待细胞生长达70%-80%满度时,进行再次传代或相关实验研究。
1.4 兔Tenon’s囊成纤维细胞的免疫荧光鉴定将处于对数生长期细胞消化,接种于6孔细胞培养板中,接种密度为1×105个/孔,置于37℃,5%CO2培养箱中,待细胞生长达70%-80%满度时,吸弃孔中原培养液,PBS洗涤3次,4%多聚甲醛-0.01 mol/L PBS溶液(新鲜配制)室温固定30 min,加入小鼠单克隆抗波形蛋白抗体(1:10稀释度)、小鼠单克隆抗细胞角蛋白抗体(1:100稀释度)溶液,置于湿盒中4 ℃孵育过夜,次日PBS液洗涤细胞3次,加入山羊抗小鼠Alexa Fluor 488二抗(1:400稀释度)溶液,于37 ℃孵育2 h,PBS液洗涤细胞3次,加入Hoechst 33342液(浓度5 μg/ml)染核,室温静置5 min,PBS液洗涤3次,加入PBS液,于Olympus IX81型荧光倒置显微镜下观察,并拍照记录鉴定结果。
1.5 兔Tenon’s囊成纤维细胞中基因VIM、KRT3的实时荧光定量PCR鉴定待6孔细胞培养板中达70%-80%满度时,吸弃孔中原培养液,PBS洗涤1次,每孔加入Trizol溶液1 ml,充分吹打6孔细胞培养板板底,收集Tenon’s囊成纤维细胞Trizol液裂解样本。以兔角膜组织Trizol液裂解样本为对照,采用Trizol法提取各样本总RNA,用DNase Ⅰ消除所提总RNA中的基因组DNA污染,以此处理后的RNA为模板,按照Azanno公司反转录试剂盒说明书操作,合成各样本相应的cDNA。反转录反应体系总体积20 μl,具体为:5×RT Buffer 4 μl,Enzyme Mix 1 μl,Primer Mix 1μl,RNA template 10 μl,RNase-Free Water 4 μl。逆转录反应参数具体为:37 ℃,15 min;98 ℃,5 min;4 ℃,5 min。
根据NCBI上报道的基因序列,用软件Oligo 7设计基因GAPDH、VIM、KRT3实时荧光定量用上、下游引物,具体见表 1。以上述合成的cDNA为模板,采用SYBR Green Ⅰ染料法,在BioRad CFX96型荧光定量PCR仪上进行定量检测分析,设3个复孔。以基因GAPDH为内参,基因VIM、KRT3的相对表达量用2-△△Ct法计算。
| 表 1 荧光定量PCR用引物 |
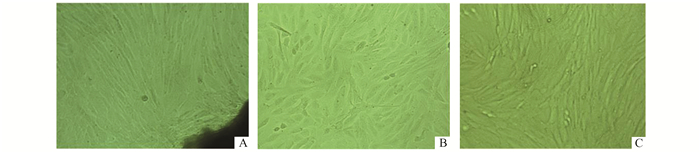
兔Tenon’s囊组织块培养5-7 d后,可见组织块边缘有细胞爬出,10-15 d细胞基本长满培养皿底。普通倒置显微镜下观察,组织块周围细胞呈放射状密集生长(图 1A),细胞大多数呈长梭形,放射状或旋涡状排列(图 1B,1C)。
|
图 1 组织块贴壁生长与成纤维细胞(10 d,×200) A:贴壁组织块,周围爬出成纤维细胞,细胞呈放射状密集生长;B:成纤维细胞,呈长梭形,放射状排列;C:成纤维细胞,呈长梭形,旋涡状排列 |
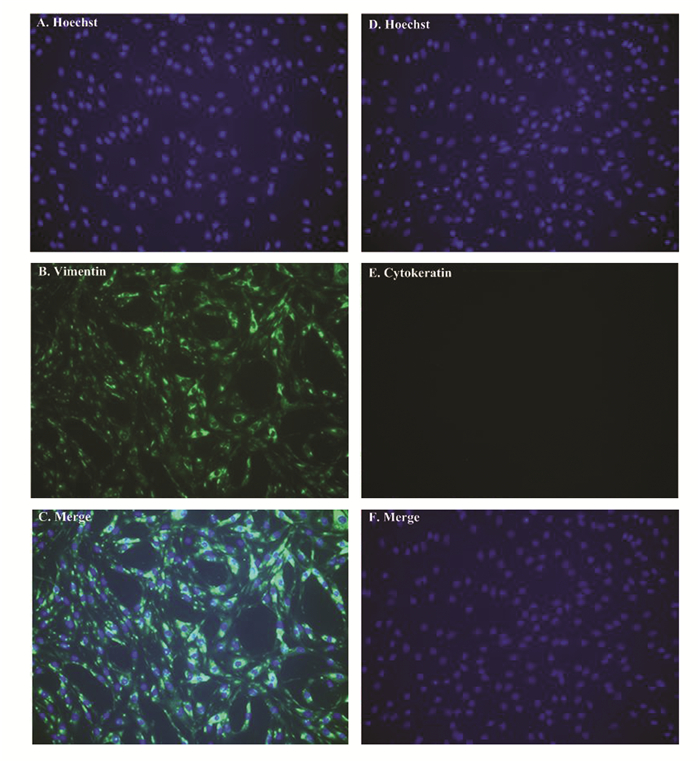
据文献报道,波形蛋白(vimentin)是成纤维细胞产生的构成性蛋白,为成纤维细胞特征性标志物,角蛋白(keratin)为上皮细胞的表面标志物[13]。为排除培养细胞中混杂结膜上皮细胞的可能,应用波形蛋白、角蛋白免疫染色技术检测培养细胞的成纤维细胞特征。成纤维细胞与波形蛋白抗体相互作用,细胞呈阳性反应,显绿色荧光(图 2A, B, C),而与角蛋白抗体作用后,细胞呈阴性反应,不显绿色荧光(图 2D, E, F)。
|
图 2 兔Tenon’s囊成纤维细胞的免疫荧光鉴定(10 d,×200) 细胞核被Hoechst 33342染成蓝色(A, D), 成纤维细胞与波形蛋白抗体作用后,呈阳性反应,显绿色荧光(B, C),而成纤维细胞与角蛋白抗体作用后,呈阴性反应,不显绿色荧光(图D, E) |
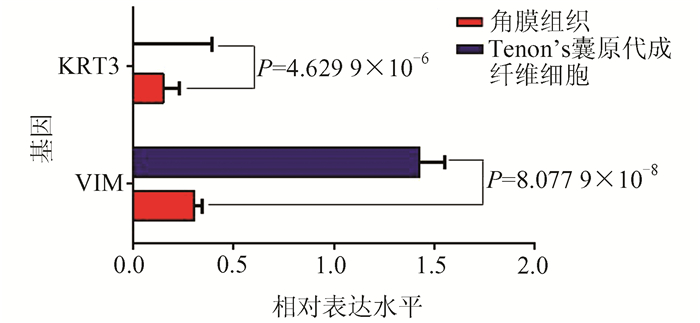
鉴于波形蛋白、角蛋白分别在成纤维细胞、上皮细胞中的特征性表达,应用实时荧光定量PCR方法,分别检测波形蛋白基因VIM、角蛋白基因KRT3在兔角膜组织(corneal tissue, corneal)与Tenon’s囊原代成纤维细胞(rabbit Tenon capsule fibroblast, Tenons cell)中mRNA的水平。结果见图 3,可见:在Tenon’s囊原代成纤维细胞中,基因VIM的表达水平是内参基因GAPDH的1.427 3倍,远远高于角膜组织中的表达量(0.305 7倍),差异极显著(P=8.079 9×10-8);基因KRT3的表达量只是基因GAPDH的2.467 4×10-5倍,远远低于角膜组织中的表达水平(0.150 4倍),存在极显著性差异(P=4.629 9×10-6)。
|
图 3 基因VIM、KRT3在角膜组织、Tenon’s原代成纤维细胞中的表达水平 |
随着对青光眼滤过术后滤过泡瘢痕化认识的不断深入,原代Tenon’s成纤维细胞成为开展相关研究的重要细胞系统。当前,相关研究中所用的成纤维细胞主要来自青光眼、白内障、翼状胬肉或斜视手术患者的Tenon’s囊[7, 9-12],细胞组织来源有限,不利于基础研究的广泛开展。本研究在已有原代成纤维细胞分离培养方法的基础上,进行改良补充,建立兔源性Tenon’s组织分离培养原代成纤维细胞的方法,以克服人Tenon’s囊原代成纤维细胞分离培养用组织块来源有限的不足。
基于已公开发表的人源性Tenon’s囊原代成纤维细胞培养方法[12],应用组织块培养法分离、培养兔Tenon’s囊原代成纤维细胞,获得较多原代细胞,倒置显微镜下观察细胞形态,结合公开报道的角蛋白、波形蛋白免疫荧光法鉴定成纤维细胞[13],补充角蛋白、波形蛋白基因荧光定量PCR法进行鉴定。组织块培养5-7 d后,显微镜下可见组织块边缘有细胞爬出,呈放射状密集生长(图 1A),大多数细胞呈长梭形,放射状或旋涡状排列(图 1B,1C)。其次,结合波形蛋白、角蛋白免疫染色技术,对培养出的细胞进行鉴定,以排除培养细胞中混杂结膜上皮细胞的可能,细胞与波形蛋白抗体相互作用,呈阳性反应,显绿色荧光(图 2A, 2B, 2C),与角蛋白抗体作用后,呈阴性反应,不显绿色荧光(图 2D, 2E, 2F)。然后,补充角蛋白、波形蛋白基因荧光定量PCR法进行鉴定,结果表明:在Tenon’s囊原代成纤维细胞中,波形蛋白基因相对表达量(1.427 3倍)远远高于角蛋白基因(2.467 4×10-5倍),差异极显著(P=8.079 9×10-8)。从细胞形态、免疫荧光、荧光定量PCR三方面鉴定,结果表明本实验培养出的是兔Tenon’s囊原代成纤维细胞。
总之,本研究改良了兔Tenon’s囊原代成纤维细胞体分离、培养方法,在原有形态、免疫荧光鉴定基础上,补充角蛋白、波形蛋白基因荧光定量PCR法,建立兔源性Tenon’s组织分离、培养、鉴定原代成纤维细胞的方法,为后续青光眼术后滤过泡抗瘢痕化的药物深入研究与抗瘢痕药物作用机制研究提供成熟的原代成纤维细胞。
致谢: 感谢武汉大学生命科学学院国家病毒重点实验室张祺老师提供实验指导与帮助,感谢湖北中医药大学针灸研究所全体老师大力协助。| [1] | Tello CA, Ahmed Ⅱ, Khaw PT. Failed trabeculectomy[J]. J Glaucoma, 2005, 14: 511-514. DOI: 10.1097/01.ijg.0000185616.60797.91. |
| [2] | Honjo M, Tanihara H, Kameda T, et al. Potential role of Rho-associated protein kinase inhibitor Y-27632 in glaucoma filtration surgery[J]. Invest Ophthalmol Vis Sci, 2007, 48: 5 549-5 557. DOI: 10.1167/iovs.07-0878. |
| [3] | Cui LJ, Sun NX, Li XH, et al. Subconjunctival sustained release 5-fluorouracil for glaucoma filtration surgery[J]. Acta Pharmacol Sin, 2008, 29: 1 021-1 028. DOI: 10.1111/aphs.2008.29.issue-9. |
| [4] | Smyth RJ, Moore JJ, Shapourifar-Tehrani S, et al. The effects of 5-fluorouridine, 5-fluorodeoxyuridine, and 5-fluorodeoxyuridine monophosphate on rabbit tenon's capsule fibroblasts in vitro[J]. J Ocul Pharmacol, 1991, 7: 329-338. DOI: 10.1089/jop.1991.7.329. |
| [5] | O'sNeill EC, Qin Q, Van Bergen NJ, et al. Antifibrotic activity of bevacizumab on human Tenon's fibroblasts in vitro[J]. Invest Ophthalmol Vis Sci, 2010, 51(12): 6 524-6 532. DOI: 10.1167/iovs.10-5669. |
| [6] | Choritz L, Grub J, Wegner M, et al. Paclitaxel inhibits growth, migration and collagen production of human Tenon's fibroblasts--potential use in drug-eluting glaucoma drainage devices[J]. Graefes Arch Clin Exp Ophthalmol, 2010, 248: 197-206. DOI: 10.1007/s00417-009-1221-4. |
| [7] | Leng F, Liu P, Li H, et al. Long-term topical antiglaucoma medications cause enhanced Tenon's capsule fibroblast proliferation and abnormal TGF-beta and MMP expressions: potential effects on glaucoma filtering surgery[J]. Curr Eye Res, 2011, 36: 301-309. DOI: 10.3109/02713683.2010.547648. |
| [8] | Kottler UB, Junemann AG, Aigner T, et al. Comparative effects of TGF-beta 1 and TGF-beta 2 on extracellular matrix production, proliferation, migration, and collagen contraction of human Tenon's capsule fibroblasts in pseudoexfoliation and primary open-angle glaucoma[J]. Exp Eye Res, 2005, 80: 121-134. DOI: 10.1016/j.exer.2004.08.018. |
| [9] |
陈珺, 李宁, 廖荣丰. 人眼Tenon's囊成纤维细胞原代培养的研究[J].
临床眼科杂志, 2016, 24(1): 1-4.
Chen J, Li N, Liao RF. In vitro culturing of human Tenon's capsule fibroblast cells[J]. J Clin Ophthalmol, 2016, 24(1): 1-4. |
| [10] | Fuchshofer R, Kottler UB, Ohlmann AV, et al. SPARC is expressed in scars of the Tenon's capsule and mediates scarring properties of human Tenon's fibroblastsin vitro[J]. Mol Vis, 2011, 17: 177-185. |
| [11] | Leonardi A, Tavolato M, Curnow SJ, et al. Cytokine and chemokine levels in tears and in corneal fibroblast cultures before and after excimer laser treatment[J]. J Cataract Refract Surg, 2009, 35: 240-247. DOI: 10.1016/j.jcrs.2008.10.030. |
| [12] | De Falco E, Scafetta G, Napoletano C, et al. A standardized laboratory and surgical method for in vitro culture isolation and expansion of primary human Tenon's fibroblasts[J]. Cell Tissue Bank, 2013, 14: 277-287. DOI: 10.1007/s10561-012-9325-1. |
| [13] | Jing J, Li P, Li T, et al. RNA interference targeting connective tissue growth factor inhibits the transforming growth factor-beta 2 induced proliferation in human tenon capsule fibroblasts[J]. J Ophthalmol, 2013, 2013: 354798. |
 2017, Vol. 38
2017, Vol. 38


