2. 北京信息职业技术学院医学门诊部 北京 100200;
3. 湖北省中医药大学附属医院内科 湖北 武汉 430061;
4. 武汉大学人民医院 精神科 湖北 武汉 430060
2. Medical Clinic, Beijing Information Technology College, Beijing 100200, China;
3. Dept. of Gastroenterology, Hubei Provincial Hospital of TCM, Wuhan 430061 , China;
4. Dept. of psychiatry, Renmin Hospital of Wuhan University, Wuhan 430060 , China
抑郁是引起肠易激综合征(irritable bowel syndrome,IBS)的重要致病因素,其在IBS的发病、症状发展与持续、治疗效果等方面起着不可忽视的作用和特征性联系[1]。它往往先于或伴随IBS出现,对其起到诱发或加重作用。抑郁与IBS相互作用,互为依存和放大,给抑郁患者带来极大精神病痛和胃肠道功能紊乱[2]。结肠平滑肌动力学异常和超敏反应是这一病理生理过程的具体表现,L-型钙通道(L-type calcium current,ICa-L)发生重构是它们的电生理基础和关键环节[3]。当抑郁发生后,结肠平滑肌细胞外Ca2+通过细胞膜上ICa-L进入细胞内,引起Ca2+内流增多,细胞膜电位升高,动作电位产生去极化状态,引起平滑肌细胞兴奋-收缩偶联增加,动作电位传导节律发生紊乱,导致结肠出现IBS病症[4],但有关抑郁引起结肠动力学改变导致细胞膜主要离子通道ICa-L重构引起IBS病症的电生理机制还不完全清楚,本文将对此进行探讨,为临床合理选择药物治疗抑郁合并IBS患者提供理论基础和实验依据。
1 材料与方法 1.1 动物与溶液试剂实验动物均选取SPF级Sprauge-Dawley(SD)雄性大鼠,由武汉大学医学院实验动物中心提供,鼠龄8周,体质量200-250 g。正常Tyrode液成分(mmol/L):NaCl 147.0,KCl 5.4,CaCl2 2.0,glucose 10.0,MgCl2 1.05,NaH2-PO4 0.42,HEPES 10.0,pH用NaOH 调至7.35。无钙生理盐溶液(free-Ca2+ physiological saline solution,free-Ca2+ PSS)成分(mmol/L):NaCl 135.0,KCl 5.0,MgCl2 1.2,葡萄糖 10.0,HEPES 10.0,pH用Tris-HCl调至7.4。获得结肠平滑肌细胞的消化液为含如下试剂的Ca2+-free PSS液:0.12% CollagenaseⅡ,0.2%胰蛋白酶抑制剂和0.2% BSA。记录ICa-L的电极内液成分(mmol/L):CsCl 135.0,MgCl2 4.0,HEPES 10.0,Na2-ATP 2.0,EGTA 10.0,TEA 20.0,pH用CsOH调至7.3。记录ICa-L的电极外液成分为正常Tyrode液。HEPES、CollagenaseⅡ、胰蛋白酶抑制剂、BSA、CsCl、CsOH、Na2-ATP、EGTA、TEA 为Sigma公司产品,其它为国产分析纯。
1.2 实验分组与抑郁症模型制备及评估本实验购回35只大鼠, 单笼饲养于本院实验动物中心(标准SPF级动物室)1周, 之后进行抑郁模型复制[5]。但在造模前, 先利用旷场试验(open field test, OFT)对每只动物展开水平和垂直运动筛查评分, 总得分低于30分和高于120分的动物予以剔除。被入选实验动物随机分为2组:正常对照组(对照组)与抑郁症模型组(抑郁组), 每组15只。对模型组动物采用慢性温和不可预知性应激刺激(chronic unpredictable mild stress, CUMS)合并独笼孤养的经典方法制造抑郁大鼠模型。造模经过第28天后分别检测动物体重和摄食量, 采用OFT测定大鼠的行动, 观察液体消耗试验(fluid consumption test, FCT)中糖水消耗量作为快感缺乏的客观指标判定抑郁症模型是否复制成功。体质变化包括:大鼠体重增长数和摄食量; OFT包括:总行程、平均运动速度、穿越格数、后肢直立次数、理毛次数及粪便颗粒数; FCT包括:总液体消耗、糖水消耗、纯水消耗, 大鼠的糖水偏爱(%)=糖水摄入/总液体消耗×100%。
1.3 抑郁对大鼠排便影响的观察指标通过观察造模前后大鼠出现临床表现、生成的粪便性状和数量加以确定, 并最后确定抑郁诱发大鼠IBS发生率。临床表现主要观察动物体质、状态、活动度以及排便情况; 粪便性状和数量是计数大鼠粪便颗粒数和含水量, 具体方法是记录大鼠抑郁模型制造之前1 d和完成后第28天, 选取同一时间起始点记录2 h内大鼠排出粪便的颗粒数, 并进行收集、称重(湿重), 后用烘箱烘干(75 ℃, 2.5 h), 再称重(干重), 计算粪便含水量(%)=(湿重-干重)/湿重×100%。抑郁诱发大鼠IBS发生率(%)=抑郁数/观察组数×100%。
1.4 大鼠结肠平滑肌细胞的分离和全细胞膜片钳记录大鼠经颈椎脱臼处死,剪开腹腔,在靠近回肠处取4-5 cm长的近端结肠,剖开、清洗、平摊并固定于硅胶板上。在解剖显微镜下分离黏膜层和黏膜下层得到肌条,将肌条剪成2 mm×4 mm小块,置于Ca2+-free PSS液中漂洗20 min,后在含消化液的Ca2+-free PSS液中消化15-20 min(37 ℃,100% O2饱和),得到含有单个结肠平滑肌细胞悬液,置于4 ℃冰箱备用。吸数滴细胞悬液加入到倒置显微镜(IX 70-122,日本Olympus公司)载物台上的细胞记录槽中(25-30 ℃,260 μl,美国Warner公司),静置5 min,后用100% O2饱和的记录ICa-L的细胞外液以2-3 ml/min速度冲灌10 min,用全细胞膜片钳记录方法对细胞进行钳制,脉冲信号由Pulse+Pulsefit软件(version8.31,德国HEKA公司)控制,经EPC-9放大器(德国HEKA公司)放大,Pulse软件收集并存储于计算机的硬盘中。玻璃微电极充灌电极内液后电阻为2.5-3.5 MΩ,对结肠平滑肌细胞进行封接,当封接电阻达1 GΩ以上后,补偿快电容,施加负压吸破细胞膜,给予慢电容和漏电容补偿,形成全细胞记录模式。
1.5 ICa-L记录及其电流-电压(I-V)曲线拟合将膜电位钳制在-60 mV,指令电位由-60 mV到+50 mV,跃阶10 mV,钳制时间300 ms,可记录到一组缓慢的内向电流,此内向电流为ICa-L(单位:pA),存入计算机以供统计分析。各组ICa-L的I-V曲线是以各自指令电位为横坐标,每个指令电位下的电流大小为纵坐标拟合而成。
1.6 统计学处理计量数据符合正态分布和方差齐性以均数±标准差(x±s)表示,多组数据比较用单因素方差分析(One-way ANOVA),两两比较采用F检验,统计分析用Origin 6.0软件完成;相关性分析用Pearson相关系数(r)法;计数资料以率表示。 P<0.05为差异有统计学意义。
2 结果 2.1 成功建立抑郁大鼠模型与对照组比较,抑郁组大鼠明显消瘦,体重增长速度明显放缓(P<0.01,n=15) ;穿越格数、前腿竖立次数、理毛时间均减少(P均<0.01,n=15) ;糖水消耗、饮水总量、糖水消耗/纯水消耗均显著降低(P均<0.01,n=15) 。提示本实验抑郁模型的制备取得成功(表 1) 。
| 表 1 建立抑郁大鼠模型的观察结果(x±s,n=15) |
与对照组比较,抑郁组大鼠出现明显的毛发干枯、疏松、成直刺状,食欲减退、活动度减少、消瘦、排便次数明显增加,大便性状为稀水或糊状。排便颗粒数及其含水量分别由对照组的(3.95±0.48) 粒/2 h和(36.72±7.49) %增加为(7.31±1.03) 粒/2 h和(75.39±10.87) %(P均<0.01,n=15) ;分别与抑郁组中OFT和FCT比较,排便颗粒数及其含水量呈显著的负相关性(r值均>-0.89,P均<0.01);与对照组比较,抑郁组大鼠出现上述症状的发病率达到87.36%,明显高于对照组的9.21%(P<0.01,n=15) 。
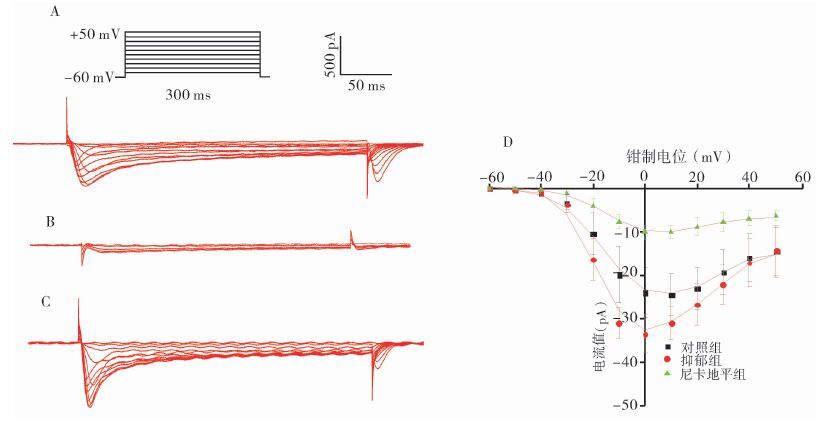
2.3 抑郁对结肠平滑肌细胞ICa-L及其I-V曲线影响研究发现,在对照组大鼠结肠平滑肌细胞膜上记录的内向电流,在-40 mV开始激活,+10 mV达到最大,后随钳制电压的增加,逐步减小,给予10 μmol/L尼卡地平,可严重抑制各钳制电压下的电流峰值,表明此内向电流为ICa-L(图 1A和B)。与对照组比较,抑郁组大鼠结肠平滑肌细胞膜上ICa-L自激活开始,在各钳制电压下均明显增加,当钳制电位为+10 mV时,其ICa-L由对照组的(-21.31±4.79) pA增加为(-33.52±4.45) pA(P<0.01,n=15) (图 1C)。与抑郁组大鼠排便颗粒数及其含水量比较,抑郁组大鼠结肠平滑肌细胞膜上ICa-L与它们具有显著正相关(r均>0.91,P均<0.01) 。从各组拟合ICa-L的I-V曲线上发现(图 1D),对照组的I-V曲线处在中部,最大峰值在+10 mV左右;抑郁组I-V曲线处在最底部,最大峰值在0 mV左右,略向左偏移,但各组I-V曲线形态没有发生明显改变。
|
图 1 结肠平滑肌细胞膜上ICa-L及其I-V曲线变化 A.对照组;B.尼卡地平组;C.抑郁组;D.各组I-V曲线比较 |
抑郁患者比没有抑郁的病人更容易出现IBS症状,而IBS患者中几乎有一半患者会出现抑郁等精神心理障碍,但有关抑郁引起IBS病因基础目前仍处在初步研究阶段,对其影响IBS的详细机制还很少涉及,需要有更多实验投入到这些研究中[6]。本文对此开展了一些研究,首先是制备抑郁模型,结果发现抑郁组大鼠明显消瘦,体重增长严重放缓; OFT和FCT测试的各项观察指标明显低于对照组。提示这些大鼠的活动度严重不足,对周围的新鲜事情的好奇度严重缺乏; 失去对糖水的喜好,对新鲜事物表现出抵触情绪,对各种奖赏缺乏兴趣和热情度以及快感。说明本文抑郁组大鼠被成功复制成抑郁模型,且理论依据符合临床上抑郁患者起病于慢性、低水平的应激源促进疾病发生、发展的机理; 评价建立抑郁模型是否成功的标准和文献报道相一致,操作方法稍简单、易行,病死率不高,值得一些需要制造抑郁模型的实验室借鉴、尝试[7]。
本研究发现抑郁大鼠出现明显毛发干枯、食欲减退、消瘦、排便次数明显增加、大便表现为稀水或糊状,排便颗粒数及其含水量显著增高,与运动试验和液体消化试验各数据相比呈显著负相关。提示抑郁大鼠出现了严重的胃肠道症状,诱发了IBS,而且这种发生率达到87.36%。说明抑郁组大鼠在遭受长期慢性应激刺激后,精神上出现症状,之后诱发了胃肠道IBS病症[8]; 反映出抑郁导致大鼠结肠动力持续异常、运动过度以及节律失常,而IBS症状可能成为抑郁的躯体化表现,且这些顽固的躯体化症状反过来又加重抑郁症状反复发作和恶化[9]。
研究还发现抑郁大鼠结肠平滑肌细胞膜上ICa-L在各钳制电压下均显著增大,幅度增高,其I-V曲线明显上抬,并略向左偏移; 与其排出粪便颗粒数和含水量相比,具有显著正相关,提示抑郁诱发了大鼠结肠平滑肌细胞膜ICa-L的明显增加与开放速度增快,而这种ICa-L的增加和开放速度增快可能源自于抑郁大鼠结肠出现IBS病症[10]; 说明在抑郁长期刺激下,大鼠结肠平滑肌细胞膜ICa-L的数量出现了增加、或更多的开启与分布,抑郁造成了结肠平滑肌细胞膜ICa-L的电重构,在其基础上,细胞外Ca2+通过ICa-L进入细胞内增多,并引起Ca2+触发Ca2+释放的连锁反应,使肌浆网钙池中储备的Ca2+释放到胞质中,双管齐下,造成结肠平滑肌细胞内Ca2+超载,引起Ca2+震荡,诱发结肠性动作电位节律失常,动作电位上出现早后除极和(或)晚后除极,从而打破平滑肌正常的兴奋收缩偶联活动,使结肠平滑肌收缩反应过度,张力增高,最终诱发IBS症状[11]。所以本结果提示,抑郁大鼠结肠平滑肌细胞膜ICa-L的增加是抑郁引起患病大鼠出现IBS症状的动力基础和致病机制[12]。
总之,采用慢性不可预见性温和刺激加孤养相结合经典方法可成功制备抑郁动物模型。抑郁可促进大鼠结肠平滑肌运动异常亢进病理生理反应,致使动作电位的传导节律失常、紊乱,出现IBS病症,其电生理机制可能是抑郁引起了大鼠结肠平滑肌细胞膜ICa-L的异常增加引起离子通道电重构,导致结肠平滑肌细胞动作电位节律失常。通过本研究能针对性指导临床医师在治疗抑郁并发IBS症状过程中找到新的治疗靶点及其理论基础。
| [1] | Hillilä MT, Siivola MT, Färkkilä MA. Comorbidity and use of health-care services among irritable bowel syndrome sufferers[J]. Scand J Gastroenterol, 2007, 42(7): 799-806. DOI: 10.1080/00365520601113927. |
| [2] | Lee S, Wu J, Ma YL, et al. Irritable bowel syndrome is strongly associated with generalized anxiety disorder: a community study[J]. Aliment Pharmacol Ther, 2009, 30(6): 643-651. DOI: 10.1111/apt.2009.30.issue-6. |
| [3] | Gallego D, Aulí M, Aleu J, et al. Effect of otilonium bromide on contractile patterns in the human sigmoid colon[J]. Neurogastroenterol Motil, 2010, 22(6): e180-e191. DOI: 10.1111/nmo.2010.22.issue-6. |
| [4] |
谭樺, 罗和生. 离子通道与肠易激综合征[J].
中华消化杂志, 2009, 29(9): 582-584.
Tan H, Luo HS. Ion channels and irritable bowel syndrome[J]. Cnin J Dig, 2009, 29(9): 582-584. |
| [5] | Willner P. Chronic mild stress (CMS) revisited: consistency and behavioural- neurobiological concordance in the effects of CMS[J]. Neuropsychobiology, 2005, 52(2): 90-110. DOI: 10.1159/000087097. |
| [6] |
许东, 方秀才, 王承党. 抗抑郁药对肠易激综合征的疗效及其机制研究进展[J].
中华医学杂志, 2012, 92(48): 3445-3447.
Xu D, Fang XC, Wang CD. Progress of treatments and mechanisms on antidepressants on irritable bowel syndrome[J]. Natl Med J China, 2012, 92(48): 3445-3447. |
| [7] | Gronli J. Effects of chronic mild stress on sexual behavior, locomotor activity and consumption of sucrose and saccharine solutions[J]. Physiol Behav, 2005, 84(4): 571-577. DOI: 10.1016/j.physbeh.2005.02.007. |
| [8] | Joenes MP, Growell MD, Olden KW, et al. functional gastrointestinal disorders: an update for the psychiatrist[J]. Psychosomatics, 2007, 48: 93-102. DOI: 10.1176/appi.psy.48.2.93. |
| [9] |
黄丹, 方秀才, 朱丽明. 抗抑郁剂在肠易激综合征治疗中的作用[J].
中华内科杂志, 2012, 51(1): 70-72.
Huang D, Fang SC, Zhu LM. Effects of treatments on antidepressants in irritable bowel syndrome[J]. Chin J Intern Med, 2012, 51(1): 70-72. |
| [10] | Saito YA, Strege PR, Tester DJ, et al. Sodium channel mutation in irritable bowel syndrome: evidence for an ion channelopathy[J]. Am J Physiol Gastrointest Liver Physiol, 2009, 296: G211-G218. |
| [11] |
祝捷, 罗和生, 陈玲, 等. 腹泻型肠易激综合征大鼠结肠L-型钙通道α1C及α1D亚基的表达变化[J].
中华医学杂志, 2009, 89(38): 2713-2717.
Zhu J, Lou HS, Chen L, et al. Altered expression of L-type calcium channel a1C and a1D subunits in colon of rats with dlarrheapredominant irritable bowel syndrome[J]. Natl Med J China, 2009, 89(38): 2713-2717. |
| [12] | Qian AH, Liu XQ, Yao WY, et al. Voltage-gated potassium channels in IB4-positive colonic sensory neurons visceral hypersensitivity in the rat[J]. Am J Gastroenterol, 2009, 104(8): 2014-2027. DOI: 10.1038/ajg.2009.227. |
 2017, Vol. 38
2017, Vol. 38
