射线诱导的组织和器官的纤维化是肿瘤放疗过程中出现的严重副作用之一。全身照射(total body irradiation,TBI)是一种常见的放疗方式,广泛运用于临床治疗各种实体肿瘤和血液系统疾病[1]。但其可以导致一些严重的并发症如放射性肺炎[2]、肾炎[3]、白内障[4]等。肾脏是一类射线敏感器官,TBI或腹部肿瘤的放疗会导致慢性进行性肾功能损害。研究发现放射性肾损伤引起明显临床症状一般发生于TBI后1-1.5年,临床主要表现为血肌酐升高、蛋白尿、血尿、贫血、高血压等[5]。Borg[6]等回顾性分析7年间因骨髓移植行全身照射预处理的59例患者临床资料,4例患者在骨髓移植后12个月出现血肌酐升高,在存活时间达2年的33例患者中2例血肌酐升高,肾脏病理可见系膜细胞增生、溶解、毛细血管内皮细胞肿胀等。TBI导致肾功能异常可能有多方面原因,一方面患者原发病因如多发性骨髓瘤、蛋白复合物在肾脏的沉积、长期抗生素的使用、感染等,另一方面TBI可以诱导转化生长因子(TGF)-β信号通路活化导致放射性肾病。
既往体外研究将大鼠肾小管上皮细胞暴露于X射线下会促使其发生表型改变,细胞外基质合成相关基因如纤溶酶原抑制物激活因子(PAI)-1,TGF-β1,基质金属蛋白酶(MMP)-2,胶原蛋白(COL)-Ⅰ等的表达上调[7, 8]。有研究对单侧肾切除的大鼠健侧肾进行辐照,发现辐照能明显抑制肾脏生长及成熟[9],此外,对接受射线照射后的小鼠进行长期观察发现其肾功能进行性下降,并出现肾脏纤维化[10]。
JLP又称JNK相关的亮氨酸拉链蛋白,是连接JNK和P38MAPK信号通路中的一个支架蛋白。研究发现JLP广泛表达于哺乳动物的大脑、卵巢、脾脏、肾脏等器官。本课题组前期研究显示,JLP在B淋巴细胞、树突状细胞(DC)的CD40受体内化过程中发挥重要作用[11, 12]。此外,我们前期研究结果显示,支架蛋白JLP主要表达于小鼠肾脏的肾小管上皮细胞,在肾小球和间质未见明显JLP的表达,JLP可以通过下调TGF-β1发挥抗纤维化效应,证实JLP可能在抑制纤维化方面起保护作用[16]。本课题组前期研究偶然发现辐照可以影响细胞及小鼠肾脏JLP表达的,本研究拟进一步研究辐照对肾小管上皮细胞JLP表达的影响,并探讨JLP在放射性肾损伤中可能的作用机制。
1 材料与方法 1.1 细胞培养人肾小管上皮细胞系(HK-2,武汉大学典型物种保藏中心),培养于含10%胎牛血清的DMEM/F12培养基,并加入100 U/ml青霉素和100 μg/ml链霉素,HK-2细胞置于恒定湿度,温度为37 ℃,5%CO2的培养箱中进行培养,细胞生长融合至80%-90%左右进行传代。
1.2 动物饲养JLP杂合基因(jlp+/-)C57/BL6背景小鼠由日本金泽大学Katsuyi Yoshioka教授馈赠, 小鼠饲养并繁殖于武汉大学动物实验中心,实验所用小鼠均为SPF级别,SPF级实验室每周以有效氯消毒鼠笼一次,木屑及垫料均经高压灭菌消毒,每周更换一次,所用饲料经过60Co照射消毒。野生型(jlp+/+)由jlp+/-小鼠繁殖而得,并经基因鉴定为纯合子。实验用鼠均为8-10周龄,体重16-20 g之间。
1.3 细胞和动物实验设计和干预细胞和小鼠的辐照均在武汉大学人民医院放疗科进行,采用直线加速器(VARIAN 23EX)进行辐照,细胞辐照剂量分为4 Gy和6 Gy两个剂量,放射源距离六孔板液平面100 cm,照射1 min;动物辐照剂量为6 Gy,皮缘距100 cm,照射2 min。
细胞实验分组:① 对照组(非辐照组);② 4 Gy X线干预组;③ 6 Gy X线干预组;每组分别设置4组对照;在辐照后24 h和48 h提取细胞蛋白及RNA。
动物实验分组:① jlp+/+非辐照组(n=10);② jlp+/+辐照组(n=10);辐照后7 d处死小鼠,留取肾皮质进行Western印迹实验以及PAS染色。
1.4 Western印迹收集并提取细胞以及组织蛋白,BSA法测蛋白浓度,配制10%分离胶进行电泳,用微量加样器将制备好的蛋白样品和Marker加入上样孔, 各样品总蛋白量约为40 μg。加样后先恒压80 V电泳至浓缩胶与分离胶交界处,改为恒压120 V至指示剂到凝胶底部。随后进行转膜,转膜条件:GAPDH:200 mA,90 min;JLP:200 mA, 120 min后300 mA, 60 min;α-SMA:200 mA,90 min;TGF-β1:200 mA,90 min,COL-Ⅰ:200 mA, 120 min后300 mA, 30 min。转膜成功后5%脱脂牛奶封闭1 h,TBST洗膜3次,将PVDF膜分别置于抗体稀释液稀释后的一抗中,4 ℃孵育过夜,抗体稀释浓度:兔抗GAPDH抗体(杭州至贤生物有限公司,1:1 000),兔抗JLP抗体(Abcam,1:1 000),兔抗TGF-β1抗体(北京博奥森生物技术有限公司,1:200);兔抗α-SMA抗体(Abcam,1:25 000),兔抗COL-Ⅰ抗体(Abcam,1:7 500)。TBST洗膜3次,随后二抗孵育1 h,TBST洗膜3次,曝光。
1.5 RT-PCR采用Trizol法提取RNA,所用引物由擎科生物合成,以GAPDH作为内参,根据GAPDH和目的基因的特异性序列设计引物,引物序列见表 1。根据设计的引物逆转录合成cDNA,RT-PCR分析目的基因表达水平。
| 表 1 引物序列 |
C57/BL6小鼠麻醉处死后取1/4肾脏置于4%多聚甲醛中固定24 h,石蜡包埋固定肾组织,切成3 μm的切片,石蜡切片依次经二甲苯透明,梯度乙醇脱水,蒸馏水洗2 min,1%过碘酸水溶液浸泡切片10 min,蒸馏水洗2 min脱蜡,滴加Schiff氏试剂于切片组织上,室温避光孵育15-30 min,流水冲洗切片5-10 min,Mayer苏木素复染2 min,自来水冲洗至细胞核变蓝,无水乙醇脱水、二甲苯透明,中性树胶封片后显微镜下观察。
1.7 统计学分析采用SPSS 19.0软件进行统计学分析,所有数据用均数±标准差(x±s)表示,组间比较采用t检验,以P<0.05为差异具有统计学意义。
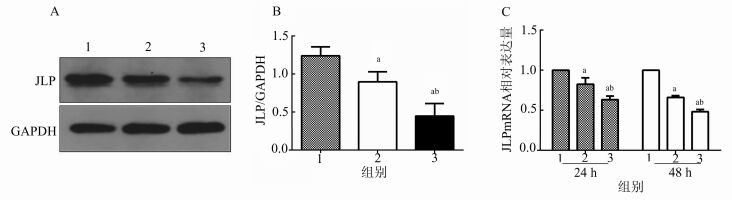
2 结果 2.1 辐照下调JLP的表达不同剂量X线干预HK-2细胞不同时间,Western印迹结果显示,HK-2细胞经不同剂量X线干预后JLP蛋白表达均下调,6 Gy X线干预后JLP蛋白表达明显下调(P<0.05)。实时荧光定量PCR结果显示,4 Gy和6 Gy X线干预HK-2细胞24 h、48 h,JLP mRNA表达均明显下调,在不同干预时间点,6 Gy X线干预组JLP mRNA下调更明显(P<0.05),见图 1。
|
图 1 不同剂量X线干预HK-2细胞后JLP表达改变 1:对照组(无射线干预组);2:4 Gy X线干预组;3:6 Gy X线干预组;A、B:Western印迹法检测不同剂量X线干预后HK-2细胞JLP表达变化,与对照组比较,aP<0.05,与4 Gy X线干预组比较,bP<0.05;C:实时荧光定量PCR检测不同剂量X线干预24 h、48 h,检测JLP mRNA表达,与对照组比较,aP<0.05,与4 Gy X线干预组比较,bP<0.05 |
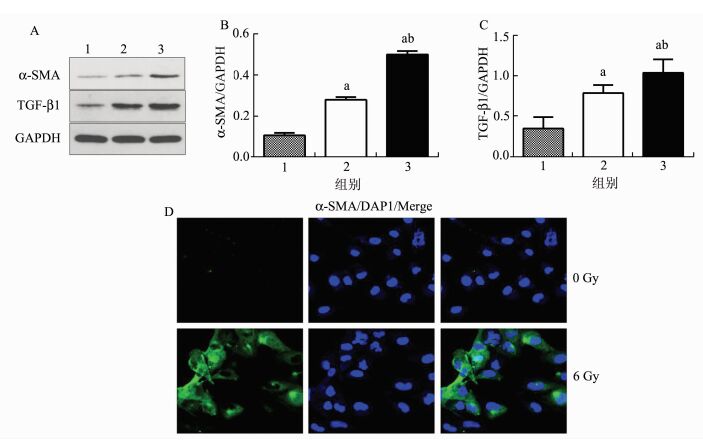
不同剂量X线干预HK-2细胞48 h,Western印迹法检测HK-2细胞TGF-β1和α-SMA表达改变,结果显示,与对照组相比,4 Gy和6 Gy X线干预组TGF-β1和α-SMA蛋白的表达均上调,6 Gy X线干预组TGF-β1和α-SMA蛋白表达明显上调(P<0.05)。免疫荧光观察6 Gy X线干预48 h后α-SMA荧光的表达,结果显示,与对照组比较,6 Gy X线干预组α-SMA表达明显增加,见图 2。接下来实验均采用6 Gy X线干预小鼠。
|
图 2 辐照后各组HK-2细胞TGF-β1和α-SMA表达改变 1:对照组(无射线干预组);2:4 Gy X线干预组;3:6 Gy X线干预组A:Western Blot;B、C:A图的定量分析,与对照组比较,aP<0.05,与4 Gy X线干预组比较,bP<0.05;D:免疫荧光 |
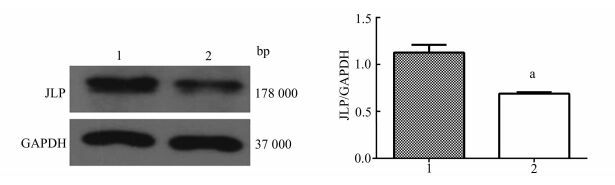
将JLP+/+小鼠分为辐照组和非辐照组,Western印迹结果显示,辐照后JLP蛋白的表达下调(P<0.05)(图 3)。
|
图 3 辐照后肾组织JLP表达变化 1:对照组(非辐照组);2:辐照组;与对照组比较,aP<0.05 |
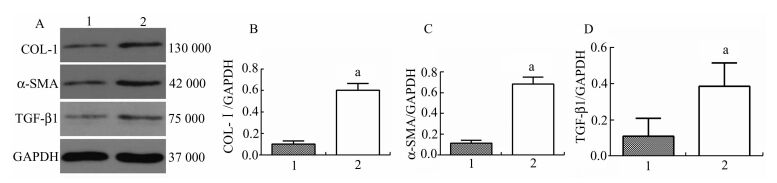
Western印迹结果显示,辐照能够上调小鼠肾脏TGF-β1、α-SMA、COL-Ⅰ的表达(图 4)。
|
图 4 辐照对小鼠肾脏的影响 1:jlp+/+非辐照组;2:jlp+/+辐照组A:Western Blot;B、C、D:A图的定量分析,与对照组(非辐照jlp+/+)比较,aP<0.05 |
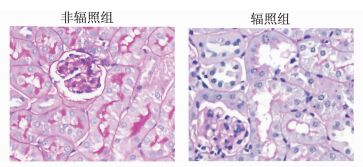
PAS染色观察肾脏病理变化,结果显示,辐照后第7天观察JLP+/+小鼠肾脏可见明显系膜细胞增生,肾小管上皮细胞空泡变性、坏死、脱落和再生(图 5)。
|
图 5 辐射后小鼠病理改变 |
近年来骨髓移植前全身照射预处理以及肿瘤放疗导致放射性肾损伤的发病率逐渐增加。早期放射性肾损伤主要表现为肾小管上皮细胞脱落、坏死、再生,随着病情演变逐渐进展至肾小球硬化、肾小管萎缩、间质纤维化等慢性肾脏病改变,肾小管间质在放射性肾损伤的发病中起重要的作用[10, 13]。
转化生长因子β1(TGF-β1) 是TGF-β超家族的成员之一,主要存在于哺乳动物中。大量研究证实TGF-β1参与肾脏纤维化的发生发展,如诱导肾小管上皮-间质转化(EMT)、内皮间质转化(EnMT)等,促进细胞外基质成分如αSMA,COL-Ⅰ,COL-Ⅲ等表达增加降解减少,进而导致细胞外基质在肾脏的聚集,加重肾脏纤维化[14, 15]。Zhao[7]和Hageman[8]等学者研究发现,辐照可以活化肾小管上皮细胞TGF-β1,并促进一些纤维化相关基因的表达,导致肾小管发生纤维化改变。
我们前期研究发现,支架蛋白JLP主要表达于肾小管上皮细胞,肾脏其他细胞未见明显JLP表达。JLP可以抑制单侧输尿管结扎模型所致肾脏纤维化,主要体现在下调TGF-β1的表达,使细胞外基质产生减少进而发挥保护效应[16]。既往研究也证实TGF-β1参与了放射性肾损伤的发病过程[9],本研究体内外实验结果均显示,辐照可以下调JLP的表达,伴有TGF-β1的活化以及α-SMA表达增加;体外实验结果显示辐照导致肾小管上皮细胞发生空泡变性、坏死、脱落及再生。
综上所述,本研究首次发现射线照射可以下调支架蛋白JLP的表达,同时促进TGF-β1的活化,促进放射性肾损伤的进展。放射性肾损伤中JLP是否同样通过抑制TGF-β1的表达而发挥保护作用有待进一步研究证实。
| [1] | Verma V. Relationship and interactions of curcumin with radiation therapy[J]. World J Clin Oncol, 2016, 7(3): 275-283. DOI: 10.5306/wjco.v7.i3.275. |
| [2] | Shin D, Lee G, Sohn SH, et al. Regulatory T cells contribute to the inhibition of radiation-induced acute lung inflammation via bee venom phospholipase A2 in mice[J]. Toxins (Basel), 2016, 8(5): pii: E131.. DOI: 10.3390/toxins8050131. |
| [3] | Kal HB, van Kempen-Harteveld ML. Renal dysfunction after total body irradiation: dose-effect relationship[J]. Int J Radiat Oncol Biol Phys, 2006, 65(4): 1228-1232. DOI: 10.1016/j.ijrobp.2006.02.021. |
| [4] | Kal HB, van Kempen-Harteveld ML. Induction of severe cataract and late renal dysfunction following total body irradiation: dose-effect relationships[J]. Anticancer Res, 2009, 29(8): 3305-3309. |
| [5] | Lawton CA, Cohen EP, Murray KJ, et al. Long-term results of selective renal shielding in patients undergoing total body irradiation in preparation for bone marrow transplantation[J]. Bone Marrow Transplant, 1997, 20(12): 1069-1074. DOI: 10.1038/sj.bmt.1701022. |
| [6] | Borg M, Hughes T, Horvath N, et al. Renal toxicity after total body irradiation[J]. Int J Radiat Oncol Biol Phys, 2002, 54(4): 1165-1173. DOI: 10.1016/S0360-3016(02)03039-0. |
| [7] | Zhao W, O'Malley Y, Wei S, et al. Irradiation of rat tubule epithelial cells alters the expression of gene products associated with the synthesis and degradation of extracellular matrix[J]. Int J Radiat Biol, 2000, 76(3): 391-402. DOI: 10.1080/095530000138736. |
| [8] | Hageman J, Eggen BJ, Rozema T, et al. Radiation and transforming growth factor-beta cooperate in transcriptional activation of the profibrotic plasminogen activator inhibitor-1 gene[J]. Clin Cancer Res, 2005, 11(16): 5956-5964. DOI: 10.1158/1078-0432.CCR-05-0427. |
| [9] | Donaldson SS, Moskowitz PS, Canty EL, et al. Radiation-induced inhibition of compensatory renal growth in the weanling mouse kidney[J]. Radiology, 1978, 128(2): 491-495. DOI: 10.1148/128.2.491. |
| [10] | Jaggi JS, Seshan SV, McDevitt MR, et al. Renal tubulointerstitial changes after internal irradiation with alpha-particle-emitting actinium daughters[J]. J Am Soc Nephrol, 2005, 16(9): 2677-2689. DOI: 10.1681/ASN.2004110945. |
| [11] | Wang H, Zhao C, Zhang M, et al. A novel role of the scaffolding protein JLP in tuning CD40-induced activation of dendritic cells[J]. Immunobiology, 2013, 218(6): 835-843. DOI: 10.1016/j.imbio.2012.10.002. |
| [12] | Wang HM, Yan Q, Yang T, et al. Scaffold protein JLP is critical for CD40 signaling in B lymphocytes[J]. J Biol Chem, 2015, 290(9): 5256-5266. DOI: 10.1074/jbc.M114.618496. |
| [13] | Robbins ME, O'Malley Y, Zhao W, et al. The role of the tubulointerstitium in radiation-induced renal fibrosis[J]. Radiat Res, 2001, 155(3): 481-489. DOI: 10.1667/0033-7587(2001)155[0481:TROTTI]2.0.CO;2. |
| [14] | Zhao Y, Qiao X, Wang L, et al. Matrix metalloproteinase 9 induces endothelial-mesenchymal transition via Notch activation in human kidney glomerular endothelial cells[J]. BMC Cell Biol, 2016, 17(1): 21. DOI: 10.1186/s12860-016-0101-0. |
| [15] | Hu N, Duan J, Li H, et al. Hydroxysafflor Yellow A ameliorates renal fibrosis by suppressing TGF-beta1-induced epithelial-to-mesenchymal transition[J]. PLoS One, 2016, 11(4): e0153409. DOI: 10.1371/journal.pone.0153409. |
| [16] | Fu Q, Wang HM, Yan Q, et al. Role of scaffolding protein JLP on the progression of renal interstitial fibrosis in mice model of unilateral ureteral obstruction and its underlying mechanism[J]. Chinese Journal of Nephrology, 2016, 32(1): 30-36. |
 2017, Vol. 38
2017, Vol. 38

 ,
,