过敏性鼻炎(allergic rhinitis)又称变态反应性鼻炎,为机体再次接触致敏原后由IgE介导的组胺等介质释放,且伴随多种免疫细胞活化及细胞因子释放的鼻黏膜的慢性反应性疾病[1]。其严重影响患者的工作、学习及生活质量,且可诱发鼻窦炎、支气管哮喘等呼吸道疾病或变应性结膜炎的发生。
目前公认的过敏性鼻炎的发病机制是过敏原诱导的免疫球蛋白(Ig) E抗体与肥大细胞表面的高亲和性IgE受体(FcεRI)结合激活肥大细胞,进而诱发细胞内信号级联反应,同时能够分泌多种炎症细胞因子如肿瘤坏死因子(TNF)-α、白细胞介素(IL)-4和转化生长因子(TGF)-β等,这些炎症细胞因子在过敏性鼻炎中具有重要作用[2]。
丹参酮ⅡA(tanshinone ⅡA, Tan ⅡA)是中药丹参的脂溶性成分之一,具有广泛的生物活性,具有改善微循环、清除氧自由基、抑制血小板聚集和抗血栓形成等作用[3]。大量研究表明,Tan ⅡA在抑制炎症发生方面具有重要作用[4]。所以本研究通过建立小鼠过敏性鼻炎模型及分离小鼠腹腔肥大细胞,研究Tan ⅡA对肥大细胞介导的过敏性鼻炎的影响,并探讨其具体作用机制,为中药治疗过敏性鼻炎提供理论基础。
1 材料与方法 1.1 研究对象C57BL/6(6-14周龄)小鼠购自武汉大学中南医院医学中心,动物按常规饲育。
1.2 主要试剂卵清蛋白(Ovalbumin, OVA)、二硝基苯-人血清白蛋白(DNP-HSA)及抗DNP IgE购自Sigma公司。丹参酮ⅡA购自南京欣奥盛公司。Western Blot相关抗体均购自Ebioscience公司。
1.3 细胞培养肥大细胞RBL-2H3细胞和小鼠腹腔肥大细胞分别培养于DMEM及α-MEM培养基,并置于37 ℃、5%CO2培养箱中进行培养。
1.4 过敏性鼻炎小鼠模型的建立采用腹腔注射联合鼻腔滴注的方法建立过敏性鼻炎小鼠模型。将小鼠随机分为5组(PBS组,OVA混合物组,OVA混合物+Tan ⅡA 2 mg/kg组,OVA混合物+Tan ⅡA 10 mg/kg组,OVA混合物+Tan ⅡA 50 mg/kg组)。在建模第1天、第8天及第15天分别给予各实验组小鼠腹腔注射200 μl OVA混合物(100 μg OVA+2 mg明矾佐剂+200 μl PBS),对照组小鼠注射200 μl超纯水作为阴性对照。在第22天至第29天,用浓度为40 mg/ml的OVA溶液以鼻腔滴注的方法激发实验组小鼠,每只小鼠滴注20 μl,对照组小鼠同样采用超纯水做阴性对照。造模成功后测量小鼠直肠温度,每10 min测一次,共测8次,80 min后从每个小鼠的腹主动脉采集血标本用于血清组胺、总IgE和OVA-特异性IgE水平检测。
1.5 分离小鼠腹腔肥大细胞(RPMCs)处死造模成功的模型小鼠,向其腹腔中注射40 ml Tyrode’s缓冲液,按摩腹部一定时间,用注射器抽取腹腔中的液体。将收集的液体4 000 r/min离心10 min,弃上清,1 ml Tyrode’s缓冲液A重悬细胞,在加入2 ml 0.235 g/ml Histodenz溶液混匀后于室温4 000 r/min离心15 min将细胞进行分层,即将肥大细胞和腹腔中的其他细胞(如巨噬细胞、小淋巴细胞)进行分离。收集Tyrode’s缓冲液A和Histodenz溶液间的细胞层,洗涤后离心,弃上清重悬细胞。甲苯胺蓝染色显色所制备的小鼠腹腔肥大细胞的纯度约95%。台盼蓝颜色显示有超过97%的肥大细胞具有活性[5]。
1.6 血清及细胞培养上清中组胺检测将抗-DNP IgE (100 ng/ml)致敏的小鼠用Tan ⅡA预处理1 h后用DNP-HSA (100 ng/ml)刺激4 h,收集小鼠静脉血于4 ℃ 4 000 r/min离心15 min收集血清。将分离的RPMCs接种于含有anti-DNP IgE (500 ng/mL)的24孔板中(2×104细胞/孔)。24 h后,用PBS洗涤细胞,再用Tan ⅡA预处理1 h,然后再用DNP-HSA (100 ng/ml)刺激30 min,4 ℃ 1 500 r/min离心5 min收集细胞上清。为检测血清和细胞培养上清中的组胺浓度,在血清和细胞培养上清中加入0.1 mol/L HCl和60%高氯酸然后离心,并将上清转移到1.5 ml EP管中,在EP管中加入5 mol/L NaCl, 5 mol/L NaOH和n-丁酸,旋涡混匀后离心。在上清中加入0.1 mol/L HCl和n-haptane充分混匀后再离心。用荧光板阅读器(Molecular Devices)读取440 nm发射波长和380 nm激发波长处的荧光强度。
1.7 细胞内钙离子浓度检测用荧光指示剂Fluo-3/AM测量细胞内钙离子浓度(Invitrogen, Carlsbad, CA, USA)。在37 ℃用Fluo-3/AM (5 μmol/L)预培养细胞1 h后用抗-DNP IgE (100 ng/ml)致敏RBL-2H3细胞,细胞用/不用Tan ⅡA处理1 h后,继续用DNP-HSA (100 ng/ml)对刺激细胞30 min。用荧光阅读器读取485 nm激发波长和510 nm发射波长处的荧光强度。根据读取的荧光强度计算细胞内钙离子浓度。
1.8 定量PCR将分离的RPMCs及RBL-2H3细胞接种于含有anti-DNP IgE (500 ng/ml)的24孔板中(2×104细胞/孔)。24 h后,用PBS洗涤细胞,再用Tan ⅡA预处理1 h,然后再用DNP-HSA (100 ng/ml)刺激30 min,提取肥大细胞总RNA,逆转录后定量测定炎症因子IL-4及TNF-α在转录水平的表达量。
1.9 Western Blot将细胞经上述处理后提取细胞总蛋白,将等量的细胞蛋白用8%-12%的SDS PAGE凝胶进行电泳、转膜、封闭、抗体孵育一系列步骤后用增强型ECL显色液在蛋白呈像仪(Fujifilm luminescent image LAS-1000 analyzer, Fujifilm)中观察蛋白条带。灰度扫描后对蛋白条带进行定量。
1.10 统计学分析数据均以均值±标准差表示。SAS 8.0统计学软件对数据进行统计学分析。Duncan’s multiple range tests方差分析对处理组间的效应进行分析。P<0.05为差异有统计学意义。
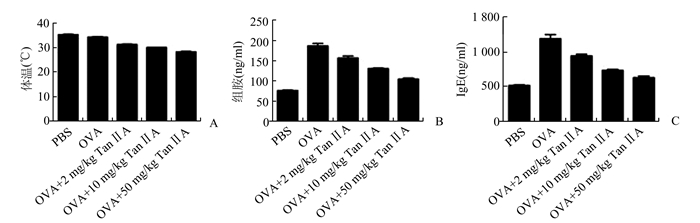
2 结果 2.1 Tan ⅡA对小鼠过敏性鼻炎反应的影响对各组小鼠体温、组胺释放、IgE产生进行测定。结果显示,小鼠单独给予OVA处理后,小鼠体温降低,而在经Tan ⅡA预处理后,小鼠体温发生进一步降低(图 1A)。而对小鼠血清中组胺水平检测发现(图 1B),Tan ⅡA可逆转OVA引起的血清组胺水平上升现象,并具有浓度依赖性。所以猜测小鼠体温降低可能与血清中组胺水平变化有关。此外,小鼠注射OVA后其血清中IgE水平明显上升,而加入Tan ⅡA后,IgE水平随着Tan ⅡA浓度的上升逐渐下降(图 1C)。
|
图 1 Tan ⅡA对小鼠过敏性鼻炎反应的影响 A:体温; B:组胺水平; C: IgE水平 |
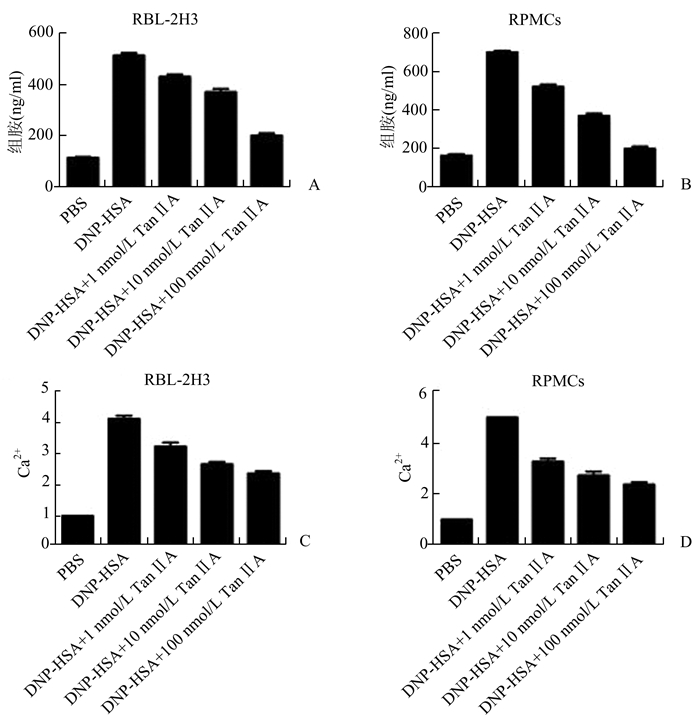
对各组细胞培养上清中组胺的释放水平进行测定,数据显示Tan ⅡA表现出能够显著地降低肥大细胞中组胺的释放量,且在一定程度上显示出剂量依赖性(图 2A, 2B);同样,在对肥大细胞脱颗粒的过程中至关重要钙离子的测定过程中,数据显示Tan ⅡA对细胞钙离子的内流具有一定的抑制作用(图 2C, D)。
|
图 2 Tan ⅡA对小鼠过敏性鼻炎反应的影响 A-B:细胞培养上清中组胺水平;C-D:细胞内钙离子水平 |
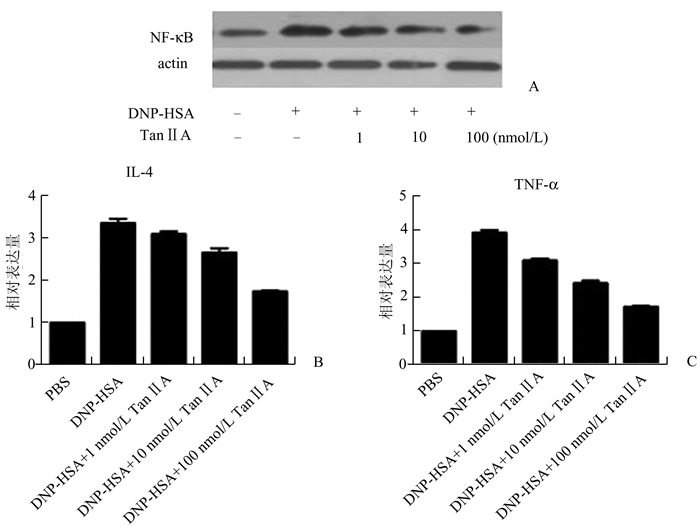
本研究通过测定NF-κB及下游炎症因子的表达量进一步研究Tan ⅡA对NF-κB通路及下游炎症因子的影响。数据显示Tan ⅡA能够通过抑制NF-κB通路的激活(图 3A)并下调下游炎症因子的表达水平(图 3B, C)。
|
图 3 Tan ⅡA对NF-κB通路及下游炎症因子的影响 A:细胞NF-κB的表达;B-C:IL-4及TNF-α的表达 |
过敏性鼻炎即变态反应性鼻炎,是一个发生于各年龄段的全球性健康问题。其是指特异性个体接触变应原后,主要由IgE介导的介质(主要是组胺)释放,并有多种免疫活性细胞和细胞因子等参与的鼻黏膜非感染性炎性疾病[6]。临床治疗常使用的有H1受体阻断剂、糖皮质激素、色酮类、抗胆碱类等药物。而中药单体对过敏性鼻炎的研究相对较少,因此本研究选择了具有消炎、活血化瘀功效的丹参酮作为治疗过敏性鼻炎的研究对象。
Tan ⅡA是中药丹参重要的脂溶性单体成分之一。大量研究表明,Tan ⅡA在抑制炎症发生方面也具有重要作用。因此本研究通过建立小鼠过敏性鼻炎模型,随后给予Tan ⅡA处理后发现,Tan ⅡA能够缓解小鼠过敏性鼻炎反应,其表现为包括体温降低,血清组胺水平及IgE水平。这一结果显示小鼠过敏性鼻炎模型治疗前后体征数据趋势与临床症状比较吻合。
众所周知,肥大细胞所释放的过敏介质、促炎因子及化学物质在过敏性鼻炎的发生中具有重要的作用[7],所以肥大细胞可能是治疗过敏鼻炎的一个潜在靶点。分离小鼠腹腔肥大细胞,探讨Tan ⅡA对介导过敏性鼻炎的肥大细胞脱颗粒效应的影响。结果发现Tan ⅡA能够抑制肥大细胞的脱颗粒效应,减少组胺的释放。以上结果表明Tan ⅡA可能是通过抑制肥大细胞的某一或某些生物学行为达到缓解过敏性鼻炎症状的功效。其具体作用机制还需进一步探究。
过敏性鼻炎作为一种炎性疾病,其发生时必然伴随着参与过敏过程的细胞内炎症通路的激活[8]。而NF-κB及MAPK通路是经典的两条炎症信号通路。炎症发生时,通过激活该信号通路介导下游大量炎症因子的分泌[9, 10]。之前的研究结果表明Tan ⅡA可通过抑制肥大细胞的生物学行为来缓解过敏性鼻炎的症状,但其作用机制并不明确。本研究通过测定NF-κB及下游炎症细胞因子的表达量研究Tan ⅡA对NF-κB通路及下游炎症因子的影响,来探究NF-κB通路是否参与Tan ⅡA抑制肥大细胞生物学行为的作用,结果发现Tan ⅡA可通过抑制NF-κB通路的激活并下调下游炎症因子IL-4及TNF-α的表达。鉴于以上实验数据,Tan ⅡA是如何与肥大细胞发生作用仍需要作进一步的研究,这也将是本课题组下一步将要开展的工作。
综上所述,Tan ⅡA通过调节肥大细胞NF-κB通路达到对肥大细胞介导的过敏性鼻炎的缓解作用,或可为中药治疗过敏性鼻炎提供理论依据。
| [1] | Pablos-Tanarro A, López-Expósito I, Lozano-Ojalvo D, et al. Antibody production, anaphylactic signs, and T-cell responses induced by oral sensitization with ovalbumin in BALB/c and C3H/HeOuJ mice[J]. Allergy Asthma Immunol Res, 2016, 8(3): 239-245. DOI: 10.4168/aair.2016.8.3.239. |
| [2] | Je IG, Choi HG, Kim HH, et al. Inhibitory effect of 1, 2, 4, 5-tetramethoxybenzene on mast cell-mediated allergic inflammation through suppression of IκB kinase complex[J]. Toxicol Appl Pharmacol, 2015, 287(2): 119-127. DOI: 10.1016/j.taap.2015.05.006. |
| [3] | Wan L, Zou Y, Wan LH, et al. Tanshinone ⅡA inhibits the proliferation, migration and invasion of ectopic endometrial stromal cells of adenomyosis via 14-3-3 downregulation[J]. Arch Gynecol Obstet, 2015, 292(6): 1 301-1 309. DOI: 10.1007/s00404-015-3766-2. |
| [4] | Zhu J, Xu Y, Ren G, et al. Tanshinone ⅡA Sodium sulfonate regulates antioxidant system, inflammation, and endothelial dysfunction in atherosclerosis by downregulation of CLIC1[J]. Eur J Pharmacol, 2017, 815: 427-436. DOI: 10.1016/j.ejphar.2017.09.047. |
| [5] | Yoo JM, Yang JH, Kim YS, et al. Inhibitory effects of viscum coloratum extract on IgE/antigen-activated mast cells and mast cell-derived inflammatory mediator-activated chondrocytes[J]. Molecules, 2016, 22(1): pii: E37. DOI: 10.3390/molecules22010037. |
| [6] | Hart PH. Regulation of the inflammatory response in asthma by mast cell products[J]. Immunol Cell Biol, 2001, 79(2): 149-153. DOI: 10.1046/j.1440-1711.2001.00983.x. |
| [7] | Walczak H. TNF and ubiquitin at the crossroads of gene activation, cell death, inflammation, and cancer[J]. Immunol Rev, 2011, 244(1): 9-28. DOI: 10.1111/imr.2011.244.issue-1. |
| [8] | Chen L, Grabowski KA, Xin JP, et al. IL-4 induces differentiation and expansion of Th2 cytokine-producing eosinophils[J]. J Immunol, 2004, 172(4): 2 059--2 066. DOI: 10.4049/jimmunol.172.4.2059. |
| [9] | Je IG, Kim DS, Kim SW, et al. Tyrosol suppresses allergic inflammation by inhibiting the activation of phosphoinositide 3-kinase in mast cells[J]. PLoS One, 2015, 10(6): 0129829. |
| [10] | Fan G, Jiang X, Wu X, et al. Anti-inflammatory activity of tanshinone ⅡA in LPS-stimulated RAW264.7 macrophages via miRNAs and TLR4-NF-κB pathway[J]. Inflammation, 2016, 39(1): 375-384. DOI: 10.1007/s10753-015-0259-1. |
 2018, Vol. 39
2018, Vol. 39

