2. 中山大学药学院临床药理研究所 广东 广州 510080
2. Institute of Clinical Pharmacology, School of Pharmaceutical Sciences, Sun Yat-sen University, Guangzhou 510080, China
细胞色素P450(cytochrome P450, CYPs)酶系统为肝脏Ⅰ相药物代谢酶,是机体代谢的主要酶系统[1]。抗氧化酶能抑制体内氧自由基的产生,平衡人体的代谢,防止由于氧化损伤造成的老化性疾病[2]。CYP同工酶和抗氧化酶系统功能易受到外界不良因素的影响而发生改变。烟雾(尼古丁)是人们日常生活中接触较多的有毒外源物之一,也是孕期不良因素中一个常见和明确的诱因。流行病学调查显示,约16.3%孕妇在妊娠期主动吸烟[3],即使不吸烟也有约50%孕妇处于被动吸烟状态[4]。研究报道,孕期尼古丁暴露(prenatal nicotine exposure, PNE)会影响胎鼠肝脏CYP同工酶某些亚型功能[5-7];外源物暴露所致的机体应激也会对胎儿抗氧化酶系统产生一定影响[8]。然而,对于PNE对子代成年后不同时期肝脏药物代谢酶系统及抗氧化酶系统的影响,目前尚未见报道。
本研究建立PNE模型,选择CYP1、CYP2和CYP3家族几种与药物代谢密切相关的亚型(如CYP1A2、CYP2A2、CYP2B1、CYP2C11、CYP2D2、CYP2E1、CYP3A1)作为CYP同工酶代表,选择谷胱甘肽过氧化物酶(glutathione peroxidase, GSH-Px)、超氧化物歧化酶(superoxide dismutase, SOD)和过氧化氢酶(catalase, CAT)作为抗氧化酶代表,观察雄性子代成年不同时期肝脏CYP同工酶和抗氧化酶的表达及功能变化,为充分认识孕期外源物暴露带来的不良影响,指导孕期不良因素暴露人群成年后个体化用药,提供实验依据。
1 材料与方法 1.1 药品与试剂BCA蛋白定量试剂盒,普利莱公司,中国;GSH-Px、SOD和CAT试剂盒,南京建成生物工程研究所;甲苯磺丁脲(tolbutamide,TOL)、奥美拉唑(omeprazole,OME)、右美沙芬(dextromethorphan,DEXM)、氯唑沙宗(chlorzoxazone,CHL)、硝苯地平(nifedipine,NIF)、对乙酰氨基酚(paracetamol,PAR)、4-羟甲苯磺丁脲(4-hydroxytolbutamide,OHTOL)、氧去甲基右美沙芬(dextrorphan,DEXP)、6-羟基氯唑沙宗(6-hydroxychlorzoxazone,OHCHL)、氧化硝苯地平(dehydronifedipine,DNIF),Sigma公司,美国;5’-羟奥美拉唑(5’-hydroxy omeprazole,OHOME),AstraZeneca公司,瑞典;氯雷他定(loratadine,LOR),中国药品生物制品检定所;NADPH tetrasodiumsalt,AppliChem公司,德国;TRIZOL,Invitrogen,美国;逆转录试剂盒,大连宝生物工程有限公司,中国;引物,上海生工生物工程技术有限公司,中国;RT-PCR试剂盒,Takara公司,日本;其他试剂均为国产分析纯或化学纯。
1.2 动物处理雌性(220-240 g)和雄性(250-280 g) Wistar大鼠由湖北省预防医学科学院实验动物中心提供,许可证号:SCXK (鄂) 2007-2009。大鼠适应性喂养1周后,于每天18:00将雌雄大鼠以2:1的比例合笼,次日清晨用棉签取阴道分泌物镜检,以发现精子为妊娠第0天。按妊娠顺序分为对照组和尼古丁组,于孕9-20 d尼古丁组每天皮下注射尼古丁2 mg/(kg·d)(分2次给予),而对照组皮下注射等体积生理盐水。自然分娩后给予标准饮食,雄性子代大鼠分别于出生后3个月和7个月经异氟烷麻醉处死,摘取肝脏,置于-80 ℃冰箱保存备用。
1.3 RT-PCR检测CYP同工酶mRNA表达取冰冻肝脏组织50 mg,用Trizol试剂抽提,紫外分光光度计测定总RNA的260 nm和280 nm处的光密度值,以OD260/OD280比值检验纯度,调整总RNA浓度至1 μg/μl。逆转录反应按照试剂盒说明书进行。计算CYP1A2、CYP2A2、CYP2B1、CYP2C11、CYP2D2、CYP2E1、CYP3A1与GAPDH相对浓度的比值,作为mRNA表达的相对水平。引物序列见表 1,除CYP2E1和CYP3A1引物序列设计是参照文献[9, 10]外,CYP1A2、CYP2A2、CYP2B1、CYP2C11、CYP2D2及GAPDH引物序列均利用Primer Blast网站自行设计。
| 表 1 实时定量PCR的引物序列 |
分别取3月龄及7月龄雄性仔鼠肝脏组织于冰冻生理盐水中剪碎,漂洗,吸干并称重,放入匀浆缓冲液(0.05 mol/L Tris-HCl, 1.15% KCl, pH 7.4)中制成25%匀浆液。4 ℃离心(200 g, 10 min),取上清液,4 ℃高速离心(9 000 g, 20 min),取上清液,加入匀浆缓冲液平衡,4 ℃超速离心(105 000 g, 60 min),刮起离心后的沉淀物,于0.25 mol/L蔗糖溶液中重悬,BCA法蛋白定量后分装,-80 ℃冰箱保存备用。
选取TOL、OME、DEXM、CHL、NIF分别为CYP2C6、CYP2C11、CYP2D2/3、CYP2E1和CYP3A1的特异性底物,孵育体系及孵育时间参照文献方法[11]。代谢产物分别为OHTOL、OHOME、DEXP、OHCHL、DNIF。参照文献方法[11],正离子检测时流动相为甲醇:水(含0.1%甲酸)=70:30,分析时间为2.1 min;负离子检测时流动相为甲醇:水(含0.1%甲酸)=90:10,分析时间为1.6 min。柱温均为室温,流速为300 μl/min。
1.5 抗氧化酶活性检测将上述25%肝匀浆液,经4 ℃超速离心(105 000 g, 60 min)后,上清即胞质,BCA法蛋白定量,按照GSH-Px、SOD及CAT活性测定试剂盒说明书步骤操作,分别计算GSH-Px、SOD及CAT的活性。
1.6 统计学分析实验结果均以x±s表示,按SPSS 11.0软件包进行统计分析,两组间比较采用t检验。
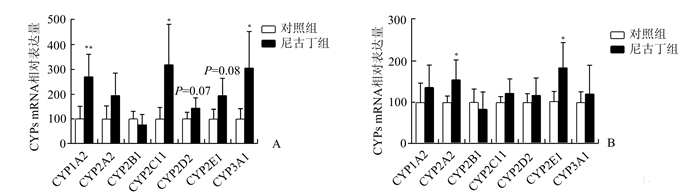
2 结果 2.1 不同时期肝脏CYP同工酶mRNA表达的变化结果表明(图 1A),PNE 3月龄成年雄性子代大鼠肝脏CYP1A2、CYP2C11和CYP3A1的mRNA表达较对照组有显著增加,分别为对照组的271%、319%和307%(P<0.05,P<0.01);CYP2A2、CYP2D2和CYP2E1的mRNA表达有增加趋势,分别为对照组的196%、144%和194%;CYP2B1的mRNA表达有降低趋势,为对照组的77%。进一步,与对照组相比,PNE的7月龄成年雄性子代肝脏CYP2A2和CYP2E1的mRNA表达有显著增加,分别为对照组的155%和180%(P<0.05);CYP1A2、CYP2C11、CYP2D2和CYP3A1的mRNA表达有增加趋势,分别为对照组的137%、122%、117%和121%;CYP2B1的mRNA表达量有降低趋势,为对照组的84%(图 1B)。
|
图 1 孕期尼古丁暴露[2 mg/(kg·5d)]对3月龄(A)及7月龄(B)成年雄性子代大鼠肝脏CYP1A2、CYP2A2、CYP2B1、CYP2C11、CYP2D2、CYP2E1和CYP3A1的mRNA表达的影响 x±s, n=5,与对照组相比,*P<0.05, **P<0.01 |
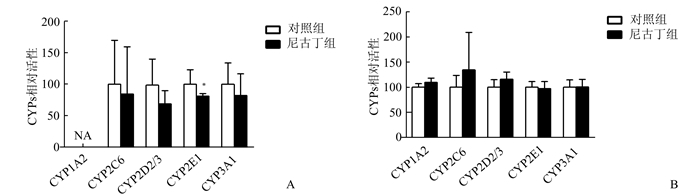
结果表明(图 2A),PNE的3月龄成年雄性子代大鼠CYP2E1活性显著降低,为对照组的81%(P<0.05);除CYP1A2酶活性未检测出外,CYP2C6、CYP2D2/3和CYP3A1酶活性均为降低趋势,分别为对照组的85%、89%、71%和82%。进一步发现,PNE 7月龄成年雄性子代大鼠肝脏CYP1A2、CYP2C6和CYP2D2/3的活性较对照组有升高趋势,分别为对照组的110%、135%、116%;CYP3A1和CYP2E1的活性无明显变化(图 2B)。
|
图 2 孕期尼古丁暴露[2 mg/(kg·5d)]对3月龄(A)及7月龄(B)成年雄性子代大鼠肝脏CYP1A2、CYP2C6、CYP2D2/3、CYP2E1和CYP3A1活性的影响 x±s, n=5, 与对照组相比,*P<0.05 |
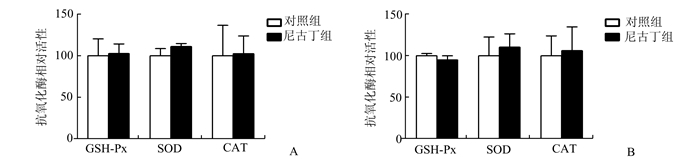
结果表明(图 3),与各自对照组相比,PNE 3月龄和7月龄组的肝脏GSH-Px、SOD和CAT活性几乎无变化。
|
图 3 孕期尼古丁暴露[2 mg/(kg·5d)]对3月龄(A)及7月龄(B)雄性成年子代大鼠肝脏GSH-Px、SOD和CAT活性的影响 x±s, n=5 |
已知尼古丁是CYP同工酶的诱导剂或抑制剂,能诱导CYP1A1、CYP1A2和CYP1B1的活性或mRNA表达,抑制CYP3A的mRNA及蛋白表达[5-7]。孕妇是特殊易感人群,妊娠期尼古丁暴露对胎儿药物代谢酶功能亦有影响。研究发现,尼古丁能诱导孕鼠胎盘及胎鼠CYP1A、CYP2B亚型的表达[12-14]。宫内不良环境对子代CYP功能的影响可延续至出生后[15],有些甚至可持续至成年[16]。然而,PNE对子代药物代谢酶的影响是否能延续至成年尚无报道。
Fowden提出,不良的宫内环境可减慢胎儿的生长速度,以确保胎儿出生后在营养物质缺乏的情况下能生存,但胎儿出生后在营养充足状态下会出现“追赶式”生长[17]。本研究结果表明,PNE可导致3月龄雄性子代肝脏CYP同工酶多种亚型(如CYP1A2、CYP2A2、CYP2C11、CYP2D2、CYP2D3、CYP2E1和CYP3A1)的mRNA表达增加或呈增加趋势,其中,少数亚型(如CYP2A2和CYP2E1)的表达增加,甚至可持续到出生后7月龄。该结果与孕期蛋白饮食限制子代成年后CYP亚型mRNA表达增加[16]是一致的,提示孕期宫内不良环境的子代出生后肝脏代谢酶也同样存在代偿性表达增加。
已知多种CYP亚型在药物及外源物代谢中均有极为重要的作用,酶活性的降低会导致其成年后药物代谢功能下降,可能造成药物毒性反应或环境毒性物质蓄积等不良后果。在本研究中,我们发现,多个CYP同工酶(如CYP2D2/3、CYP2E1和CYP3A1)的活性在3月龄雄性子代肝脏呈降低趋势,然而7月龄时酶活性几无变化,CYP2C6和CYP2D2/3有升高趋势。提示PNE的雄性子代大鼠成年初期,肝脏药物代谢酶功能仍受到宫内不良环境影响,而在正常营养状态下随着年龄的增长,肝脏药物代谢酶活性经代偿趋于正常甚至有升高趋势。有趣的是,本研究中药物代谢酶的mRNA表达与活性不一致现象,可能与转录后调控和无效翻译相关[18]。而关于这一现象的机制,今后还将开展进一步的研究。
已知机体受到应激(如外源物暴露、缺氧等)时,抗氧化酶表达及活性容易受影响而发生改变。孕晚期地塞米松暴露的狨猴,其胎鼠主动脉中一些抗氧化酶指标的mRNA表达显著增加[19];PNE可显著降低胎鼠肝脏SOD活性[20]。本研究结果显示,PNE后无论3月龄还是7月龄雄性子代,其肝脏抗氧化酶GSH-Px、SOD和CAT的活性均无明显变化。提示PNE对子代成年后抗氧化酶几无影响。
| [1] | 郭喻, 汪晖. 人细胞色素P450同工酶探针底物特异性的研究进展[J]. 中国药理学通报, 2007, 23(7): 851-854. |
| [2] | 甘璐, 刘琼, 徐辉碧. 硒对大鼠肝脏抗氧化酶活性及基因表达的影响[J]. 中国公共卫生, 2003, 19(2): 159-160. |
| [3] | Himes SK, Stroud LR, Scheidweiler KB, et al. Tobacco Exposure, Biomarkers for Tobacco in Meconium, and Neonatal Growth Outcomes[J]. J Pediatr, 2013, 162(5): 970-975. DOI: 10.1016/j.jpeds.2012.10.045. |
| [4] | Azab M, Khabour OF, Alzoubi KH, et al. Exposure of pregnant women to waterpipe and cigarette smoke[J]. Nicotine Tob Res, 2013, 15(1): 231-237. DOI: 10.1093/ntr/nts119. |
| [5] | Czekaj P, Wiaderkiewicz A, Florek E, et al. Tobacco smoke-dependent changes in cytochrome P450 1A1, 1A2, and 2E1 protein expressions in fetuses, newborns, pregnant rats, and human placenta[J]. Arch Toxicol, 2005, 79(1): 13-24. DOI: 10.1007/s00204-004-0607-7. |
| [6] | Yan YE, Wang H, Feng YH. Alterations of placental cytochrome P450 1A1 and P-glycoprotein in tobacco-induced intrauterine growth retardation in rats[J]. Acta Pharmacol Sin, 2005, 26(11): 1387-1394. DOI: 10.1111/aphs.2005.26.issue-11. |
| [7] | Czekaj P, Wiaderkiewicz A, Florek E, et al. Expression of cytochrome CYP2B1/2 in nonpregnant, pregnantand fetal rats exposed to tobacco smoke[J]. Acta Biochim Pol, 2000, 47(4): 1115-1127. |
| [8] | Atanasova S, Wieland E, Schlumbohm C, et al. Prenatal dexamethasone exposure in the common marmoset monkey enhances gene expression of antioxidant enzymes in the aorta of adult offspring[J]. Stress, 2009, 12(3): 215-224. DOI: 10.1080/10253890802305075. |
| [9] | Wang T, Chen M, Yan YE, et al. Growth retardation of fetal rats exposed to nicotine in utero: possible involvement of CYP1A1, CYP2E1, and P-glycoprotein[J]. Environ Toxicol, 2009, 24(1): 33-42. DOI: 10.1002/tox.v24:1. |
| [10] | Glöckner R, Steinmetzer P, Lupp A, et al. In vitro induction of cytochrome P450 2B1-and 3A1-mRNA and enzyme immunostaining in cryopreserved precision-cut rat liver slices[J]. Toxicology, 2002, 176(3): 187-193. DOI: 10.1016/S0300-483X(02)00136-1. |
| [11] | He F, Bi HC, Xie ZY, et al. Rapid determination of six metabolites from multiplecytochrome P450 probe substrates in human livermicrosome by liquid chromatography/massspectrometry: application to high-throughput inhibition screening of terpenoids[J]. Rapid Commun Mass Spectrom, 2007, 21(5): 635-643. DOI: 10.1002/(ISSN)1097-0231. |
| [12] | Chang JT, Chang H, Chen PH, et al. Requirement of aryl hydrocarbon receptor overexpression for CYP1B1 up-regulation and cell growth in human lung adenocarcinoma[J]. Clin Cancer Res, 2007, 13(1): 38-45. DOI: 10.1158/1078-0432.CCR-06-1166. |
| [13] | Anttila S, Vainio H, Hietanen E, et al. Immunohistochemical detection of pulmonary cytochrome P4501A and metabolic activities associated with P4501A1 and P4501A2 isozymes in lung cancer patients[J]. Environ Health Perspect, 1992, 98: 179-182. DOI: 10.1289/ehp.9298179. |
| [14] | Piipari R, Savela K, Nurminen T, et al. Expression of CYP1A1, CYP1B1 and CYP3A, and polycyclic aromatic hydrocarbon-DNA adduct formation in bronchoalveolar macrophages of smokers and non-smokers[J]. Int J Cancer, 2000, 86(5): 610-616. DOI: 10.1002/(ISSN)1097-0215. |
| [15] | Wu J, Ramesh A, Nayyar T, et al. Assessment of metabolites and AhR and CYP1A1 mRNA expression subsequent to prenatal exposure to inhaled benzo (a) pyrene[J]. Int J Dev Neurosci, 2003(21): 333-346. |
| [16] | Sohi G, Barry EJ, Velenosi TJ, et al. Protein restoration in low-birth-weight rat offspring derived from maternal low-protein diet leads to elevated hepatic CYP3A and CYP2C11 activity in adulthood[J]. Drug Metab Dispos, 2014, 42(2): 221-228. |
| [17] | Fowden AL, Li J, Forhead AJ. Glucocorticoids and the preparation for life after birth: are there long-term consequences of the life insurance?[J]. Proc Nutr Soc, 1998, 57(1): 113-122. DOI: 10.1079/PNS19980017. |
| [18] | Kocarek TA, Zangar RC, Novak RF. Post-transcriptional Regulation of Rat CYP2E1 Expression: Role of CYP2E1 mRNA Untranslated Regions in Control of Translational Efficiency and Message Stability?[J]. Arch Biochem Biophys, 2000, 376(1): 180-190. DOI: 10.1006/abbi.2000.1704. |
| [19] | Nakayama H, Okuda H, Nakashima T, et al. Nicotine metabolism by rathepatic cytochrome P450s, 1993, 45(12):2 554-2 556. |
| [20] | Sheng HP, Yuen ST, So HL, et al. Hepatotoxicity of prenatal and postnatal exposure to nicotine in rat pups[J]. Exp Biol Med, 2001, 226(10): 934-939. |
 2016, Vol. 37
2016, Vol. 37

