2. 武汉大学中南医院心血管内科 湖北 武汉 430071
Behavior of Cervical Cancer SiHa Cells
2. Dept. of Cardiovescular Medicine, Zhongnan Hospital of Wuhan University, Wuhan 430071, China
宫颈癌是女性生殖系统最常见的恶性肿瘤之一。据2015年中国癌症数据统计,我国宫颈癌的发病率有逐年上升的趋势,其致死率在女性肿瘤中高居第二[1],严重危害着女性的健康,因此深入研究宫颈癌的分子机制对宫颈癌的临床诊断与治疗具有重要的意义。microRNA是一类长度约22个碱基的非编码RNA,它可以通过与靶基因的3′UTR互补结合使靶基因失活或者降解,从而对靶基因进行转录后调控[2],microRNA的功能与肿瘤的发生发展有密切的关系[3]。miR-214定位于1号染色体,由Dicer酶将其环状前体剪切形成hsa-miR-214-3p以及hsa-miR-214-5p,其中hsa-miR-214-3p呈高表达。已有研究证实,hsa-miR-214-3p在乳腺癌[4]、鼻咽癌[5]、骨肉瘤[6]等细胞中呈高表达并能促进细胞的增殖、侵袭,加速癌症发展进程,但在宫颈癌中少见报道。本研究通过hsa-miR-214-3p对宫颈癌SiHa细胞增殖、凋亡等生物学行为的影响,并进一步探讨宫颈癌细胞凋亡的分子机制,为宫颈癌的分子机制的研究提供了新的思路。
1 材料与方法 1.1 主要试剂胎牛血清DMEM培养基购自美国HyClone公司,TRIzol试剂购自于天根生化科技 (北京) 有限公司,RIPA裂解液及脂质体Zlip2000购自于北京庄盟国际生物基因科技有限公司,cDNA合成试剂盒购自于美国Thermo有限公司,PCR引物均由上海生工有限公司合成,实时荧光定量PCR试剂盒购自北京全式金生物 (TransGene Biotech),hsa-miR214 mimics/inhibitor, microRNA mimics NC/inhibitor NC由苏州吉玛基因有限公司合成,ECL显影液购自于碧云天生物技术研究所,BCA蛋白质定量检测试剂盒及细胞凋亡检测试剂盒购自于上海贝博生物公司,DMSO与MTT购自于美国Sigma公司,Bcl2、β-catenin鼠抗人单克隆抗体及辣根过氧化物酶 (HRP) 标记的羊抗鼠IgG抗体均购自于Promotor公司。
1.2 细胞及细胞培养人宫颈癌麟状上皮SiHa细胞由本实验室保存,用含有10%胎牛血清的高糖DMEM培养液,置于37 ℃恒温、CO2体积分数为5%及饱和湿度的培养箱中培养。
1.3 实时荧光定量PCR检测细胞中hsa-miR-214-3p的表达水平用TRIzol试剂分别提取各组细胞的总RNA后,使用NanoDrop2000C微量分光光度计 (美国Thermo公司) 检测RNA的浓度和纯度,纯度以A280/A260在1.80-2.0之间为合格。采用cDNA合成试剂盒分别将各组RNA逆转录制备成hsa-miR-214-3p和内参照U6的cDNA。hsa-miR-214-3p的逆转录引物序列5′-GTCGTATCCAGTGCAGGGTCCGAGGTATTCGCACTGGATACGACACTGCC-3′,U6的逆转录序列为:5′-GTCGTATCCAGTGCAGGGTCCGAGGTATTCGCACTGGATACGACAAAAATATG-3′。逆转录反应条件:16 ℃ 30 min;30 ℃ 30 s、42 ℃ 30 s、50℃ 1 s,共60个循环;85 ℃ 5 min。采用实时荧光定量PCR试剂盒进行PCR扩增,hsa-miR-214-3p的上游引物序列为:5′-CGCCGACAGCAGGCACA-3′,下游引物序列为:5′-GTGCAGGGTCCGAGGT-3′;U6的上游引物序列为:5′-GCGCGTCGTGAAGCGTTC-3′,下游引物序列为:5′-GTGCAGGGTCCGAGGT-3′。实时荧光定量PCR反应条件:95 ℃预变性3 min;95 ℃ 10 s、57 ℃ 1 min,共45个循环。以2-△△Ct法表示hsa-miR-214-3p的相对表达水平。
1.4 hsa-miR-214-3p mimics/inhibitor转染SiHa细胞转染前1 d,将处于对数生长期的SiHa细胞接种于6孔板中 (4×105个/孔),待细胞丰度达到30%-50%时,按Zlip2000说明书提供的方法将hsa-miR-214-3p mimis、mimics NC、hsa-miR-214-3p inhibitor、inhibitor NC分别转染细胞,hsa-miR-214-3p mimics及mimic NC的终浓度为80 nmol/L,hsa-miR-214-3p inhibitor及inhibitor NC的终浓度为160 nmol/L。
1.5 MTT实验检测细胞的增殖能力转染前24 h将SiHa细胞制备成1×104个/ml的细胞悬液,接种于96板中 (100 μl/孔),分4组,每组6个复孔。转染按照1.4描述的方法和分组进行。转染72 h后,加入MTT试剂 (5 mg/ml)10 μl/孔,继续培养3-4 h,弃去培养液,每孔加入DMSO试剂150 μl,脱色摇床上室温震荡15 min,用酶联免疫检测仪测定570 nm下各孔的吸光度值,吸光度值在0.2-0.8之间为合格。
1.6 克隆形成实验按照1.4描述的方法进行细胞铺板和转染。转染24 h后,分别将各组细胞消化计数,最后制备成200个/ml的细胞悬液,接种于6孔板中,分两组,每组3个复孔,每个复孔加入1 ml细胞悬液,常规培养2周后,待肉眼可见细胞集团后终止培养。4%多聚甲醛PBS溶液固定细胞30 min后,使用0.1%结晶紫染色30 min,PBS洗去多余的染液,显微镜下分别计数每组>50个细胞的克隆数。
1.7 细胞迁移实验按1.4的分组和方法转染SiHa细胞24 h后,对每组细胞进行计数,用无血清DMEM培养基将各组细胞配成1×105个/ml的细胞悬液,按1.4的分组分为4组,每组2个复孔,每个transwell小室加入200 μl细胞悬液;下室每孔加入600 μl含10%胎牛血清的DMEM培养基,常规培养24 h后,4%多聚甲醛PBS溶液固定细胞30 min,再用0.1%结晶紫染色30 min,PBS洗去多余的染液,在倒置显微镜下 (×100) 随机选取5个视野,进行拍照并计数穿过小室的细胞数量。
1.8 流式细胞仪检测细胞凋亡按照1.3描述的方法和分组进行转染。转染24 h后,按照广州贝博公司Annexin-FITC/PI细胞凋亡检测试剂盒说明书收集并进行细胞染色,染色后使用BD FACSAria Ⅲ流式细胞分选仪立即进行检测。
1.9 Western Blot检测相关蛋白质的表达按照1.3描述的方法和分组进行转染,48 h后提取细胞总蛋白,采用BCA蛋白定量检测试剂盒检测蛋白浓度,取20×10-6 g进行12%SDS-PAGE电泳,并转移至NC膜,室温下用5%脱脂奶粉封闭3-4 h。TBS缓冲液洗涤10 min,加入鼠抗人Bcl2单克隆一抗 (1:1 000),置于4 ℃脱色摇床孵育过夜,二抗为辣根过氧化物酶标记的羊抗鼠抗体 (1:5 000),4℃脱色摇床孵育1.5-2 h。然后用ECL显影液进行显色反应。用β-catenin内参条带对数值进行标准化处理。
1.10 hsa-miR-214-3p靶基因的预测以及富集通路分析使用Targetscan Human7.1 (http://www.targetscan.org/vert_71/)、Pictar (http://pictar.mdc berlin.de/)、miRanda (http://www.microrna.org/microrna/home.do) 三种靶基因预测软件分别预测hsa-miR-214-3p的靶基因,用Draw Venn Diagram (http://bioinformatics.psb.ugent.be/webtools /Venn/) 取三种预测结果的交集,并结合miRTarBase (http://mirtarbase.mbc.nctu.edu.tw/) 中至少用三种方法确定的靶基因,采用DAVID (https://david.ncifcrf.gov/) 对靶基因进行KEGG富集通路分析[7]。
1.11 统计学分析统计学分析采用SPSS 16.0软件。实验数据用x±s表示,两组间均数比较采用配对t检验,P<0.05为差异有统计学意义。
2 结果 2.1 宫颈癌细胞SiHa、CaSki、C33A中hsa-miR-214-3p呈高表达分别提取人胚肾细胞293T以及SiHa、CaSki、C33A三种宫颈癌细胞 (SiHa、CaSki为HPV16型阳性,C33A为HPV阴性) 的总RNA,进行实时荧光定量PCR检测各组细胞中hsa-miR-214-3p的表达水平。结果 (图 1) 显示,相对于293T细胞,宫颈癌细胞SiHa、CaSki、C33A中hsa-miR-214-3p均呈高表达 (P<0.01)。
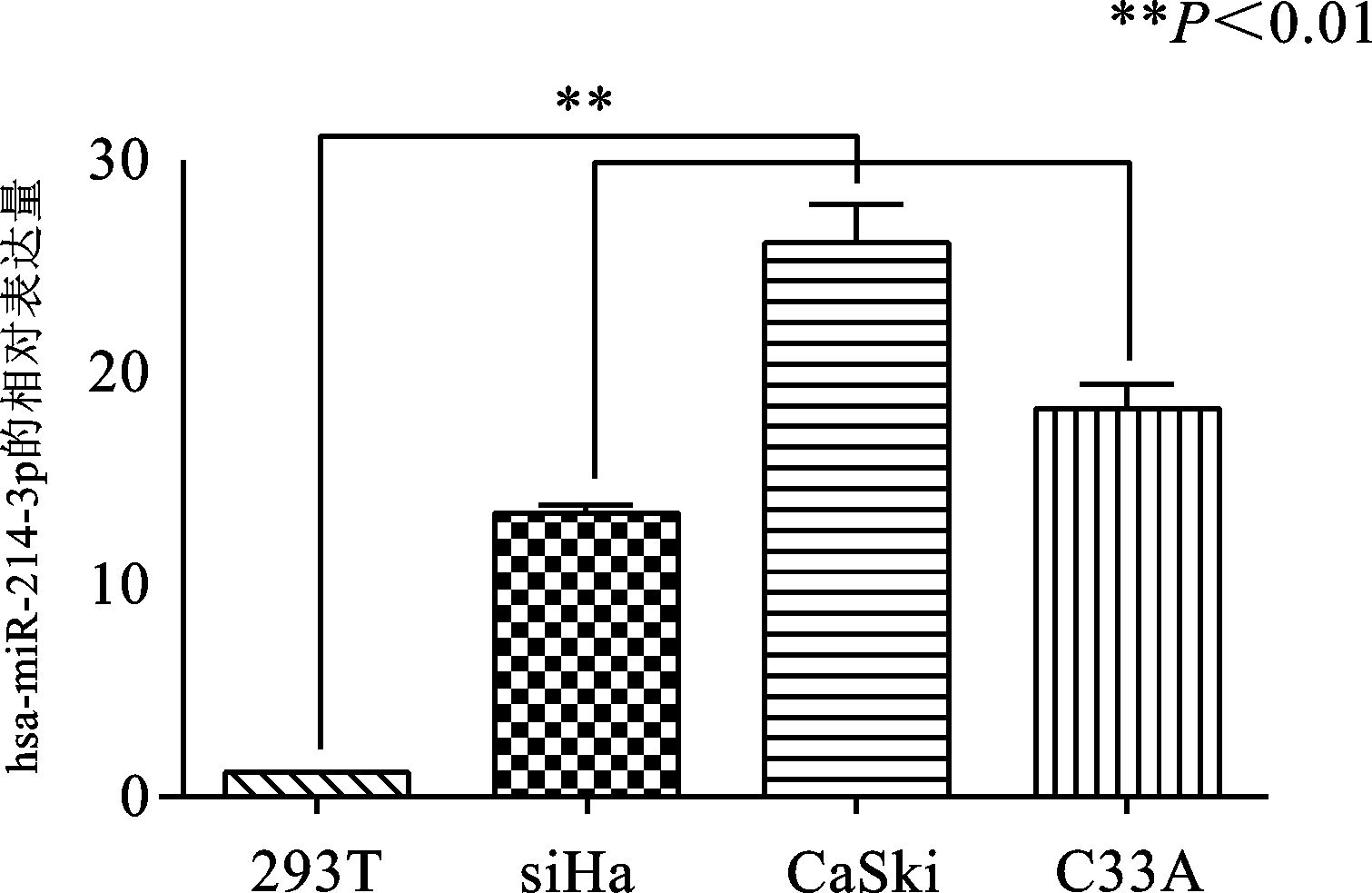
|
图 1 宫颈癌细胞SiHa、CaSki、C33A中hsa-miR-214-3p的表达水平 |
转染后24 h,提取各组总RNA,进行实时荧光定量PCR检测各组hsa-miR-214-3p的表达情况。结果 (图 2) 显示,过表达hsa-miR-214-3p后相对于mimics NC组hsa-miR-214-3p的表达明显上升 (P<0.05),而转染hsa-miR-214-3p抑制剂后与其阴性对照组相比hsa-miR-214-3p的表达显著下降 (P<0.001)。
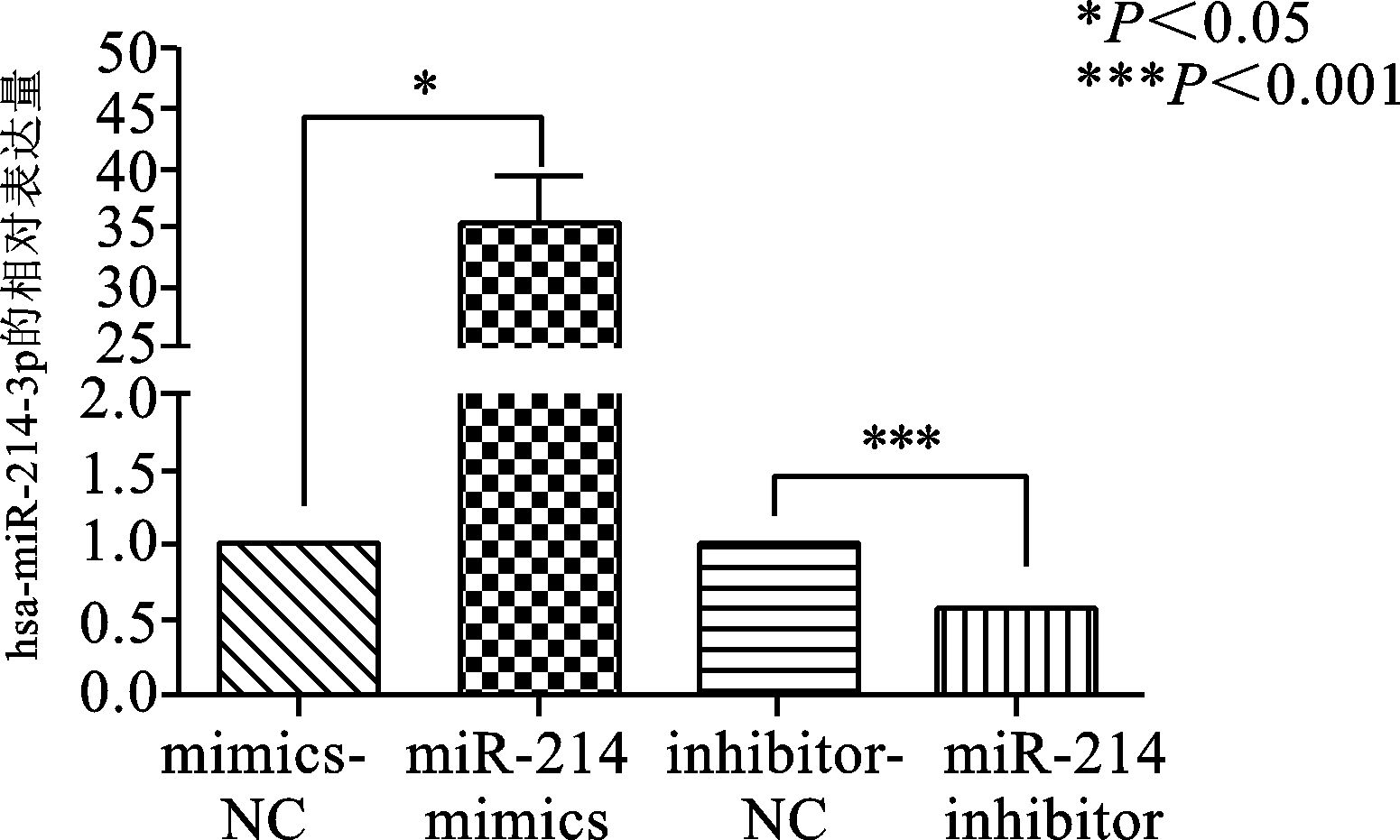
|
图 2 转染后各组hsa-miR-214-3p的表达情况 |
hsa-miR-214-3p mimics/mimics NC及hsa-miR-214-3p inhibitor/inhibitor NC转染SiHa细胞后应用MTT及克隆形成实验检测SiHa细胞增殖能力的变化。结果 (图 3、图 4) 显示,过表达hsa-miR-214-3p后相较于阴性对照组SiHa细胞的增殖及克隆形成能力显著增强 (P均<0.05);而抑制hsa-miR-214-3p内源性表达之后,SiHa细胞的增殖能力显著减弱 (P<0.001)。
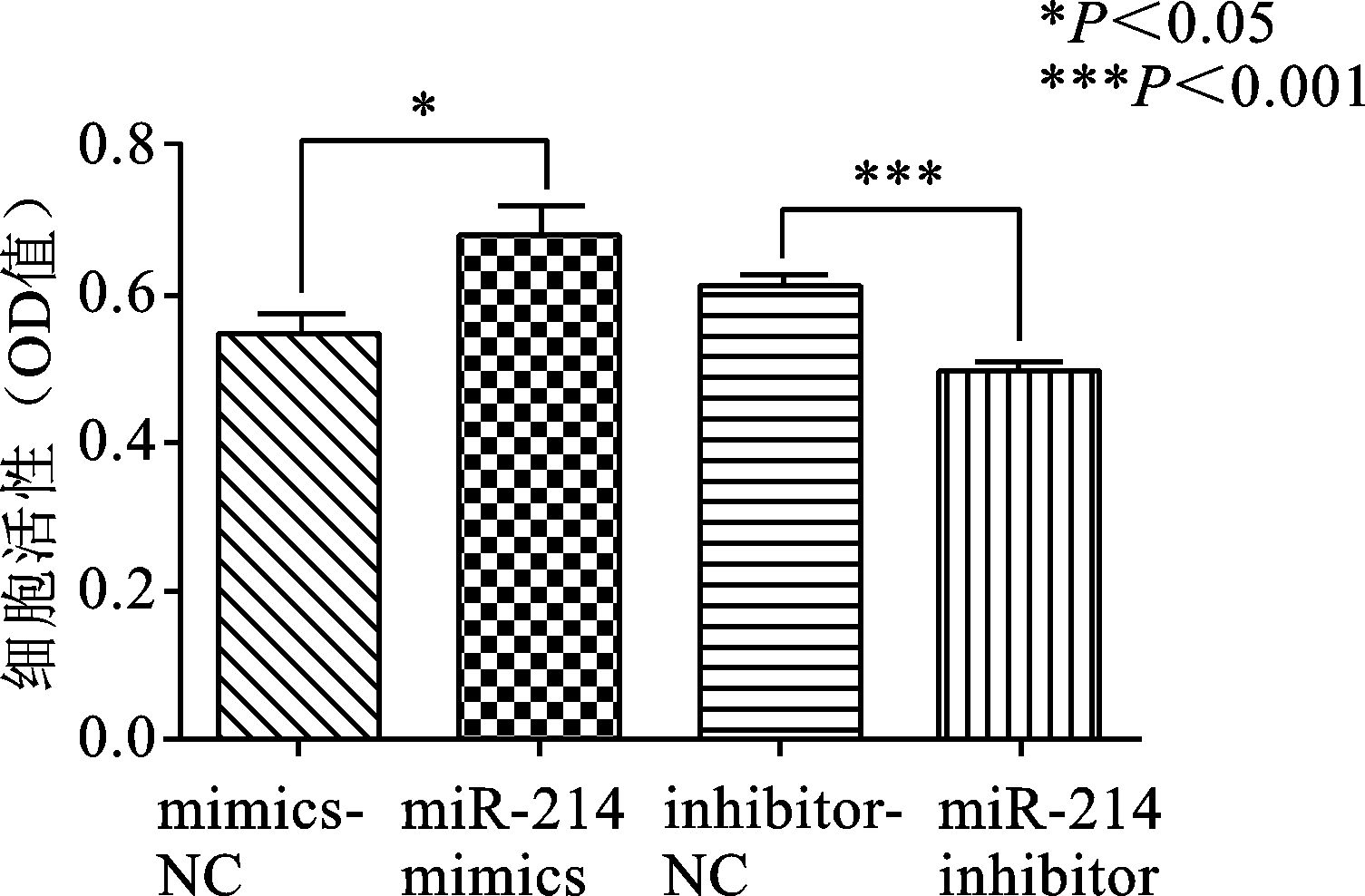
|
图 3 MTT法检测转染后各组细胞增殖活性 |
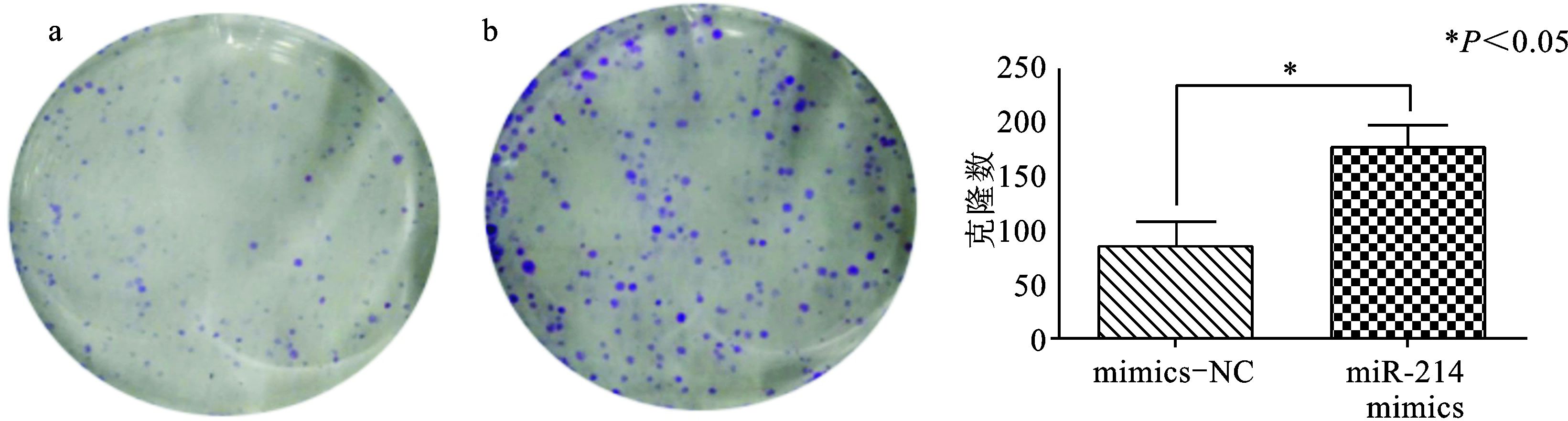
|
图 4 过表达hsa-miR-214-3p后SiHa细胞克隆形成能力的变化 a:mimics NC; b:miR-214 mimics |
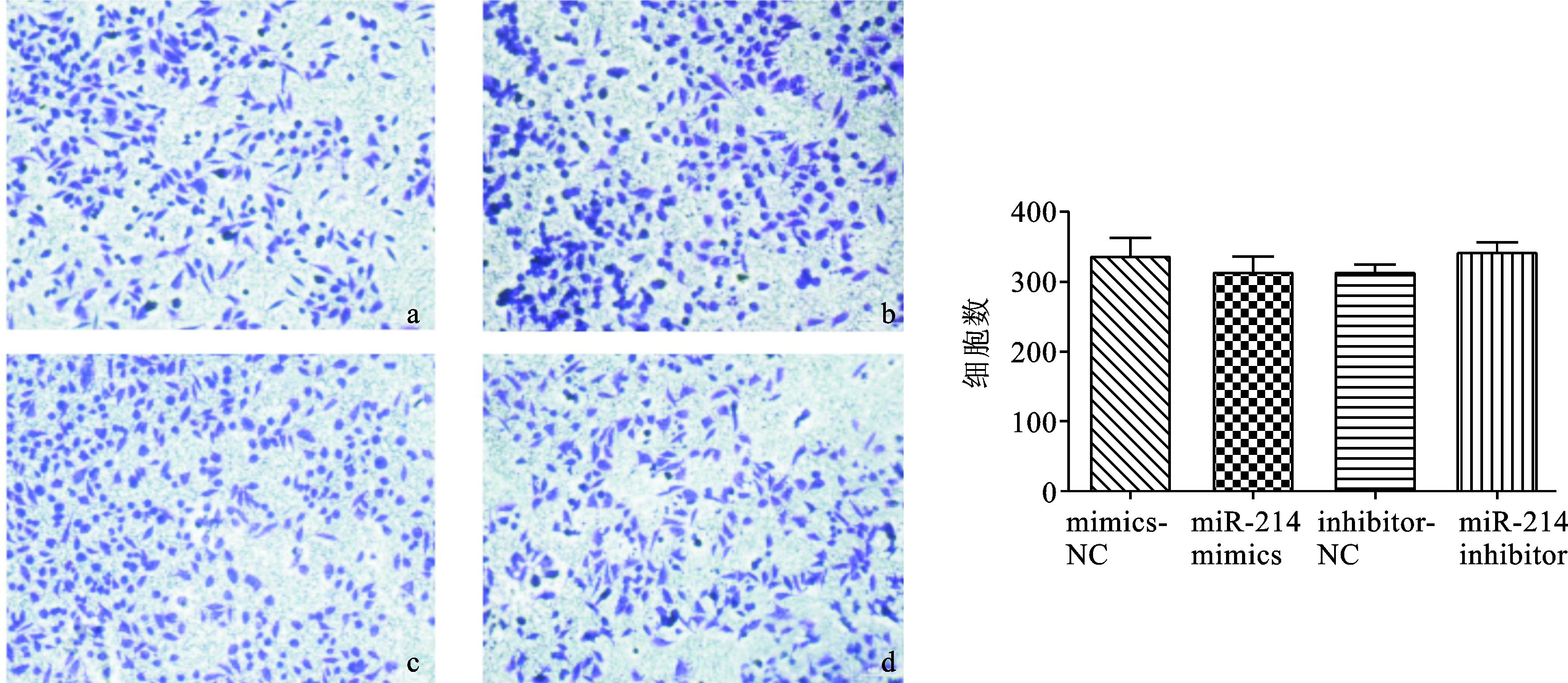
细胞迁移试验结果 (图 5) 显示,无论是过表达hsa-miR-214-3p还是下调内源性hsa-miR-214-3p的表达,细胞迁移都没有明显的变化 (P>0.05)。
|
图 5 转染后各组细胞迁移结果 (×100) a:mimics NC; b:miR-214 mimics; c:inhibitor NC; d:miR-214 inhibitor |
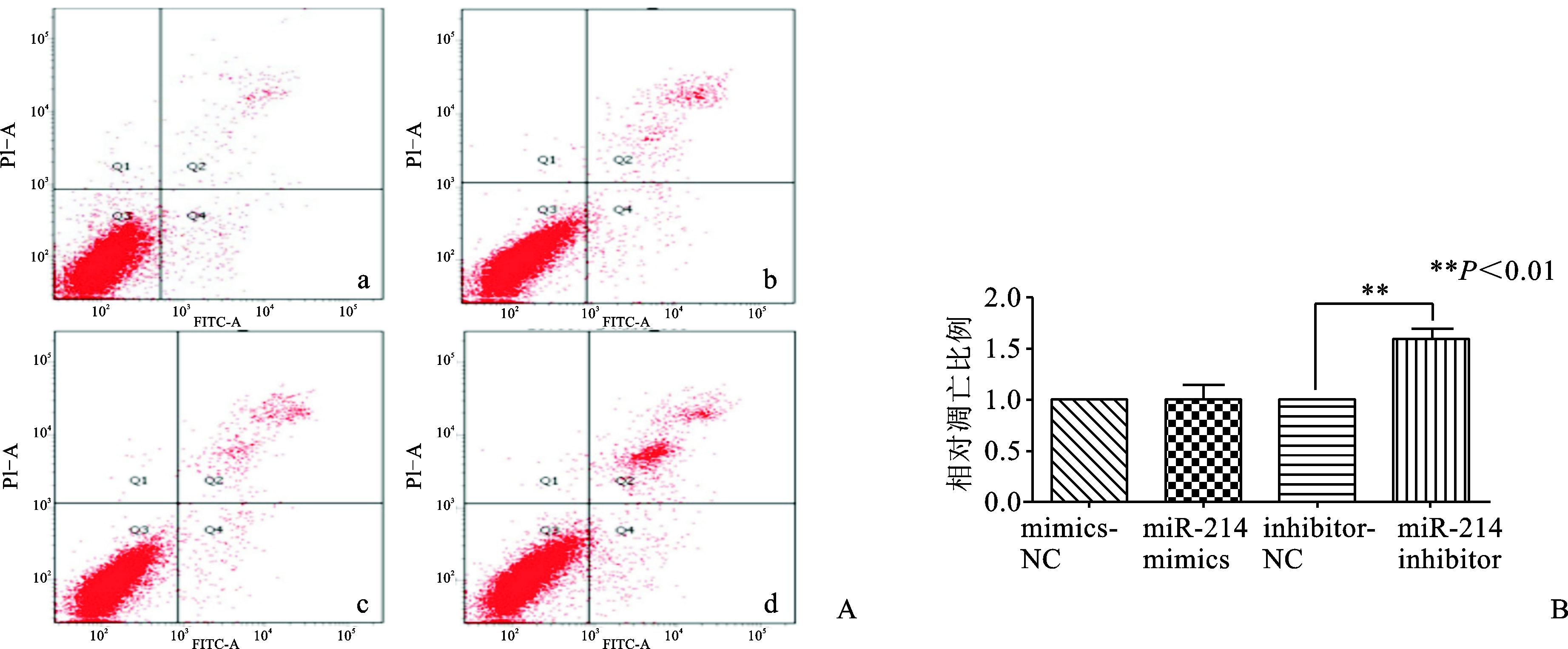
hsa-miR-214-3p mimics/mimics NC及hsa-miR-214-3p inhibitor/inhibitor NC转染SiHa细胞36 h后,使用流式细胞仪检测各组早期凋亡细胞的比例。结果 (图 6A、6B) 显示,抑制内源性hsa-miR-214-3p的表达相较于其阴性对照组,凋亡细胞的比例显著上升 (P<0.05);而过表达hsa-miR-214-3p后凋亡细胞的比例并无明显改变 (P>0.05)。
|
图 6 hsa-miR-214-3p促进SiHa细胞的凋亡 A:细胞凋亡散点图; B:细胞凋亡率分析; a:mimics NC; b:miR-214 mimics; c:inhibitor NC; d:miR-214 inhibitor |
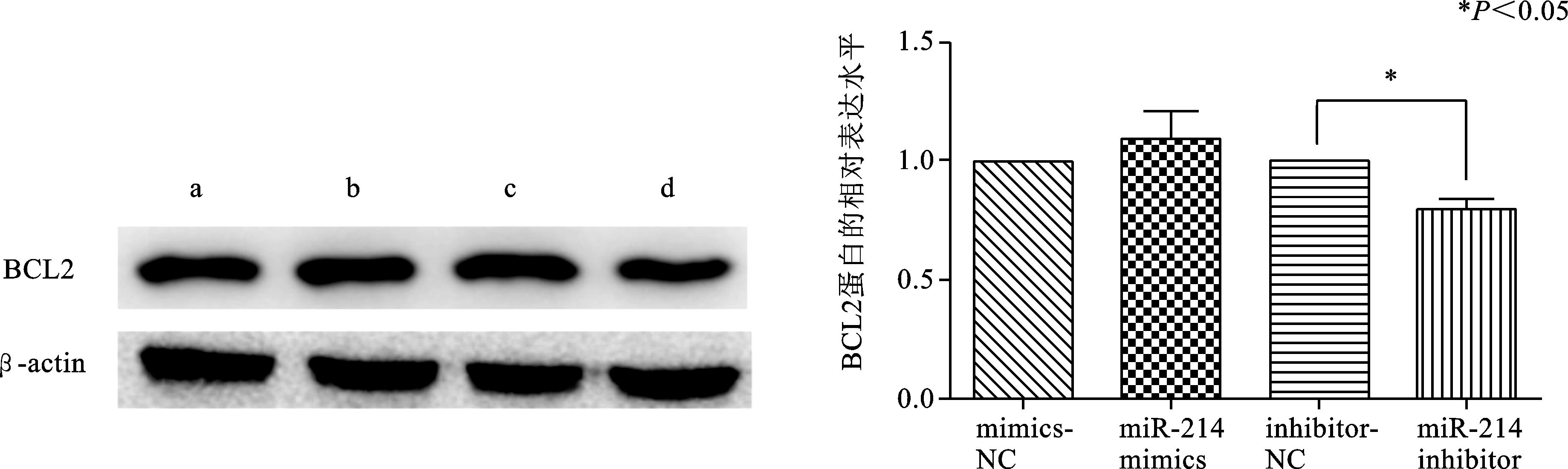
hsa-miR-214-3p mimics/mimics NC及hsa-miR-214-3p inhibitor/inhibitor NC转染SiHa细胞48 h后,分别提取各组总蛋白,采用蛋白质免疫印迹法检测Bcl2蛋白表达水平。结果 (图 7) 显示,抑制内源性hsa-miR-214-3p的表达相对于阴性对照组Blc2蛋白水平显著下降 (P<0.05);而过表达hsa-miR-214-3p后相较于其阴性对照组Bcl2蛋白水平并没有明显的变化 (P>0.05)。
|
图 7 转染后各组Bcl2蛋白的表达水平 a: mimics NC; b:miR-214 mimics; c: inhibitor NC; d: miR-214 inhibitor |
使用TargetscanHuman7.1、Pictar、miRanda三种靶基因预测软件分别预测hsa-miR-214-3p的靶基因,取三个数据库结果的交集并结合miRTarBase中已经至少用三种方法验证出来的靶基因,最后共得出169个靶基因。应用DAVID数据库对得出的靶基因进行KEGG富集通路分析,结果 (表 1) 显示hsa-miR-214-3p的靶基因显著富集于Wnt信号通路以及磷脂酰肌醇信号系统等 (P<0.01)。
| 表 1 hsa-miR-214-3p预测靶基因及富集通路 |
目前已发现多种miRNA与宫颈癌的发生发展密切相关。例如,miR-2861可以通过靶定EGFR/AKT2/CCND1抑制HPV16 E6阳性SiHa、CaSki细胞的增殖、迁移并促进其凋亡[8];miR-21可以通过下调抑癌基因PTEN的表达促进宫颈癌细胞的增殖并抑制其凋亡[9];miR-150可以通过靶定FOXO4促进宫颈癌细胞的增殖、促进细胞周期进程并抑制细胞凋亡[10]。hsa-miR-214-3p也是细胞内重要的miRNA,在多种恶性肿瘤中发挥着重要的作用。研究表明,miR-214可以通过抑制β-catenin蛋白的表达抑制肝癌细胞的生长增殖[11];miR-214可以通过直接作用于sema 4D抑制卵巢癌细胞的增殖并促进细胞凋亡[12]。目前hsa-miR-214-3p在宫颈鳞癌中的相关研究尚不深入,作用机制也尚不明确。本研究选用人宫颈癌鳞状上皮SiHa细胞作为研究对象,通过转染人工合成的hsa-miR-214-3p mimics/inhibitor,分别过表达和敲降癌细胞内hsa-miR-214-3p的水平,进一步观察癌细胞增殖、迁移以及凋亡等细胞生物学行为的改变,并探寻可能的分子机制。
实验结果表明,过表达hsa-miR-214-3p可以促进SiHa细胞的增殖,而抑制内源性hsa-miR-214-3p的表达之后,细胞的增殖能力显著降低,凋亡细胞的比例显著上升,Bcl2蛋白的表达显著下降。值得注意的是,过表达hsa-miR-214-3p后细胞凋亡及Bcl2蛋白的表达均没有明显变化,可能是由于hsa-miR-214-3p在SiHa细胞中呈高表达,而且调控癌细胞凋亡的途径复杂,所以导致转染了外源性的hsa-miR-214-3p模拟物后作用不明显所致。我们的结果还发现,无论是过表达或是抑制hsa-miR-214-3p的表达,SiHa细胞的迁移没有受到明显的影响,这表明hsa-miR-214-3p可能与SiHa细胞的迁移无关。生物信息学分析结果表明,hsa-miR-214-3p的靶基因主要富集在Wnt信号通路及磷脂酰肌醇信号系统等。另外本研究发现在HPV16型阳性SiHa、CaSki细胞以及HPV阴性C33A细胞中hsa-miR-214-3p的表达没有明显的差异,表明在宫颈癌中hsa-miR-214-3p的表达与HPV的作用可能不存在相关性。
Zhu等[13]组织芯片结果发现,相对于癌旁组织,Bcl2基因在宫颈癌组织中的表达是显著上升的。Bcl2蛋白家族是调节线粒体通透性的主要成分,通过形成同源二聚体抑制细胞凋亡[14]。而本研究结果显示,在抑制内源性hsa-miR-214-3p的表达后,Bcl2蛋白的表达显著下降,提示着hsa-miR-214-3p可能通过调节Bcl2基因的表达影响SiHa细胞的凋亡进程。hsa-miR-214-3p的靶基因预测与富集通路分析结果显示,PTEN、Bcl2L1、CDK6、MAPK1、MAPK8等基因参与多个信号通路,可以推测这些基因与hsa-miR-214-3p的功能高度相关。其中PTEN是公认的抑癌基因,已有研究证实miR-214可以通过下调PTEN的表达促进胃癌的腹膜转移[15],但在宫颈癌中未见报道;Bcl2L1为Bcl2家族的一员,本研究结果证实hsa-miR-214-3p与Bcl2存在一定的相关性,但hsa-miR-214-3p是否直接作用于Bcl2L1还需要后续实验的验证;CDK6是细胞周期蛋白依赖激酶 (CDK) 家族的一员,它可以使抑癌蛋白Rb磷酸化从而使细胞实现从G1期到S期的转换,这表明hsa-miR-214-3p可能与细胞周期的调控有关;MAPK1、MAPK8均为丝裂原活化蛋白激酶 (MAPK) 家族成员,表明hsa-miR-214-3p可能参与调控MAPK信号通路。以上分析为寻找hsa-miR-214-3p的直接靶基因和相关调控机制研究提供了思路。
综上所述,本研究证实过表达hsa-miR-214-3p可以促进宫颈癌SiHa细胞的增殖,抑制内源性hsa-miR-214-3p的表达后可以抑制SiHa细胞的增殖、促进其凋亡并下调Bcl2蛋白的表达,hsa-miR-214-3p可能通过调节Bcl2基因的表达影响SiHa细胞的凋亡进程,hsa-miR-214-3p靶基因的主要富集在Wnt信号通路以及磷脂酰肌醇信号系统等。本研究成果为hsa-miR-214-3p在宫颈癌中的作用及其机制研究提供了实验依据以及新的思路。
| [1] | Chen W, Zheng R, Baade PD, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-132. DOI: 10.3322/caac.21338. |
| [2] | Mohr AM, Mott JL. Overview of microRNA biology[J]. Semin Liver Dis, 2015, 35(1): 3-11. DOI: 10.1055/s-00000069. |
| [3] | Hayes J, Peruzzi PP, Lawler S. MicroRNAs in cancer: biomarkers, functions and therapy[J]. Trends Mol Med, 2014, 20(8): 460-469. DOI: 10.1016/j.molmed.2014.06.005. |
| [4] | Wang F, Lv P, Liu X, et al. microRNA-214 enhances the invasion ability of breast cancer cells by targeting p53[J]. Int J Mol Med, 2015, 35(5): 1395-1402. |
| [5] | Deng M, Ye Q, Qin Z, et al. miR-214 promotes tumorigenesis by targeting lactotransferrin in nasopharyngeal carcinoma[J]. Tumour Biol, 2013, 34(3): 1793-1800. DOI: 10.1007/s13277-013-0718-y. |
| [6] | Phatak P, Byrnes KA, Mansour D, et al. Overexpression of miR-214-3p in esophageal squamous cancer cells enhances sensitivity to cisplatin by targeting survivin directly and indirectly through CUG-BP1[J]. Oncogene, 2016, 35(16): 2087-2097. DOI: 10.1038/onc.2015.271. |
| [7] |
徐战战, 石芳, 赵旻. Let-7i抑制人卵巢癌SKOV3细胞的增殖、迁移和侵袭[J].
肿瘤, 2016, 36(2): 149-157.
Xu Z, Shi F, Zhao M. Let-7i inhibits the proliferation, migration and invasion of human ovarian cancer Skov3 cells[J]. Tumor, 2016, 36(2): 149-157. DOI: 10.3781/j.issn.1000-7431.2016.11.793. |
| [8] | Xu J, Wan X, Chen X, et al. miR-2861 acts as a tumor suppressor via targeting EGFR/AKT2/CCND1 pathway in cervical cancer induced by human papillomavirus virus 16 E6[J]. Sci Rep, 2016, 6: 28968. DOI: 10.1038/srep28968. |
| [9] | Peralta-Zaragoza O, Deas J, Meneses-Acosta A, et al. Relevance of miR-21 in regulation of tumor suppressor gene PTEN in human cervical cancer cells[J]. BMC Cancer, 2016, 16: 215. DOI: 10.1186/s12885-016-2231-3. |
| [10] | Li J, Hu L, Tian C, et al. microRNA-150 promotes cervical cancer cell growth and survival by targeting FOXO4[J]. BMC Mol Biol, 2015, 16: 24. DOI: 10.1186/s12867-015-0052-6. |
| [11] | Wang X, Chen J, Li F, et al. MiR-214 inhibits cell growth in hepatocellular carcinoma through suppression of β-catenin[J]. Biochem Biophys Res Commun, 2012, 428(4): 525-531. DOI: 10.1016/j.bbrc.2012.10.039. |
| [12] | Liu Y, Zhou H, Ma L, et al. MiR-214 suppressed ovarian cancer and negatively regulated semaphorin 4D[J]. Tumour Biol, 2016, 37(6): 8239-8248. DOI: 10.1007/s13277-015-4708-0. |
| [13] | Zhu MY, Chen F, Niyazi M, et al. Variation in apoptotic gene expression in cervical cancer through oligonucleotide microarray profiling[J]. J Low Genit Tract Dis, 2015, 19(1): 46-54. DOI: 10.1097/LGT.0000000000000030. |
| [14] | Hata AN, Engelman JA, Faber AC. The BCL2 family: key mediators of the apoptotic response to targeted anticancer therapeutics[J]. Cancer Discov, 2015, 5(5): 475-487. DOI: 10.1158/2159-8290.CD-15-0011. |
| [15] | Xin R, Bai F, Feng Y, et al. MicroRNA-214 promotes peritoneal metastasis through regulating PTEN negatively in gastric cancer[J]. Int Heart J, 2016, 57(2): 247-250. DOI: 10.1536/ihj.15-293. |
 2017, Vol. 38
2017, Vol. 38

