眼底视网膜神经细胞凋亡后,可引发多种疾病。常见疾病如青光眼,主要的病理表现是视网膜神经节细胞的凋亡,导致患者进行性视野缩小。常规抗青光眼药物主要是降低患者眼压,而对抑制视网膜神经节细胞凋亡方面,则缺乏特效药物。
雌激素不仅在生殖系统中有着重要的作用,在中枢神经保护方面也有作用。有统计表明,女性帕金森患病率较男性低[1],可能与雌激素作用有关。同样,在关于中枢神经损伤的研究中发现,雌激素也能保护缺血-再灌注损伤中的神经细胞[2]。视网膜作为中枢神经系统的一部分,近年来,有大量研究证实雌激素对视网膜损伤有保护作用,但是其具体机制尚不明确。
G蛋白偶联受体30(G protein-coupled receptor 30, GPR30)是雌激素受体中较晚发现的一种受体,广泛表达于全身多系统组织中,越来越多的研究证实它对雌激素靶器官的病理反应中有重要作用[3]。不同于经典的雌激素受体Eα和Eβ直接形成受体配体复合物进入核内,GPR30作为一种膜受体主要参与细胞质中的ERKs信号通路[4]。GPR30受体可表达在中枢神经系统,并参与神经保护作用[2, 5, 6]。激活该受体,可通过AKT通路影响细胞钙内流,从而保护神经细胞。同样,GPR30参与视网膜神经保护也有相关研究。Nixon[7]等人在研究视网膜光感受器细胞系中,发现GPR30受体激动剂G-1可保护该细胞系免受谷氨酸诱导的细胞凋亡。除此之外,关于GPR30在视网膜中其他层次结构中的作用则鲜有报道。
目前玻璃体腔注射N-甲基-D-天冬氨酸(NMDA)是国际公认的一种青光眼造模方法,可以激活视网膜神经节细胞上NMDA受体,诱导神经节细胞凋亡[8]。Müller细胞在视网膜中广泛存在,有研究表明,在青光眼动物模型中,Müller细胞的胞质内胶质纤维酸性蛋白(GFAP)表达量增加[9]。本实验用NMDA玻璃体腔注射后建立小鼠青光眼模型,研究雌激素及其受体GPR30在视网膜神经节细胞的保护作用和相关机制,为青光眼视神经保护提供新思路。
1 材料与方法 1.1 实验动物7-9周雄性C57BL/6J小鼠,由武汉大学人民医院动物中心及北京维通利华实验动物技术有限公司提供。
1.2 主要试剂和仪器N-甲基-D-天冬氨酸(NMDA)(Sigma公司,#684935,玻璃体腔注射,30 nmol/L); 雌二醇(上海紫一试剂厂,皮下注射10 d,10 μg/ml); 他莫西芬(Tamoxifen Tocris公司,皮下注射,皮下注射10 d,0.1 mg/ml); G-1(Cayman公司,皮下注射10 d,10 μg/ml); G-15(Cayman公司,皮下注射10 d,皮下注射,20 μg/ml); GPR30抗体(Abcam公司); Brn3a抗体(Santa Cruz公司); PKCα抗体(Santa Cruz公司); Opsin抗体(Santa Cruz公司); GFAP抗体(Santa Cruz公司); DAPI (谷歌生物公司); CY3标记的驴抗山羊IgG (谷歌生物公司,1:100稀释); FITC标记的驴抗小鼠IgG (谷歌生物公司,1:100稀释); FITC标记的驴抗山羊IgG (谷歌生物公司,1:100稀释); CY3标记的驴抗兔IgG (谷歌生物公司,1:100稀释); 冰冻切片机(德国Leica公司); 正置荧光显微镜(日本Olympus公司); CCD摄像机(Photometrics CoolSNAPTM ES2);激光共聚焦显微镜(FV1000)。
1.3 冰冻切片免疫荧光染色取7周C57/BL小鼠处死后立即取眼球,去除角膜、虹膜、晶体及玻璃体后于质量分数4%多聚甲醛中固定40 min,10%、20%和30%梯度浓度蔗糖脱水后,液氮迅速冷冻,制作小鼠眼球冻头,并于-80 ℃保存。冰冻切片制作小鼠视网膜(含巩膜)切片并于-20 ℃保存。将视网膜切片于质量分数5% BSAT封闭2 h,加入1:200 BSAT稀释的一抗,4 ℃过夜孵育。洗涤玻片,并加入1:200 BSAT稀释的二抗,室温孵育2 h。洗去二抗,加入DAPI (武汉谷歌生物公司),室温孵育20 min,于共聚焦显微镜下观察。以上实验重复3次,选取具有代表性结果。
1.4 视网膜铺片免疫荧光染色取7周C57小鼠处死后立即取眼球,去除角膜、虹膜、晶体及玻璃体后于质量分数4%多聚甲醛中固定40 min,显微镜下轻柔剥离巩膜及脉络膜,并于视网膜锯齿缘12点、3点、6点和9点方位,剪开视盘中心到锯齿缘边缘连线约2/3,在载玻片上铺成四叶草形状(玻璃体腔面朝上)。将视网膜铺片于质量分数5% BSAT,4 ℃条件下封闭24 h,加入1:200 BSAT稀释的一抗,4 ℃孵育3 d。洗涤视网膜铺片,并加入1:200 BSAT稀释的二抗,4 ℃环境24 h孵育。洗涤二抗,并重新铺片后封片,于荧光显微镜下观察。以上实验重复3次,选取具有代表性结果。
1.5 统计学分析实验数据拍照后以Photoshop CC 2014处理,并采用软件Graphpad Prism 5.0进行统计分析,图片后期处理使用Adobe Illustrator CC 2014。本研究检测指标数据采用t检验,P<0.05为差异有统计学意义。
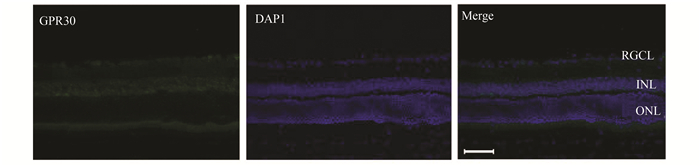
2 结果 2.1 C57小鼠视网膜中GPR30受体分布对C57小鼠视网膜冰冻切片,进行免疫荧光染色,观察GPR30在视网膜各层结构表达(图 1)。在正常C57小鼠中,GPR30受体(绿)主要表达于视网膜内核层和视网膜神经节细胞层。在外核层中,GPR30受体表达量很少。
|
图 1 GPR30受体在C57小鼠视网膜上表达(×400) 绿色为GPR30蛋白,蓝色为DAPI染色细胞核RGCL:视网膜神经节细胞层,INL:内核层,ONL:外核层(图中标尺为50 μm) |
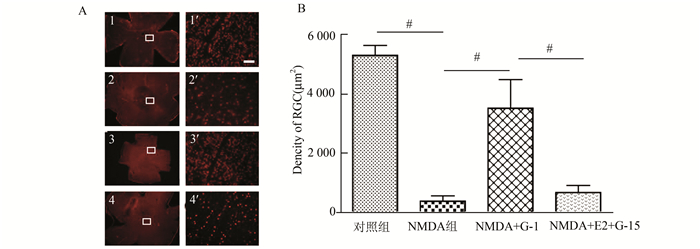
对C57雄性小鼠视网膜铺片,进行荧光染色,观察视网膜神经节细胞形态及数量变化并计数统计。C57雄性小鼠予以NMDA玻璃体腔注射,12 h后取眼球进行视网膜铺片,可见Brn3a (红)标记的神经节细胞数量明显较对照组减少,体积变小(图 2A); 相应给予雌激素及GPR30受体激动剂(G-1)、拮抗剂(G-15)和雌激素α与β受体拮抗剂(他莫西芬)后,观察神经节细胞数量及体积变化。雌激素连续注射10 d后(4.606±0.517, t检验, n=3)和单独给予雌激素受体激动剂(G-1)后(3.528±0.959, t检验, n=3)的NMDA模型小鼠中,视网膜神经节细胞数量相比NMDA组(0.398±0.174, t检验, n=3)增多(图 2B,P<0.05);在雌激素和GPR30受体拮抗剂(G-15)组中,视网膜神经节细胞数量(3.387±0.869, t检验, n=3)相比于加入他莫西芬组(0.686±0.236, t检验, n=3)下降(P<0.05)。该结果说明雌激素能抑制NMDA对视网膜神经节细胞的凋亡作用。通过雄鼠视网膜切片及染色观察(图 3),可看到Brn3a减少情况与铺片统计结果对应。
|
图 2 雌激素膜受体GPR30受体激活后对视网膜神经节细胞凋亡保护作用 A:免疫荧光染色示Brn3a标记神经节细胞(红); A1:对照组; A2:NMDA玻璃体腔注射12 h后,神经节细胞明显减少; A3:G-1皮下注射,并给予NMDA处理,未凋亡的神经节细胞数量增加; A4:G-15和17β-雌二醇皮下注射,并给予NMDA处理,神经节细胞凋亡增多; 图中标尺为100 μm。A1-A4(×20), A1′-A4′ (×200)。B:视网膜未凋亡的神经节细胞密度统计(t检验, P<0.05, n=3) |
|
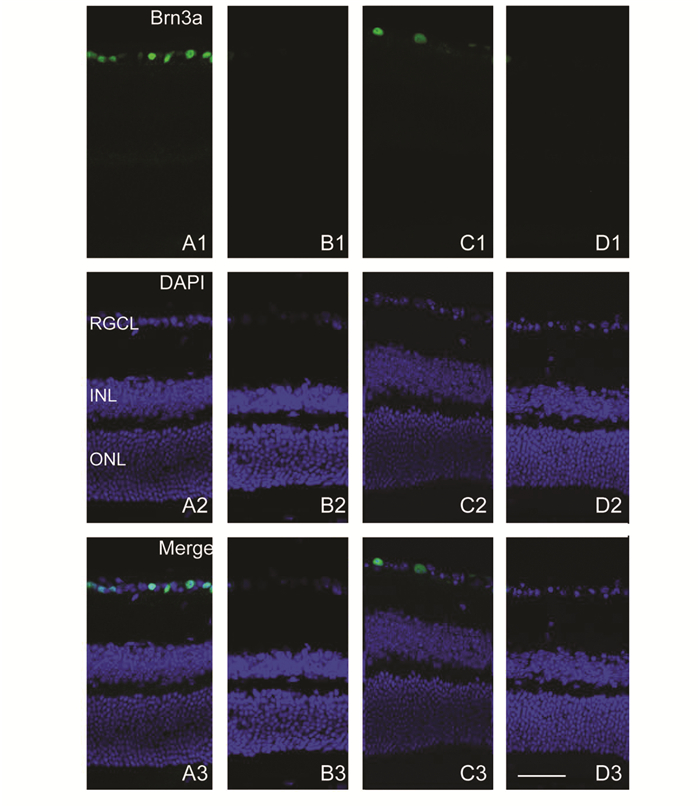
图 3 小鼠视网膜神经节细胞凋亡切片(×400) 免疫荧光示Brn3a标记视网膜神经节细胞(绿); A1-A3:对照组; B1-B3:NMDA玻璃体腔注射12 h后,神经节细胞凋亡明显; C1-C3:G-G1皮下注射后NMDA处理,神经节细胞未凋亡细胞增多; D1-D3:G-15和17β-雌二醇皮下注射后,给予NMDA处理,神经节细胞明显凋亡; 图中标尺为50 μm |
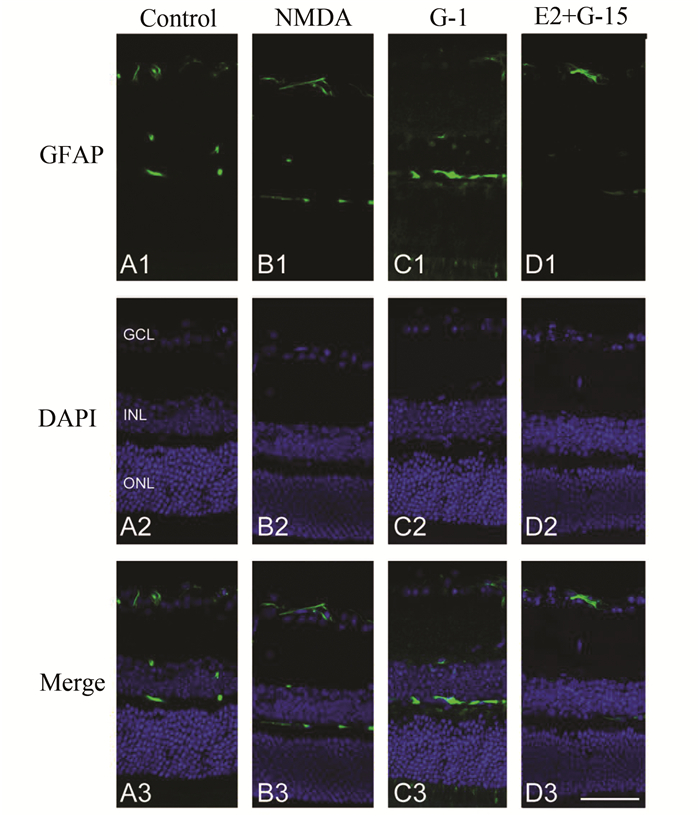
在雄性小鼠视网膜切片中染色,通过GFAP蛋白标记Müller细胞与Brn3a染色双标,观察神经节层胶质细胞增生与神经节细胞存活情况(图 4)。从图中可看出NMDA玻璃体腔注射12 h后,Brn3a标记的神经节细胞相比对照组明显减少,且胶质细胞明显增生(图 4A与图 4B)。经过GPR30受体激动剂(G-1)处理后,雄鼠在NMDA诱导下,视网膜神经节细胞层中胶质细胞增生减少(图 4C); 当给予雌激素同时抑制GPR30受体,玻璃体腔注射NMDA后视网膜节细胞层胶质细胞增多(图 4D)。这表明激活GPR30受体可抑制Müller细胞增生,从而减少NMDA诱导的视网膜神经节细胞凋亡。
|
图 4 GPR30抑制Müller细胞增生(×400) 免疫荧光示GFAP标记视网膜Müller细胞(绿) A1-A3:对照组; B1-B3:NMDA玻璃体腔注射12 h后,神经节细胞层中胶质细胞明显增生; C1-C3: G-1皮下注射后NMDA处理,神经节细胞层中胶质细胞减少; D1-D3: G-15和17β-雌二醇皮下注射后,给予NMDA处理,神经节细胞层中胶质细胞增生明显; 图中标尺为50 μm |
雌激素对于神经系统的保护作用已有相关研究。然而,GPR30作为雌激素的重要受体之一,是否参与视网膜神经保护作用?我们通过在NMDA模型中给予雌激素及GPR30受体激动剂和拮抗剂等干预,初步证明雌激素主要通过激活受体GPR30,抑制视网膜胶质细胞增生,并抑制了神经节细胞的凋亡,从而保护视网膜神经节细胞。
GPR30对神经细胞的保护,在这个受体发现不久就有相关报道。Lebesgue[10]在研究大脑缺血时发现,GPR30可通过激活细胞内的信号通路来促进脑细胞缺血后的存活; 在对帕金森氏病的动物研究中[6],发现GPR30对纹状体和黑质有保护作用; 对大鼠的空间学习研究中[11]发现,GPR30可加强雌激素在基底前脑的学习作用,从而影响学习功能。在眼科研究中,Nixon[7]发现激活GPR30可对光感受器细胞系起到保护作用,但这个作用不能被GPR30的抑制剂所逆转; Hayashi等人[8]在大鼠NMDA急性损伤视网膜神经节细胞的模型中发现,雌激素可抑制神经节细胞的凋亡。
我们的结果首次发现在活体中GPR30可保护视网膜神经节细胞。并且首次发现GPR30可抑制以Müller细胞为主的视网膜神经胶质细胞的增生。在神经节细胞培养中,神经节细胞可受到神经胶质细胞来源的PEDF保护[12]。同时,Müller细胞也是视网膜中唯一可产生谷氨酰胺合成酶的细胞[13]。本实验中发现Müller细胞内GFAP增生可被GPR30所抑制,可能是GPR30调节了Müller细胞的功能,抑制了Müller细胞的增生,从而指导Müller细胞对视网膜谷氨酸的代谢调节,抑制NMDA引起的谷氨酸神经毒性。
雌激素对视网膜神经节细胞的保护已有公认,通过GPR30途径保护神经节细胞则鲜有报道。GRP30在细胞内主要通过激活ERKs信号通路,产生多种作用。其中在研究大脑缺血损伤模型时发现,GPR30通过抑制DPAK1的磷酸化,抑制细胞钙内流,从而起到神经保护作用[5]。在视网膜神经节细胞中的具体细胞信号通路,则需要进一步的研究。GPR30受体介导的视网膜神经节细胞保护作用,可能在今后的抗青光眼药物中占有一席之地。
| [1] | Smith M, Dahodwala N. Sex differences in Parkinson's disease and other movement disorders[J]. Experimental Neurology, 2014, 259: 44-56. DOI: 10.1016/j.expneurol.2014.03.010. |
| [2] | Hu R, Sun H, Zhang Q, et al. G-protein coupled estrogen receptor 1 mediated estrogenic neuroprotection against spinal cord injury[J]. Critical Care Medicine, 2012, 40(12): 3230-3237. DOI: 10.1097/CCM.0b013e3182657560. |
| [3] | Olde B, Leeb-Lundberg LM. GPR30/GPER1: searching for a role in estrogen physiology[J]. Trends in endocrinology and metabolism: TEM, 2009, 20(8): 409-416. DOI: 10.1016/j.tem.2009.04.006. |
| [4] | Prossnitz ER, Barton M. The G-protein-coupled estrogen receptor GPER in health and disease[J]. Nature reviews Endocrinology, 2011, 7(12): 715-726. DOI: 10.1038/nrendo.2011.122. |
| [5] | Liu SB, Zhang N, Guo YY, et al. G-Protein-Coupled Receptor 30 Mediates Rapid Neuroprotective Effects of Estrogen via Depression of NR2B-Containing NMDA Receptors[J]. Journal of Neuroscience, 2012, 32(14): 4887-4900. DOI: 10.1523/JNEUROSCI.5828-11.2012. |
| [6] | Bouroue M, Morissette M, Cote M, et al. Implication of GPER1 in neuroprotection in a mouse model of Parkinson's disease[J]. Neurobiology of Aging, 2013, 34(3): 887-901. DOI: 10.1016/j.neurobiolaging.2012.05.022. |
| [7] | Nixon E, Simpkins JW. Neuroprotective effects of nonfeminizing estrogens in retinal photoreceptor neurons[J]. Investigative Ophthalmology & Visual science, 2012, 53(8): 4739-4747. |
| [8] | Hayashi Y, Kitaoka Y, Munemasa Y, et al. Neuroprotective effect of 17beta-estradiol against N-methyl-D-aspartate-induced retinal neurotoxicity via p-ERK induction[J]. Journal of Neuroscience Research, 2007, 85(2): 386-394. DOI: 10.1002/(ISSN)1097-4547. |
| [9] | Wang L, CioffigG A, Cull G, et al. Immunohistologic evidence for retinal glial cell changes in human glaucoma[J]. Investigative Ophthalmology & Visual Science, 2002, 43(4): 1088-1094. |
| [10] | Lebesgue D, Chevaleyre V, Zukin RS, et al. Estradiol rescues neurons from global ischemia-induced cell death: multiple cellular pathways of neuroprotection[J]. Steroids, 2009, 74(7): 555-561. DOI: 10.1016/j.steroids.2009.01.003. |
| [11] | Hammond R, Nelson D, Kline E, et al. Chronic treatment with a GPR30 antagonist impairs acquisition of a spatial learning task in young female rats[J]. Hormones and Behavior, 2012, 62(4): 367-374. DOI: 10.1016/j.yhbeh.2012.07.004. |
| [12] | Unterlauft JD, Claudepierre T, Schmidt M, et al. Enhanced survival of retinal ganglion cells is mediated by Muller glial cell-derived PEDF[J]. Exp Eye Res, 2014, 127: 206-214. DOI: 10.1016/j.exer.2014.08.004. |
| [13] | Linser PJ, Sorrentino M, Moscona AA. Cellular compartmentalization of carbonic anhydrase-C and glutamine synthetase in developing and mature mouse neural retina[J]. Brain Research, 1984, 315(1): 65-71. |
 2016, Vol. 37
2016, Vol. 37

