2. 武汉大学中南医院呼吸内科 湖北 武汉 430071;
3. 武汉大学人民医院呼吸内科 湖北 武汉 430060
2. Dept. of Respiratory Medicine, Zhongnan Hospital of Wuhan University, Wuhan 430071, China;
3. Dept. of Respiratory Medicine, Renmin Hospital of Wuhan University, Wuhan 430060, China
自然杀伤(natural killer,NK) T细胞是一群独特和数量较少的淋巴细胞亚群,分为Ⅰ型和Ⅱ型NKT细胞,两者之间存在相互调节作用[1]。我们的初步研究显示α半乳糖神经酰胺活化Ⅰ型NKT细胞可以增强哮喘小鼠气道炎症[2],但硫酸脑苷脂活化Ⅱ型NKT细胞抑制Ⅰ性NKT细胞活性并不能完全抑制哮喘小鼠气道炎症[3]。因此,Ⅰ型NKT细胞在哮喘气道炎症形成中是发挥效应作用,还是调节作用存在争论[4]。本研究首先观察哮喘小鼠肺Ⅰ型NKT细胞数量和活性,并了解过继转移Ⅰ型NKT细胞对哮喘小鼠气道炎症的影响;进一步以卵清白蛋白(OVA)致敏和激发CD1d-/--BALB/c小鼠(缺乏功能性Ⅰ型NKT细胞),观察缺乏Ⅰ型NKT细胞对小鼠气道炎症的影响,探讨Ⅰ型NKT细胞在哮喘小鼠气道炎症形成中的作用。
1 材料与方法 1.1 实验动物和主要试剂6周龄健康雌性BALB/c小鼠购自武汉大学实验动物中心,6周龄健康雌性CD1d-/--BALB/c小鼠购自美国Jackson实验室,无特定病原菌(SPF)环境饲养。鸡卵清白蛋白(OVA,Grade,V)和氢氧化铝凝胶(美国Sigma公司),IL-4、IL-5和IL-13 ELISA试剂盒(美国Ebioscience公司),大鼠抗小鼠IgE和IgG1抗体(美国Biolegend公司),亲和素连接的辣根过氧化物酶(美国Sigma公司),Brefeldin A、PE-Cy5标记的TCR-β、PE-Cy5的同型阴性对照、FITC标记的IFN-γ、FITC标记的IL-4、链霉亲和素连接的PE、固定剂、破膜剂均购于美国eBioscience公司,Ⅰ型胶原酶购自Invitrogen公司,PE标记的未负载的小鼠CD1d四聚体由美国国家卫生研究院(National Institutes of Health,NIH)赠送。
1.2 小鼠分组与哮喘模型的建立24只野生型BALB/c小鼠按随机数字表法随机分为对照组、哮喘组和过继转移组,每组8只;随机数字表法随机选取8只CD1d-/--BALB/c小鼠为CD1d-/-组。建立小鼠哮喘模型的方法参考文献[3]。正常对照组小鼠在相应时间内腹腔注射等量的PBS并以PBS鼻腔滴入。
1.3 哮喘小鼠Ⅰ型NKT细胞的制备与过继转移取哮喘小鼠第27天OVA激发后24 h的脾脏,制备成脾单个核细胞悬液,流式细胞仪分选Ⅰ型NKT细胞(PBS57/CD1d四聚体+TCR-β+细胞)。于第25天OVA激发前1 h,将哮喘小鼠Ⅰ型NKT细胞经尾静脉注射到过继转移组小鼠体内,每只注入3×106细胞。
1.4 标本的收集和处理与细胞学、组织学检测各组小鼠于末次激发48 h后眼球取血2 ml,分离血清分装,-80 ℃保存,用于检测血清OVA特异性IgE和IgG1。小鼠肺泡灌洗方法参考文献[3]。支气管肺泡灌洗液(BALF)在4 ℃下1 500 r/min离心5 min,收集上清液,-80 ℃保存,用于检测IL-4、IL-5和IL-13水平。用含1%BSA的PBS重悬细胞沉淀,调整细胞浓度为1×106/ml,取100 μl细胞悬液离心涂片,姬姆萨染色检测各细胞分类计数。取右肺组织,肺组织的处理和肺单个核细胞(MNCs)的制备参考文献[3]。取左肺组织,以10%中性甲醛溶液固定,常规石蜡包埋、切片,HE和PAS染色,观察肺组织炎症和气道基底膜PAS+细胞(杯状细胞)。
1.5 肺Ⅰ型NKT细胞数量和分泌细胞因子水平的检测取肺单个核细胞(MNCs)悬液,调整浓度为1×106/ml,肺Ⅰ型NKT细胞数量和分泌细胞因子水平检测方法参考文献[2]。
1.6 血清OVA特异性IgE和IgG1以及BALF中细胞因子的检测采用ELISA法检测小鼠血清OVA特异性IgE和IgG1的水平,结果以OD值表示为相对水平,其检测步骤参考文献[3]。采用ELISA法检测BALF中的IL-4、IL-5和IL-13的水平。
1.7 统计学处理应用SPSS 13.0软件进行统计分析。数据以均数±标准差(x±s)表示,采用单因素方差分析和配对t检验,P<0.05为差异有统计学意义。
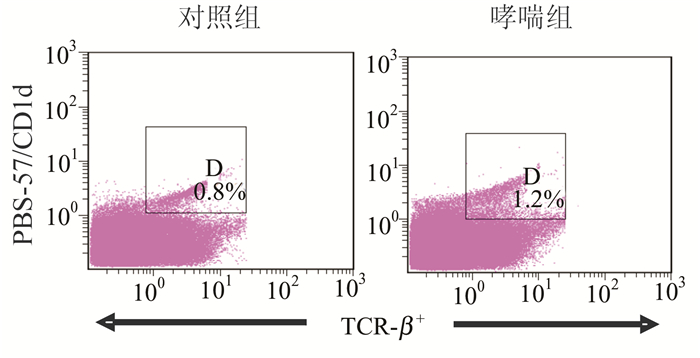
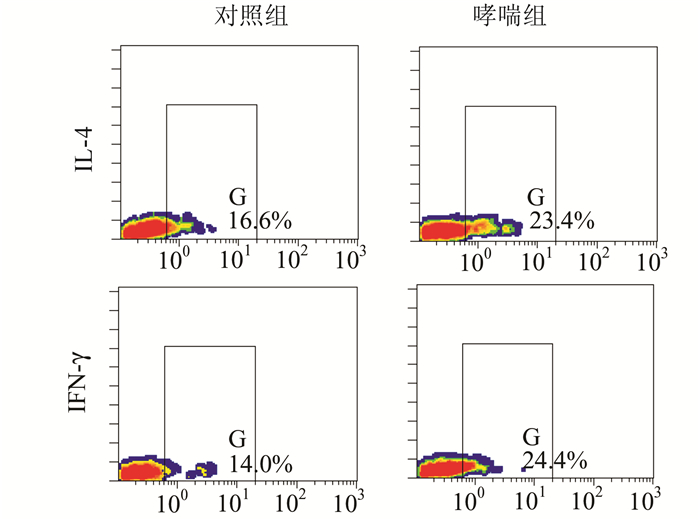
2 结果 2.1 哮喘组与对照组小鼠肺Ⅰ型NKT细胞数量和活性比较哮喘组小鼠肺Ⅰ型NKT细胞百分比与对照组比较差异有统计学意义(P<0.01)(图 1,表 1);以分泌细胞因子的水平表示肺Ⅰ型NKT细胞的活性,哮喘组小鼠IL-4+和IFN-γ+Ⅰ型NKT细胞百分比与对照组比较差异有统计学意义(P<0.05或P<0.01)(图 2,表 1)。
|
图 1 肺Ⅰ型NKT细胞占肺单个核细胞百分数比较 D门中的百分数表示肺Ⅰ型NKT细胞(PBS57/小鼠CD1d四聚体+TCR-β+细胞)占肺单个核细胞(MNCs)的百分数 |
|
图 2 分泌IL-4和IFN-γ的肺Ⅰ型NKT细胞占肺Ⅰ型NKT细胞的百分数比较 G门中的百分数表示分泌IL-4(上图)和IFN-γ(下图)的肺Ⅰ型NKT细胞占肺Ⅰ型NKT细胞的百分数 |
| 表 1 各组小鼠肺Ⅰ型NKT细胞、IL-4+和IFN-γ+Ⅰ型NKT细胞数量(x±s) |
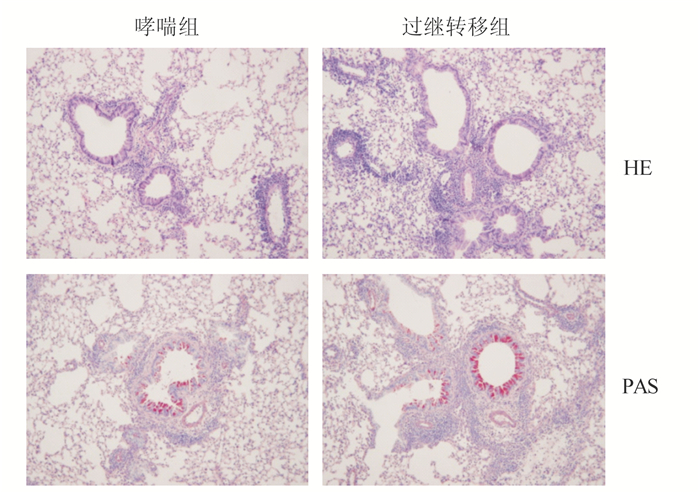
哮喘组小鼠肺组织、气道和血管周围可见炎性细胞浸润,以嗜酸性粒细胞、淋巴细胞为主,肺泡上皮细胞破坏,支气管黏膜增厚、管腔狭窄,气道基底膜可见较多PAS+细胞(杯状细胞);过继转移组小鼠支气管肺组织炎症反应更加明显,气道基底膜PAS+细胞更多(图 3)。
|
图 3 各组肺组织HE染色(×100倍)及PAS染色(×100倍) |
过继转移组小鼠BALF中嗜酸性粒细胞百分比与哮喘组比较差异有统计学意义(P<0.01)(表 2)。
| 表 2 各组小鼠BALF中细胞分类百分数比较(x±s) |
过继转移组和哮喘组小鼠血清OVA特异性IgE与IgG1水平分别为(0.293 2±0.061 3) pg/ml和(0.214 8±0.033 2) pg/ml,(0.609 5±0.135 9)和(0.375 6±0.101 9) pg/ml,两组比较差异有统计学意义(P<0.01);BALF中IL-4、IL-5和IL-13的水平与哮喘组比较差异有统计学意义(P<0.05或P<0.01)(表 3)。
| 表 3 各组小鼠BALF中IL-4、IL-5和IL-13水平比较(x±s,pg/ml) |
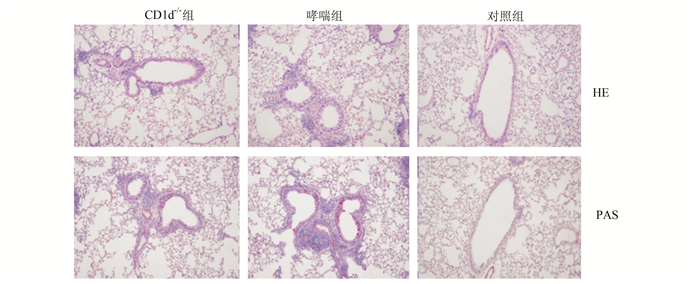
哮喘组小鼠肺组织、气道和血管周围可见炎性细胞浸润,以嗜酸粒细胞、淋巴细胞为主,肺泡上皮细胞破坏,支气管黏膜增厚、管腔狭窄,气道基底膜可见较多PAS+细胞(杯状细胞);CD1d-/-组小鼠支气管肺组织炎症反应减轻,气道基底膜PAS+细胞(杯状细胞)减少,但比对照组小鼠更为明显(图 4)。
|
图 4 各组肺组织HE染色(×100)及PAS染色(×100)照片 |
CD1d-/-组小鼠BALF中嗜酸粒细胞百分比明显低于哮喘组(P<0.01),但明显高于对照组(P<0.01)(表 4)。
| 表 4 各组小鼠BALF中细胞分类百分比比较(x±s) |
CD1d-/-组小鼠血清OVA特异性IgE和IgG1水平明显低于哮喘组(P<0.01),但明显高于对照组(P<0.01)(表 5);BALF中IL-4、IL-5和IL-13水平明显低于哮喘组(P<0.05或P<0.01),但明显高于对照组(P<0.01)(表 6)。
| 表 5 各组小鼠血清OVA特异性IgE和IgG1水平比较(pg/ml, x±s) |
| 表 6 各组小鼠BALF中IL-4、IL-5和IL-13水平比较(x±s, pg/ml) |
NKT细胞可以识别CD1d限制的特异性脂类配体,根据其T细胞受体是否可变分为Ⅰ型NKT细胞和Ⅱ型NKT细胞[1]。Ⅰ型NKT细胞在哮喘气道炎症形成中是发挥效应作用,还是调节作用存在争论[4]。本研究显示随着OVA诱导哮喘小鼠气道炎症的形成,肺Ⅰ型NKT细胞的数量及活性明显增高,提示Ⅰ型NKT细胞可能参与哮喘小鼠气道炎症的形成。OVA诱导哮喘小鼠模型时,小鼠肺Ⅰ型NKT细胞活化的原因并不清楚。研究认为Ⅰ型NKT细胞可以通过识别内源性脂类抗原或病原微生物来源的外源性脂类抗原活化[1]。目前已发现几种内源性糖脂或磷脂抗原可以活化Ⅰ型NKT细胞[1],而一些细菌细胞壁中存在的外源性糖脂类抗原亦可以活化Ⅰ型NKT细胞[5, 6]。因此,我们推测哮喘小鼠肺Ⅰ型NKT细胞可能通过识别内源性或外源性脂类抗原活化,但需进一步研究。
α半乳糖神经酰胺(α-GalCer)是Ⅰ型NKT细胞特异性配体[7]。α-GalCer可以特异性激活Ⅰ型NKT细胞[2, 3]。研究显示α-GalCer可以增强OVA诱导的哮喘小鼠肺Ⅰ型NKT细胞活化水平,同时伴随哮喘小鼠气道炎症的加重[2]。为了进一步了解Ⅰ型NKT细胞在哮喘小鼠气道炎症形成中的作用,本研究观察过继转移Ⅰ型NKT细胞对OVA诱导的哮喘小鼠气道炎症的影响,结果发现过继转移组小鼠支气管肺组织炎症反应更加明显,气道基底膜PAS+细胞(杯状细胞)更多;血清OVA特异性IgE和IgG1水平和BALF中嗜酸性粒细胞数量以及IL-4、IL-5和IL-13的水平更高,提示过继转移Ⅰ型NKT细胞可以增强哮喘小鼠气道炎症。CD1d基因敲除鼠(CD1d-/-小鼠)缺乏功能性Ⅰ型NKT细胞。因此,本研究进一步以OVA致敏和激发CD1d-/-小鼠,观察缺乏Ⅰ型NKT细胞对小鼠气道炎症的影响,结果发现CD1d-/-小鼠支气管肺组织炎症反应减轻,气道基底膜PAS+细胞(杯状细胞)减少,但比对照组小鼠明显;血清OVA特异性IgE和IgG1水平和BALF中嗜酸性粒细胞数量以及IL-4、IL-5和IL-13水平明显低于哮喘组,但明显高于对照组,结果提示尽管缺乏Ⅰ型NKT细胞可以减轻OVA致敏和激发的小鼠气道炎症,但气道炎症仍然存在。
Ⅰ型NKT细胞参与OVA诱导的哮喘小鼠气道炎症形成的机制并不清楚。Fujii等[8]研究显示,静脉注射α-GalCer 4 h内可以诱导小鼠脾树突状细胞表型和功能成熟,进一步观察发现α-GalCer并不直接诱导树突状细胞成熟,而是需要存在Ⅰ型NKT细胞。Shin等[9]的研究显示,与CD1d-/-受体鼠比较,过继转移OVA特异性CD4+T细胞的CD1d+/-受体鼠的哮喘特征更为明显,进一步观察发现OVA激发的CD1d+/-受体鼠体内树突状细胞表面分子CD86水平显著高于CD1d-/-受体鼠,因此,我们推测Ⅰ型NKT细胞可能通过调节树突状细胞的功能参与哮喘小鼠气道炎症的形成,但需进一步研究。
综上所述,Ⅰ型NKT细胞可以增强哮喘小鼠气道炎症,但并不是哮喘小鼠气道炎症形成的必需因素。
| [1] | Terabe M, Berzofsky JA. The immunoregulatory role of type Ⅰ and type Ⅱ NKT cells in cancer and other diseases[J]. Cancer Immunol Immunother, 2014, 63(3): 199-213. DOI: 10.1007/s00262-013-1509-4. |
| [2] | 张固琴, 聂汉祥, 刘敏, 等. α半乳糖神经酰胺活化iNKT细胞对哮喘小鼠过敏性气道炎症的影响[J]. 武汉大学学报:医学版, 2013, 34(4): 499-503. |
| [3] | Zhang G, Nie H, Yang J, et al. Sulfatide-activated type Ⅱ NKT cells prevent allergic airway inflammation by inhibiting type Ⅰ NKT cell function in a mouse model of asthma[J]. Am J Physiol Lung Cell Mol Physiol, 2011, 301(6): L975-L984. DOI: 10.1152/ajplung.00114.2011. |
| [4] | Thomas SY, Chyung YH, Luster AD. Natural killer T cells are not the predominant T cell in asthma and likely modulate, not cause, asthma[J]. J Allergy Clin Immunol, 2010, 125(5): 980-984. DOI: 10.1016/j.jaci.2010.01.032. |
| [5] | Kinjo Y, Wu D, Kim G, et al. Recognition of bacterial glycosphingolipids by natural killer T cells[J]. Nature, 2005, 434(7 032): 520-525. |
| [6] | Tsuji M. Glycolipids and phospholipids as CD1d-binding NKT cell ligands[J]. Cell Mol Life Sci, 2006, 63(16): 1889-1898. DOI: 10.1007/s00018-006-6073-z. |
| [7] | Lynch L, Michelet X, Zhang S, et al. Regulatory iNKT cells lack expression of the transcription factor PLZF and control the homeostasis of Treg cells and macrophages in adipose tissue[J]. Nat Immunol, 2015, 16(1): 85-95. |
| [8] | Fujii S, Shimizu K, Smith C, et al. Activation of natural killer T cells by alpha-galactosylceramide rapidly induces the full maturation of dendritic cells in vivo and thereby acts as an adjuvant for combined CD4 and CD8 T cell immunity to a coadministered protein[J]. J Exp Med, 2003, 198(2): 267-279. DOI: 10.1084/jem.20030324. |
| [9] | Shin Y, Hong C, Lee H, et al. NKT cell-dependent regulation of secondary antigen-specific, conventional CD4+ T cell immune response[J]. J Immunol, 2010, 184(10): 5589-5594. DOI: 10.4049/jimmunol.0903121. |
 2016, Vol. 37
2016, Vol. 37

