青光眼视神经病变是一类以视网膜神经节细胞(retinal ganglion cell,RGC)及其轴突进行性丢失为病理基础的神经变性疾病,是全球首位不可逆性致盲眼病[1]。目前认为青光眼性视神经损害的一个重要因素是细胞外高浓度的谷氨酸[2, 3],研究发现,细胞外谷氨酸的终止灭活主要靠视网膜Müller细胞上的L-谷氨酸/L-天门冬氨酸转运体(Glutamate-aspartate transporter, GLAST)摄入细胞内,从而使细胞外谷氨酸浓度处于神经毒性水平以下[4]。一旦视网膜Müller细胞受损,神经节细胞将受到谷氨酸毒性作用。此外,研究压力梯度对视网膜Müller细胞影响少有文献报道。基于上述原因,我们开展对体外培养的视网膜Müller细胞经不同压力处理后进行形态学、活性变化和GLAST表达的研究。
1 材料与方法 1.1 材料来源SD大鼠Müller细胞来自武汉大学生命科学院馈赠。
1.2 主要试剂GLAST多克隆抗体(武汉博士德生物公司,批号:BA0892),辣根过氧化物酶(HRP)标记的羊抗兔二抗(武汉博士德生物公司,批号:BA1054),Dulbecco改良Eagle培养基(DMEM,美国Gibico公司),胎牛血清(杭州四季清公司),0.25%胰蛋白酶(美国Sigma公司)。
1.3 实验仪器自行设计与制备压力装置:注射器通过加工在尾部安装铝板,在铝板中央钻孔,通过旋转丝杠推注射器芯杆来控制注入无菌气体速度。注入无菌气体,再经除菌滤过器、链接导管、变径对接头、链接导管至三通管,三通管一端外接压力表,另一端外接培养瓶。
其他主要仪器包括细胞培养箱(美国Thermo公司),倒置显微镜(日本Olympus公司),低速离心机(德国Eppendorf公司),酶标仪(美国Thermo公司),水平摇床(江苏海门其林贝尔仪器制造有限公司),凝胶电泳仪及电泳槽、半干式转印仪、凝胶成像分析系统(美国Bio-Rad公司)。
1.4 实验方法 1.4.1 建立压力培养模型将SD大鼠Müller原代细胞第4代细胞用于实验。按不同压力将细胞随机分为5组,其中对照组为A组(+0 mmHg),实验组分别为B组(+15 mmHg)、C组(+30 mmHg)、D组(+45 mmHg)、E组(+60 mmHg),每组3瓶,37 ℃,5%CO2培养箱培养2 h。
1.4.2 倒置显微镜观察Müller细胞形态Müller细胞经上述处理后,倒置显微镜下肉眼观察Müller细胞形态并进行拍照记录。
1.4.3 加压后Müller细胞的细胞活性的变化观察取0,15,30,45,60 mmHg 5个不同压力处理2 h。每孔加入浓度为5 mg/ml的噻唑蓝(MTT)20 μl,孵育4 h后,吸出MTT,加入二甲基亚砜(DMSO),振荡10 min,用酶联免疫监测仪(Thermo-MULTISKAN MK3)测每孔样本的吸光度值。测定波长570 nm处的吸光度(A)值,以各组A值计算细胞相对存活率。细胞相对存活率=(各实验组A值/正常对照组A值)×100%。
1.4.4 Western blot法检测GLAST的表达采用免疫蛋白印迹法(Western blot)检测各组大鼠视网膜Müller细胞上GLAST的蛋白表达。取对数生长期细胞,5组分别加压0,15,30,45,60 mmHg处理2 h后,制成细胞悬液,以密度1×106个/孔细胞接种于6孔板中,置于37 ℃、5% CO2培养箱中培养24 h。获取培养细胞后,裂解缓冲液抽提蛋白,4 ℃条件下,12 000 r/min 37 ℃孵育1 h,洗涤后加入二氨基联苯胺(DAB)室温避光显色。图像扫描后,应用BandScan软件测定蛋白条带灰度值,以GLAST和β-actin的比值作为相对表达水平。
采用SPSS 17.0统计学软件进行统计分析,实验数据以均数±标准差(x±s)表示。组间比较采用单因素方差分析,组间两两比较采用LSD检验。取双侧α=0.05统计学检测水准。
2 结果光镜观察发现,正常Müller细胞体呈长圆形、星型、梭型、多角型等,细胞质丰富,细胞核位于细胞体中央,细胞体二端锥状长突起,末端膨大(图 1)。不同压力下的细胞形态改变不明显,胞体无皱缩,胞质透明,细胞间隙无增大(图 1)。

|
图 1 不同压力对体外培养的Müller细胞的光学显微镜像(×100) A-E:分别代表A-E组 |
MTT检测显示,A、B、C、D、E组A值分别为1.676 3±0.054 7、1.503 3±0.053 6、1.209 3±0.045 5、1.020 0±0.040 0、0.706 3±0.034 1;细胞相对存活率分别为100%、89.3%、71.3%、59.7%、40.3%。其中,B、C、D、E组A值均较A组降低(P<0.05)。随着压力的升高,细胞相对存活率均逐渐降低,各组间总体差异均有统计学意义(P<0.05)。
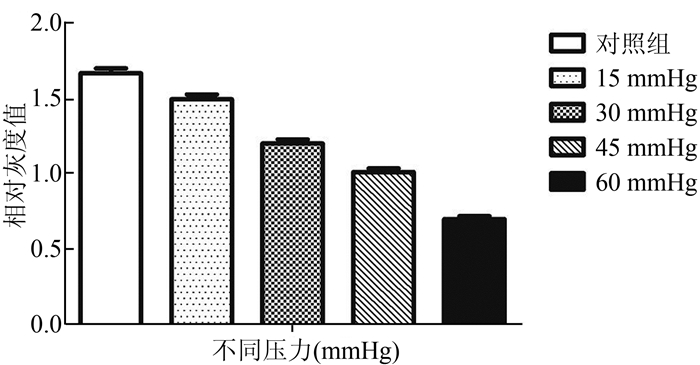
Western blot检测显示,GLAST和β-actin蛋白条带分别出现在相对分子质量6.5×104、4.2×104处。与A组相比,其余各组的大鼠视网膜Müller细胞的GLAST蛋白表达均下降,差异有统计学意义(P<0.05)。大鼠视网膜Müller细胞上GLAST的蛋白表达随着压力的升高逐渐降低,各组间总体差异均有统计学意义(P<0.05)。见图 2。
|
图 2 不同压力对大鼠视网膜Müller细胞GLAST不同压力对大鼠视网膜Müller细胞GLAST |
谷氨酸是广泛存在于视网膜神经节细胞中的一种兴奋性神经递质,研究表明细胞外5 μmol/L的谷氨酸即可对神经元有致死作用[5]。在视网膜组织中,谷氨酸代谢平衡通过视神经细胞和胶质细胞之间的谷氨酸-谷氨酰胺循环完成。视网膜主要胶质细胞--Müller细胞是调节视网膜谷氨酸的关键场所[6],其通过细胞上的L-谷氨酸/L-天门冬氨酸转运体(GLAST)将谷氨酸摄入细胞内,通过谷氨酰胺合成酶的催化把谷氨酸转化为谷氨酰胺,并将其释放到组织间隙,由神经细胞摄入转化成为谷氨酸,将其释放到突触后间隙,一部分用于递质传导,大部分被细胞上的GLAST转运到胶质细胞体内,进入新一轮的循环。
目前已确认有5种谷氨酸转运体(Excitatory amino acid carrier 1-5,EAAT 1-5)在视网膜谷氨酸清除中起作用,GLAST又称EAAT1,是其中最主要的谷氨酸转运体[7-9]。GLAST主要分布于视网膜Müller细胞[10]。Naskar[11]发现在青光眼患者的标本中Müller细胞上GLAST蛋白表达减少。Yu等[12]研究表明青光眼细胞外谷氨酸浓度升高同时Müller细胞GLAST含量减少。Tezel等[13]发现在调节细胞外谷氨酸浓度方面,GLAST较其它视网膜谷氨酸转运体更敏感。Harada等[14]报道敲除GLAST基因的正常眼压性青光眼小鼠模型的(RGC)自发性变性,给予谷氨酸受体抗体防止RGC的死亡。因此在青光眼状态下GLAST的结构和功能异常可能会导致细胞外谷氨酸浓度升高致使视网膜神经节细胞受损。
本实验观察多压力梯度处理后Müller细胞的形态、活性及GLAST的蛋白表达,以探讨Müller细胞对不同压力的耐受程度及压力梯度对其谷氨酸代谢功能的影响。我们发现不同压力处理后,Müller细胞在倒置显微镜下形态改变不明显,MTT检测细胞活性随着压力升高而降低,GLAST的蛋白表达随着压力的升高而呈降低趋势。MTT法主要反映的线粒体代谢能力的降低,由此可见随着压力增大细胞能量代谢障碍加重。GLAST为钠离子依赖性转运体,其利用钠钾-ATP酶逆浓度梯度使谷氨酸从细胞间隙转运到Müller细胞[14]。随着压力升高ATP生成减少,因此Müller细胞摄入谷氨酸的能力下降以致细胞外谷氨酸浓度升高。由于在谷氨酸-谷酰胺循环中,Müller细胞GLAST摄取细胞外谷氨酸能力下降,从而可能造成细胞外谷氨酸的积聚。我们推测在青光眼发病及进展中,GLAST的蛋白表达出现异常而出现功能变化,导致Müller细胞转运细胞外谷氨酸不能正常进行,可能是青光眼损伤过程中高浓度谷氨酸的原因。引起Müller细胞GLAST表达下降的机制可能是:①通过下调GLAST mRNA的转录而使GLAST的表达下降[16];②激活凋亡基因,诱导Müller细胞凋亡,导致GLAST活性随着下降[17, 18]。
综上所述,对于大鼠视网膜Mülle细胞,压力能直接影响其在体外培养下存活状况。随压力升高,大鼠视网膜Müller细胞存活率下降,且细胞上的GLAST的蛋白表达下降。
从我们研究的结果来看,压力诱导GLAST的蛋白表达水平发生变化,这个过程至少部分参与了青光眼的发生及发展,这为以后的研究奠定了基础,对于更进一步了解青光眼性的神经损伤具有重要意义。
| [1] | Cheng JW, Cheng SW, Ma XY, et al. The prevalence of primary glaucoma in mainland China:a systematic review and meta-analysis[J]. Glaucoma, 2013, 22(4): 301-306. DOI: 10.1097/IJG.0b013e31824083ca. |
| [2] | Aihara M. Hyperbaric pressure and increased susceptibility to glutamate toxicity in retinal ganglion cells in vitro[J]. Molecular Vision, 2014, 20(3): 606-615. |
| [3] | Bai N, Aida T, Yanagisawa M, et al. NMDA receptor subunits have different roles in NMDA-induced neurotoxicity in the retina[J]. Mol Brain, 2013, 6: 34. DOI: 10.1186/1756-6606-6-34. |
| [4] | Bringmann A, Grosche A, Pannicke T, et al. GABA and Glutamate Uptake and Metabolism in Retinal Glial (Müller) Cells[J]. Frontiers in Endocrinology, 2013, 4: 48. |
| [5] | 钱志刚, 柯敏. 花色苷对高糖培养的视网膜Müller细胞L-谷氨酸/L-天门冬氨酸转运体表达的影响[J]. 中华眼底病杂志, 2011, 27(2): 170-173. |
| [6] | Li Y, Liu X, Huang S, et al. Effect of SCH442416 on glutamate uptake in retinal Müller cells at increased hydrostatic pressure[J]. Mol Med Rep, 2015, 12(3): 3 993-3 998. |
| [7] | Jablonski MM, Freeman NE, Orr WE, et al. Genetic pathways regulating glutamate levels in retinal Müller cells[J]. Neurochemical research, 2011, 36(4): 594-603. DOI: 10.1007/s11064-010-0277-1. |
| [8] | Bringmann A, Grosche A, Pannicke T, et al. GABA and Glutamate Uptake and Metabolism in Retinal Glial (Müller) Cells[J]. Frontiers in Endocrinology, 2013, 4: 48. |
| [9] | López-Colomé AM, Martínez-Lozada Z, Guillem AM, et al. GlutamateTransporter-Dependent mTOR Phosphorylation in Müller Glia Cells[J]. Asn Neuro, 2012, 4(5): e00095. |
| [10] | Zhang XH, Feng ZH, Zhang Y. Pigment epithelium-derived factor protects the morphological structure of retinal Müller cells in diabetic rats[J]. International Journal of Ophthalmology, 2014, 7(6): 941-946. |
| [11] | Naskar R, Vorwerk CK, Dreyer EB. Concurrent downregulation of a glutamate transporter and receptor in glaucoma[J]. Investigative Ophthalmology & Visual Science, 2000, 41(7): 1 940-1 944. |
| [12] | Yu J, Huang X, Wu Q, et al. Effect of A (2A) receptor antagonist (SCH 442416) on the mRNA expression of glutamate aspartate transporter and glutamine synthetase in rat retinal Müller cells under hypoxic conditions in vitro[J]. Experimental & Therapeutic Medicine, 2012, 3(5): 803-806. |
| [13] | Tezel G, Wax MB. Glial modulation of retinal ganglion cell death in Glaucoma[J]. Journal of glaucoma, 2003, 12(1): 63-68. DOI: 10.1097/00061198-200302000-00014. |
| [14] | Harada T, Harada C, Nakamura K, et al. The potential role of glutamate transporters in the pathogenesis of normal tension glaucoma[J]. Journal of Clinical Investigation, 2007, 117(7): 1 763-1 770. DOI: 10.1172/JCI30178. |
| [15] | 钱志刚, 柯敏. Müller细胞在糖尿病视网膜病变中的作用[J]. 眼科新进展, 2010, 30(2): 189-192. |
| [16] | Zhang XH, Feng ZH, Zhang Y. Pigment epithelium-derived factor protects the morphological structure of retinal Müller cells in diabetic rats[J]. International Journal of Ophthalmology, 2014, 7(6): 941-946. |
| [17] | 李梦云, 李艳, 刘宏波, 等. 色素上皮衍生因子对高糖刺激下大鼠视网膜Müller细胞凋亡的影响[J]. 眼科新进展, 2014, 34(06): 526-529. |
| [18] | Mysona B. Effects of hyperglycemia and oxidative stress on the glutamate transporters GLAST and system xc-in mouse retinal Müller glial cells[J]. Cell & Tissue Research, 2009, 335(3): 477-488. |
 2016, Vol. 37
2016, Vol. 37

 ,
,