癫痫(epilepsy)主要是指由于脑部神经元发作性同步过度异常放电所引起的一种慢性脑神经功能障碍性临床综合征,世界上有超过6 000万人患有癫痫[1],其中以颞叶癫痫危害较为明显。虽然随着医学科学的发展,癫痫的治疗取得了很大的进展,但是迄今为止,癫痫的治疗方法仍然十分有限[2],究其原因多数在于癫痫发作种类繁多,即使同一类型癫痫,病因不同、发病机制及形式不同。因此,寻求一种有效模拟各种类型癫痫发病机制及形式的模型,对后续研究具有着重要的意义[3]。
本研究结合目前癫痫模型制备常用的技术手段,采用选择性局部阻断大鼠颞叶海马结构的血供制备一种新型的颞叶癫痫模型大鼠,通过对传统匹罗卡品组对比分析模型动物的表现、脑电图描记数据及模型动物的存活时间等,以期发现不同制备方法获得的癫痫模型的特征,为后续研究癫痫提供实验依据。
1 材料与方法 1.1 实验动物与试剂清洁级SD健康雄性大鼠, 武汉大学动物中心提供, 体重150-300 g。实验前饲养1周。试验分组:假手术对照组、匹罗卡品组(对照组)、选择性局部阻断颞叶海马血供组(实验组), 每组20只。匹罗卡品、氯化锂为Sigma公司产品。
1.2 癫痫模型的制作 1.2.1 匹罗卡品组先予氯化锂3 mg/kg腹腔注射, 18-24 h后腹腔注射硫酸阿托品1 mg/kg, 30 min后再腹腔注射匹罗卡品10 mg/kg; 观察发作情况, 如无Ⅴ级以上痫性发作, 继续注射匹罗卡品10 mg/kg, 每隔30 min重复注射1次, 直到出现癫痫持续状态(SE)为止。SE后90 min, 腹腔注射安定10 mg/kg。对照组腹腔注射等量生理盐水。
1.2.2 选择性局部阻断颞叶海马结构血供制备新型颞叶癫痫模型参照Albert的方法[4],制备过程如下:首先无菌条件下麻醉大鼠,将大鼠置于标准的离体定位仪上,中线切开头皮暴露颅骨,双边同步钻孔。灭菌记录电极,双边记录脑电变化。坐标仪实时指引下,准备定位基底动脉及其分支大脑后动脉、颈内动脉及其分支。在此基础上寻找局部的纵向海马动脉、脉络膜前动脉。采用改良的光化学法封闭局部的纵向海马动脉和/或脉络膜前动脉, 并在此基础上制作点燃杏仁核制备颞叶癫痫大鼠模型。排除不合作、死亡或手术过程中发现血管变异的大鼠。
1.3 行为学观察痫性发作行为学观察, 应用Vedio监测。癫痫发作行为评分采用Racine评分标准[5]。凡有连续至少3次Ⅳ或Ⅴ级发作的大鼠, 被认为是完全点燃。连续Ⅳ或Ⅴ级发作, 持续30 min以上, 被认为是癫痫持续状态。Ⅳ级以上发作为成功的癫痫自发发作模型。
1.4 脑电图观察在模型动物大脑植入电极接入刺激装置,参考电极放置右耳,连接于生理记录仪。脑电图资料用随机软件计算出痫样放电潜伏期、频率和波幅。根据Racine分级,Ⅳ级以上发作,脑电图在尖波或棘波的基础上出现阵发性或持续性异常放电为模型成功,以成功率表示。
1.5 颞叶区域神经元细胞凋亡检测(TUNEL染色)干预后14 d行TUNEL(TdT-mediated dUTP nick end labeling)检测细胞凋亡(n=4/组),具体过程按照试剂盒说明书进行。TUNEL是用来检测组织细胞在凋亡早期过程中细胞核DNA的断裂情况。脑组织皮层缺血区凋亡的神经细胞染色呈棕黄色颗粒。以假手术组作为阴性对照组。每张切片在同一皮层缺血区选择5个视野拍照,采用HPIAS 2000软件分析得各组大鼠缺血皮层脑组织染色阳性细胞计数(x±s)。
1.6 两组大鼠海马组织的电镜下形态学观察2.5%戊二醛固定4 h, 0.1 mol/L磷酸缓冲液漂洗3次, 1%锇酸后固定1.5 h, PBS漂洗3次, 梯度乙醇及丙酮脱水, EPON 812:丙酮(1:1)浸透及包埋, 常规制作超薄切片——铀、铅染色(醋酸双氧铀,枸橼酸铅), 随机选取10个视野,电镜下观察。
1.7 统计学方法各组数据以均数±标准差(x±s)表示,两样本间比较采用t检验,多样本间采用多因素的方差分析。所有统计计算由SPSS 13.0软件完成,P<0.05表示存在统计学差异。
2 结果 2.1 动物模型结果两组模型点燃率的比较见表 1。
| 表 1 两组癫痫模型点燃率的比较 |
20只大鼠,17只当天Ⅲ-Ⅴ级发作,1只死亡,2只未点燃,1周后死亡3只,有自发性癫痫的有14只。
2.1.2 新型颞叶癫痫模型20只大鼠,手术中死亡2只,16只当天Ⅲ-Ⅴ级发作,2只未成功,1周后死亡1只,有自发性癫痫的有15只(有自发性确认为制作成功)。
2.2 行为学观察分别于制备后的第14天时观察两组大鼠的癫痫行为表现。两组大鼠对假手术组及阴性对照组相比均有明显差异,表明制备的癫痫模型均比较成功。但是两组间相比,差异无统计学意义(P>0.05, 见表 2)。
| 表 2 两组大鼠癫痫点燃成功时癫痫发作情况 |
匹罗卡品组与实验大鼠脑电图监测异常率分别为95%、94%,所有有行为学异常表现的大鼠脑电图上均有异常表现,各组间比较差异无统计学意义(P>0.05),表明所制备的癫痫模型均有较好的脑电表现。
2.4 颞叶区域神经元细胞凋亡检测(TUNEL染色,图 1)
|
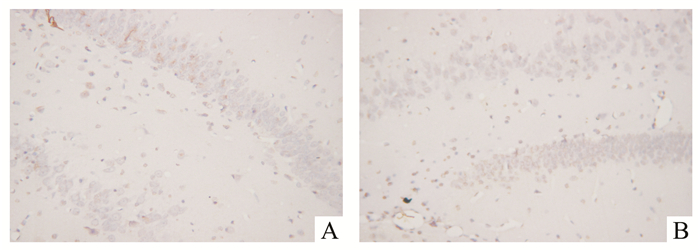
图 1 两组大鼠TUNEL染色结果(×200) A:对照组;B:实验组;与对照组相比,实验组大鼠海马区域凋亡的神经细胞明显增加 |
TUNELL检测显示,二组均可见染色棕黄色颗粒细胞,细胞形态不一,表明这些细胞系凋亡的细胞。图 1表明实验组细胞凋亡数目较对照组明显减少。
2.5 海马组织的电镜检查(图 2)
|
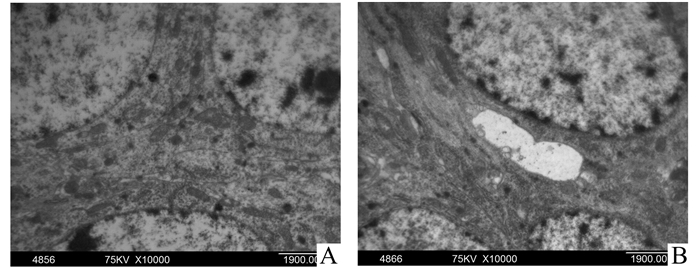
图 2 两组大鼠电镜下形态学观察(×10 000) A:对照组;B:实验组;与对照组相比,实验组大鼠的炎症水肿明显较对照组严重 |
匹罗卡品组大鼠脑组织内正常神经元有明、暗两种类型, 其细胞核大而圆, 基质中等电子密度无水肿表现,各细胞器结构完整,形态正常。细胞间结构清晰,无明显水肿积液。
实验组大鼠14 d后神经元变形、凋亡, 明暗神经元不易区分, 胞质中细胞器减少或变形, 结构不清。细胞间隙增宽,周围有大量水肿液呈低电子密度亮区,为神经细胞炎症水肿的典型表现。结果表明,选择性局部阻断颞叶海马结构血供制备新型颞叶癫痫模型可以更加准确地模拟颞叶癫痫发病机制,尤其是在致痫灶的研究上可能有着重要的临床意义。
3 讨论癫痫是威胁人类的常见疾病之一。癫痫的癫痫灶、神经元异常同步化放电和功能不全是癫痫的重要特征。目前,虽然尚未完全明确癫痫的发病机制,但传统的观点认为,神经元高度同步化异常放电是癫痫产生的根本原因。治疗方面,现代医学在癫痫研究领域取得了许多新进展,主要分为药物保守治疗和外科手术治疗[6]。药物治疗方面,目前人们已经研发出多种抗癫痫药物,包括在无数化合物实验中偶然发现的以及通过动物模型进行筛选得到的抗癫痫药物[7]。外科手术治疗的目的在于控制癫痫的发作,目前主要应用于血管性和肿瘤性病变继发性癫痫,但是其具有有创性、部分病例疗效不稳定,术后仍然需要长期药物治疗,尤其是致痫灶术前难以准确定位等缺点,限制了其应用。
较理想的癫痫模型应具有和人类癫痫相似的发生、发展过程,对于颞叶癫痫来说,杏仁核是癫痫模型点燃最敏感的区域[8]。较公认的癫痫模型至少应具备以下几点,以方便人类的研究:①具有癫痫发作的模拟“致痫灶”。其功能在于可以持续有效地引起癫痫发作来模拟癫痫发作的发作性、短暂性、重复性、刻板性等四大临床特点。且可维持一定的潜伏期来用于研究。②具有癫痫发作的病理学基础。如神经细胞的凋亡、丢失、反应性胶质细胞增生以及轴突丝状芽生和突触重建等。③制备的动物模型具有持续性。所制备的动物模型具有持续一定的时间,通常是数天到数周,这就要求模型大鼠大脑神经元具有持续的异常放电区域[9-12]。④其他条件,如比较高的成功率,低死亡率,操作简单,易于模拟等。
对于颞叶癫痫,既往研究多采用匹罗卡品动物模型,其可以有效地满足上述几个条件。本研究中我们改变了传统的研究癫痫发病机制的可能学说,从癫痫灶的局部脑血流变化特点着手,同时采用选择性局部阻断颞叶海马结构的血供,来制备颞叶癫痫模型大鼠。与传统的模型大鼠相比较,其可以通过局部阻断大鼠海马结构血供,来模拟癫痫发作的“致痫灶”,可以持续有效地引起癫痫发作来模拟癫痫发作的发作性、短暂性、重复性、刻板性等四大临床特点。且可维持一定的潜伏期来用于研究。另一方面,TUNEL及电镜检测发现了实验组大鼠海马区域的神经细胞的凋亡、丢失、反应性胶质细胞增生以及轴突丝状芽生和突触重建等癫痫发作的病理学基础。经过观察,我们制备的动物模型具有持续性,14 d以上仍然可观察到行为学发作及脑电异常放电,完全可以满足研究需要。
上述结果表明,通过选择性局部阻断颞叶海马结构的血供来制备的颞叶癫痫模型大鼠,可以有效地满足较理想癫痫动物模型的要求,更加有利于我们进行后续的研究,比如从正反两个方面分析血流供应、内皮功能、代谢变化等探索癫痫发作的不同阶段相应的脑血流变化是“因”是“果”,有利于从一个全新的视角来探索癫痫的发病机制和寻求一种新型的治疗癫痫的方法。
| [1] | Beghi E, Hesdorffer D. Prevalence of epilepsy--An unknown quantity[J]. Epilepsy, 2014, 55(7): 963-967. DOI: 10.1111/epi.12579. |
| [2] | Kobow K, Jeske I, Hildebrandt M, et al. Increased reelin promoter methylation is ass ociated with granule cell dispersion in human temporal lobe epilepsy[J]. Neuropathol Exp Neurol, 2009, 68(4): 356-364. DOI: 10.1097/NEN.0b013e31819ba737. |
| [3] | Racine RJ. Modification of seizure activity by electrical stimulation after ischarge threshold[J]. Electroencepha-logr Clin Neurephysiol, 1972, 32(3): 269-279. DOI: 10.1016/0013-4694(72)90176-9. |
| [4] | Barth AM, Mody I. Changes in hippocampal neuronal activity during and after unilateral selective hippocampal ischemia in vivo[J]. The Journal of Neuroscience, 2011, 31(3): 851-860. DOI: 10.1523/JNEUROSCI.5080-10.2011. |
| [5] | Racine RJ. Modification of seizure activity by electrical stimulation.Ⅱ. Motor seizure[J]. Electroenceph Clin Neurophysiol, 1972, 32(3): 281-294. DOI: 10.1016/0013-4694(72)90177-0. |
| [6] |
Shorvon SD, Perucca E, Fish DR, 等原著. 肖波, 刘献增, 龙小艳, 等译. 癫痫治疗学[M]. 第2版. 北京: 人民卫生出版社, 2010: 84.
Shorvon SD, Perucca E, Fish DR, et al. Original works. Xiao B, Liu XZ, Long XY, et al. Translation. Epilepsy Therapy[M]. Beijing: People's Health Publishing House, 2010: 84. |
| [7] | de Biase S, Gigli GL, Valente M, et al. Lacosamide for the treatment of epilepsy[J]. Expert Opin Drug Metab Toxicol, 2014, 10(3): 459-468. DOI: 10.1517/17425255.2014.883378. |
| [8] | Krishnan P, Chattopadhyay A, Saha M. Periventricular nodular heterotopia, frontonasal encephalocele corpus callosal dysgenesis and arachnoid cyst: A constellation of abnormalities in a child with epilepsy[J]. J Pediatr Neurosci, 2014, 9(3): 273-275. DOI: 10.4103/1817-1745.147591. |
| [9] | Soe NK, Lee SK. Unusual ictal foreign language automatisms in temporal lobe epilepsy[J]. J Epilepsy Res, 2014, 4(2): 78-81. DOI: 10.14581/jer.14016. |
| [10] | Ambhore A, Teo SG, Omar AR, et al. Electrocardiography series importance of QT interval in clinical practice[J]. Singapore Med J, 2014, 55(12): 607-612. DOI: 10.11622/smedj.2014172. |
| [11] | Ibekwe RC, Chidi NA, Ebele AA, et al. Co-Morbidity of attention deficit hyperactivity disorder (ADHD) and epilepsy in children seen in university of Nigeria teaching hospital enugu: prevalence, clinical and social correlatesJ][J]. Niger Postgrad Med J, 2014, 21(4): 273-278. |
| [12] | Méndez-Armenta M, Nava-Ruíz C, Juárez-Rebollar D, et al. Oxidative stress associated with neuronal apoptosis in experimental models of epilepsy[J]. Oxid Med Cell Longev, 2014(3): 571-573. |
 2018, Vol. 39
2018, Vol. 39


