子宫内膜癌(endometrial cancer,EC)是好发于围绝经期和绝经后女性、导致患者死亡的第三位常见妇科恶性肿瘤(仅次于卵巢癌和宫颈癌),世界范围内每年有接近20万的新发病例[1]。微小RNA (microRNA,miRNA)是近年癌症研究的热点,miRNA的异常表达与肿瘤发生发展密切相关。近年来有关EC miRNA的表达特点及功能研究逐渐增多,但miRNA在EC发病中的功能与作用机制尚缺乏深入探讨。研究发现miR-200家族在EC中高表达,在EC发生过程中起重要的促进作用[2]。miR-200家族包包括miR-141、miR-200a、miR-200b、miR-200c和miR-429五个基因。有研究报道子宫内膜样腺癌中miR-141和miR-200a高表达组的PTEN失表达率更高,且miR-141与miR-200a的表达呈正相关,而miR-200a与PTEN表达呈显著负相关,这表明miR-141和miR-200a可能通过对抑癌基因PTEN的靶向调控,参与EC的形成及演进[2, 3]。另有研究报道,EC组织中miR-200b抑制TIMP2 mRNA和蛋白质的表达,间接增强MMP-2的表达[4]。
新近研究证实与子宫内膜样腺癌相比较,未分化EC中E-cadherin表达水平显著下调,E盒结合锌指蛋白1(ZEB1)过表达,表达率为62%,而作为ZEB1靶基因的miRNA-200家族表达下调[5]。在子宫内膜癌、乳腺癌、直肠癌和卵巢癌中,miR-200c在分化好的癌细胞中高度表达,而在分化差的癌细胞中表达水平极低[5-8]。以上研究结果提示未分化EC中ZEB1的过表达与上皮-间质过渡(EMT)相关,ZEB1可能是miR-200c的直接靶点。本研究旨在探讨miR-200c和ZEB1的表达与EC恶性表型的相关性及其调控机制。
1 材料与方法 1.1 主要材料与试剂Lipofectamine 2000(Lipo2000)、TRIzol、miRNA cDNA逆转录试剂盒、Opti-MEM I培养液(Invitrogen),DMEM培养液(GIBCO)。SYBR GREEN (TOYOBO),Has-miR-200c mimics、miRNA阴性对照(Negative Control)(上海吉玛)。ZEB1兔抗人多克隆抗体和E-cadherin鼠抗人单克隆抗体为Santa Cruz公司产品。
1.2 试验方法及步骤 1.2.1 细胞培养及转染ER阳性子宫内膜癌细胞株(Ⅰ型EC细胞) Ishikawa和RL95-2,ER阴性子宫内膜癌细胞株(Ⅱ型EC细胞) HEC-1A和AN3CA购自美国ATCC,用含10%胎牛血清、100 U/ml青霉素和100 μg/ml链霉素A的DMEM/F12培养液培养,用含10% FBS RPMI 1640培养基培养在37 ℃,5% CO2条件下培养。
试验分为2组:实验组(miRNA mimics转染组)和NC组(miRNA阴性对照转染组),转染终浓度50 nmol/L。转染前24 h按3×105/孔密度接种6孔板,37 ℃培养过夜后按照Lipo 2000说明书进行转染。转染完成后继续培养进行后续实验。
1.2.2 转染效率检测转染FAM-Transfection Control 24 h后,取约1×106个细胞,PBS洗涤后重悬,立即避光行流式细胞仪检测。
1.2.3 实时荧光定量PCR检测miR-200c的表达转染48 h后,用Trizol试剂法提取总RNA。A260/A280为1.8-2.0之间方可用于检测。取500 ng总RNA做逆转录反应。试剂盒提供RT及qPCR通用引物,操作步骤按试剂盒说明书进行。反应总体积为10 μl,包含cDNA模板1 μl (1:10稀释)、qPCR通用引物1 μl、miR-200c特异性的上游引物5′-UAAUACUGCCGGGUAAUGGA-3′,下游引物5′-CCAGTGCAGGGTCCGAGGT-3′(由上海生工公司合成)、SYBR-GREEN Mi×5 μl、ddH2O 2 μl。反应条件:95 ℃变性3 min,95 ℃作用5 s,63 ℃作用35 s,共40个循环。以U6为内参照,上游引物序列为:5′-CGCAAGGATGACACGCAAAC-3′。结果分析采用2-△△t方法,以此值表示miR-200c的表达水平。
1.2.4 Western blot法检测ZEB1和E-cadherin蛋白的表达收获分组处理的细胞,裂解细胞提取总蛋白并蛋白定量(采用考马斯亮蓝G250法蛋白定量),灌制10%SDS-PAGE凝胶,每孔上样量50 μg,经电泳、转膜、封闭,依次与ZEB1和E-cadherin抗体(稀释度分别1:500和1:500)、碱性磷酸酶标记的二抗(稀释度1:500)反应1 h,用TBST液在室温洗涤15 min/次,反复4次。免疫反应通过增强化学发光试剂ECL试剂可视,膜采用Kodak XAR胶片曝光。
1.2.5 CCK-8检测肿瘤细胞增殖按照CCK-8试剂盒说明书进行。将细胞按照2 000个细胞/100 μl接种于96孔培养板,每组设3个复孔,24 h后转染。转染48 h后每孔加入10 μl CCK-8试剂,至培养箱孵育1-2 h,测定A450值,以此反映细胞增殖情况。
1.2.6 Transwell实验检测肿瘤细胞侵袭力2×105个细胞悬浮在200 μl无血清培养液中,并种于8 μm孔、6.5 mm多聚碳酸Transwell滤膜上,小室预先包被Matrigel胶,含10% FBS培养液加入下室。将细胞放置于37 ℃,5% CO2条件下培养48 h以让细胞侵袭。黏附在滤膜下面的细胞于4%甲醛溶液中室温固定30 min,用结晶紫染色,在显微镜下计数膜下面的细胞。每个膜计算5个视野细胞的总数。
1.3 统计学处理统计软件采用SPSS 17.0版本。数据结果以均数±标准差的方式显示,多组间均数比较采用单因素方差分析(ANOVA),P < 0.05认为差异有统计学意义。
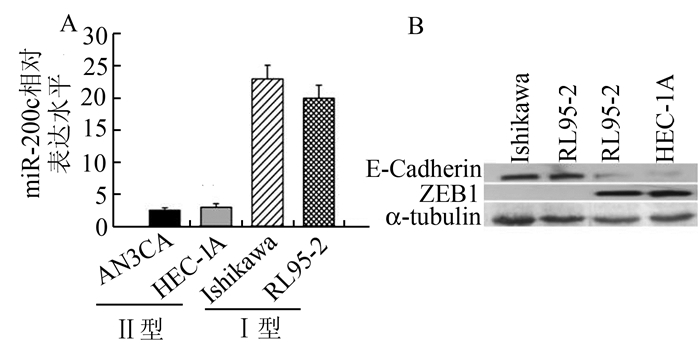
2 结果 2.1 miR-200c、ZEB1和E-cadherin在Ⅰ型(Ishikawa和RL95-2)和Ⅱ型(HEC-1A和AN3CA) EC细胞中的表达及其相关性实时定量RT-PCR结果发现,与Ⅰ型EC细胞(Ishikawa和RL95-2)相比,miR-200c在Ⅱ型EC细胞(HEC-1A和AN3CA)中显著低表达, 表达丰度分别为2.63±0.41和2.83±0.47,如图 1A所示。Western blot结果表明,ZEB1在Ⅰ型EC细胞Ishikawa和RL95-2中不表达,而在Ⅱ型EC细胞HEC-1A和AN3CA中高度表达,表达丰度分别为0.52±0.34和0.81±0.45,而E-cadherin在中Ⅰ型EC细胞高度表达,表达丰度分别为1.58±0.44和1.01±0.36,而在Ⅱ型EC细胞中极低表达,如图 1B所示。
|
图 1 miR-200c、ZEB1和E-cadherin在Ⅰ型和Ⅱ型EC细胞中的表达 A:实时定量RT-PCR法检测miR-200c在Ⅰ型和Ⅱ型EC细胞株的表达(P < 0.05);B:Western blot法检测ZEB1和E-cadherin在Ⅰ型和Ⅱ型EC细胞株的表达水平(P < 0.05) |
将三者进行相关性分析表明,在Ⅱ型EC细胞中miR-200c与ZEB1呈显著负相关,与E-cadherin呈正相关。
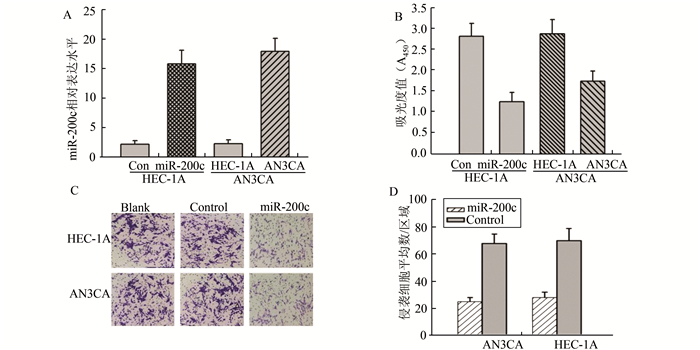
2.2 miR-200c过表达抑制Ⅱ型EC细胞增殖和侵袭选择Ⅱ型EC细胞系HEC-1A和AN3CA细胞作为细胞模型,用pre-miR-200c或阴性对照转染后,实时RT-PCR法检测miR-200c的表达情况。转染pre-miR-200c后miR-200c在HEC-1A和AN3CA中明显高度表达(图 2A)。
|
图 2 miR-200c过表达抑制Ⅱ型EC细胞增殖和侵袭 A:pre-miR-200c转染后实时RT-PCR法检测Ⅱ型EC细胞系HEC-1A和AN3CA中miR-200c的表达情况(P < 0.05);B:miR-200c处理明显抑制HEC-1A和AN3CA细胞增殖(P < 0.05);C和D:miR-200c处理明显抑制HEC-1A和AN3CA细胞侵袭(P < 0.05) |
与阴性对照相比,miR-200c过表达明显抑制HEC-1A和AN3CA细胞增殖和侵袭能力(图 2B和图 2C-D)。
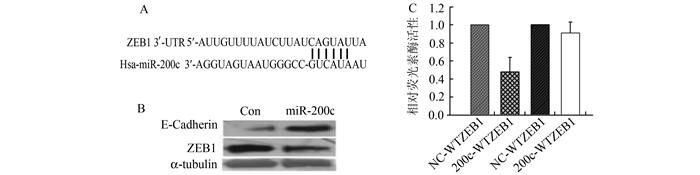
2.3 miR-200c调控Ⅱ型EC细胞E-Cadherin的表达为了明确miR-200c与靶基因ZEB1 3’-UTR区域功能性种子序列之间的相互作用(图 3A),miR-200c过表达后明显降低AN3CA细胞中ZEB1的表达并增加E-cadherin的表达水平(图 3B)。荧光素报告实验表明miR-200c前体转染AN3CA细胞后明显减低野生型报告载体的荧光素酶活性,而突变型报告载体荧光素酶活性无变化(图 3C)。以上结果表明ZEB1是miR-200c的直接靶点,miR-200c负性调控Ⅱ型EC细胞ZEB1的表达,参与肿瘤EMT。
|
图 3 miR-200c调控Ⅱ型EC细胞E-Cadherin的表达 A. miR-200c与靶基因ZEB1 3′-UTR区域功能性种子序列之间的相互作用;B. Pre-miR-200c处理AN3CA细胞后Western Blot法检测ZEB1和E-cadherin的表达;C.荧光素酶报告实验验证miR-200c和ZEB1之间的靶点关系 |
EC是女性最常见的恶性肿瘤之一,占女性生殖道恶性肿瘤的20%-30%,且发病率逐年上升,有年轻化趋势[1]。EC的发病原因迄今尚不明确,根据临床病理特点(发病机制和生物学行为特点)将EC分为两型[3]:雌激素依赖型(Ⅰ型)和非雌激素依赖型(Ⅱ型)。Ⅰ型绝大部分为子宫内膜样癌,少部分为黏液腺癌,常与雌激素异常刺激有关,多见于围绝经期女性,肿瘤分化好,预后相对良好,但仍有约15%的病例术后复发,对各种治疗效果差;而Ⅱ型病理类型为非子宫内膜样癌,主要为浆液性癌和透明细胞癌,少部分为未分化子宫内膜癌,多见于绝经后老年女性,侵袭性强,预后差。目前对两型EC发病的分子机制的差异性已有所报道,子宫内膜样癌主要因抑癌基因PTEN失活,微卫星不稳定性,PIK3CA、KRAS和β-catenin突变所致;非子宫内膜样癌的突出特点是p53基因突变及HER2过表达[3]。然而目前关于这些分子改变之间内在的关联性,特别是其本身发生的机制及如何相互协同作用诱导癌的形成和演进以及是否存在其他分子机制如miRNA等研究尚不多。
王颖等研究报道Ⅰ型EC有相对特异的miRNA表达谱。miR-200a、miR-205、miR-141、miR-43、miR-145在Ⅰ型癌中变化显著,而在Ⅱ型EC中变化不显著,但miR-449a/b在Ⅱ型EC中表达下调[3, 9],以上这些结果提示Ⅰ/Ⅱ型EC发病中发挥作用的miRNA不尽相同。Lee等采用人miRNA芯片检测甲醛固定、石蜡包埋的子宫内膜样腺癌和正常子宫内膜组织中miRNA表达谱,结果也表明miR-200a,miR-200b,miR-141,miR-182和miR-205在子宫内膜样腺癌组织中高度表达,抑制miR-200b的表达可增加EC顺铂细胞毒性[10]。
ZEB1是E-cadherin的转录抑制因子,而ZEB1基因表达又受miR-200家族(miR-200s)的调节。Singh等研究报道ZEB1在高度侵袭性内膜癌,如G3子宫内膜腺癌、子宫浆液性癌和恶性混合性苗勒氏管肿瘤的上皮性肿瘤细胞中异常表达,而在低级别子宫内膜腺癌(Ⅰ型EC)的肿瘤间质中高度表达。当ZEB1在上皮性肿瘤细胞中异常表达时,E-cadherin表达被阻遏,这种负相关与肿瘤侵袭潜能增加相关[11]。有研究表明在Ⅱ型EC中miR-200s表达水平下调导致ZEB1基因表达增加,从而使E-cadherin水平显著降低,促进EMT,使细胞失去极性及细胞间连接,增进转移潜能,预后变差[5]。miR-200c与miR-200家族的其他成员通过直接靶向ZEB1和ZEB2,增加E-cadherin的表达,从而抑制EMT[12]。miR-200c的缺失常常在EMT的癌细胞中被观察到。恢复miR-200c的表达不仅减低乳腺癌干细胞样特性、细胞迁移和侵袭能力,而且增加乳腺癌细胞对紫杉醇类药物敏感性[7]。
本研究结果显示,miR-200c和E-cadherin在Ⅰ型EC细胞系中都高度表达,而在Ⅱ型EC细胞系中低表达;ZEB1在Ⅰ型EC细胞系中不表达或低表达,而在Ⅱ型EC细胞系中高度表达。将三者进行相关性分析表明,在Ⅱ型EC细胞系中miR-200c表达与ZEB1表达呈显著负相关,与E-cadherin表达呈正相关。进一步研究表明miR-200c过表达明显抑制Ⅱ型EC细胞增殖和侵袭,ZEB1是miR-200c的直接靶点,miR-200c负性调控Ⅱ型EC细胞ZEB1的表达,参与肿瘤EMT。因此我们推论miR-200c通过调控ZEB1的表达实现对Ⅱ型子宫内膜癌细胞增殖和侵袭的抑制,从而成为子宫内膜癌侵袭治疗的新靶点。miR-200c和ZEB1的联合检测对子宫内膜癌的分型诊断和预后评估具有指导意义。
| [1] | Okuda T, Sekizawa A, Purwosunu Y, et al. Genetics of endometrial cancers[J]. Obstet Gynecol Int, 2010, 2010: 984013. |
| [2] |
刘麒薇, 杨敏, 童晓文, 等. 微小RNA与子宫内膜癌相关性的研究进展[J].
国际妇产科学杂志, 2014, 41 (4): 401-404.
Liu QW, Yang M, Tong XW, et al. Related research of endometrial cancer and microRNA[J]. J Int Obstet Gynecol, 2014, 41(4): 401-404. |
| [3] |
王颖, 阿迪拉·斯依提, 张晓明, 等. 子宫内膜癌微小RNA的表达特点及其临床意义[J].
中华病理学杂志, 2014, 43 (2): 88-94.
Wang Y, Adila STM, Zhang XM, et al. MicroRNA expression signature profile and its clinical significance in endometrioid carcinoma[J]. Chin J Pathol, 2014, 43(2): 88-94. |
| [4] |
刘霞, 夏伟, 邵宁生, 等. 微小RNA-200b对子宫内膜癌细胞中TIMP2基因表达的影响[J].
中华妇产科杂志, 2013, 48 (11): 867-869.
Liu X, Xia W, Shao NS, et al. The effect of miRNA-200c on expression of TIMP2 in endometrial carcinoma cells[J]. Chin J obstel Gynecol, 2013, 48(11): 867-869. |
| [5] | Romero-Pérez L, López-García MÁ, Díaz-Martín J, et al. ZEB1 overexpression associated with E-cadherin and microRNA-200 downregulation is characteristic of undifferentiated endometrial carcinoma[J]. Mod Pathol, 2013, 26(11): 1514-1524. DOI: 10.1038/modpathol.2013.93. |
| [6] | Panda H, Pelakh L, Chuang TD, et al. Endometrial miR-200c is altered during transformation into cancerous states and targets the expression of ZEBs, VEGFA, FLT1, IKKβ, KLF9, and FBLN5[J]. Reprod Sci, 2012, 19(8): 786-796. DOI: 10.1177/1933719112438448. |
| [7] | Howe EN, Cochrane DR, Richer JK. Targets of miR-200c mediate suppression of cell motility and anoikis resistance[J]. Breast Cancer Res, 2011, 13(2): R45. DOI: 10.1186/bcr2867. |
| [8] | Hur K, Toiyama Y, Takahashi M, et al. MicroRNA-200c modulates epithelial-to-mesenchymal transition (EMT) in human colorectal cancer metastasis[J]. Gut, 2013, 62(9): 1315-1326. DOI: 10.1136/gutjnl-2011-301846. |
| [9] |
薛纪森, 张乾, 李晓琳, 等. miR-449a/b在Ⅱ型子宫内膜癌中表达下调[J].
医学研究杂志, 2012, 41 (11): 103-107.
Xue JS, Zhang Q, Li XL, et al. miR-449a/b is downregulated in type Ⅱ endometrial carcinoma[J]. Journal of Medical Research, 2012, 41(11): 103-107. |
| [10] | Lee TS, Jeon HW, Kim YB, et al. Aberrant microRNA expression in endometrial carcinoma using formalin-fixed paraffin-embedded (FFPE) tissues[J]. PLoS One, 2013, 8(12): e81421. DOI: 10.1371/journal.pone.0081421. |
| [11] | Singh M, Spoelstra NS, Jean A, et al. ZEB1 expression in type Ⅰ vs type Ⅱ endometrial cancers: a marker of aggressive disease[J]. Mod Pathol, 2008, 21(7): 912-923. DOI: 10.1038/modpathol.2008.82. |
| [12] | Radisky DC. miR-200c at the nexus of epithelial-mesenchymal transition, resistance to apoptosis, and the breast cancer stem cell phenotype[J]. Breast Cancer Res, 2011, 13(3): 110. DOI: 10.1186/bcr2885. |
 2016, Vol. 37
2016, Vol. 37

