诸多病理状态及手术应激不但可引起肠缺血再灌注损伤(Ischemia reperfusion injury,IRI),还因伴有肠道菌群移位、氧自由基产生、炎症介质释放等多重因素,导致远隔器官的受损,其中以肺组织最为敏感,早期即出现急性肺损伤(acute lung injury, ALI),严重时甚至出现急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)[1]。新近研究证实作为重要的内源性抗缺血再灌注损伤措施,缺血后处理(ischemia postconditioning,IPO)可通过缺血后给予短暂缺血/灌注处理从而显著减轻脏器的缺血再灌注损伤[2],但具体作用机制尚待明确。PI3K/Akt信号通路作为体内调节细胞生长的重要信号通路,在诸多生理病理环节中均起着重要的作用[3],而其在缺血后处理减轻肠缺血再灌注引起的肺损伤的病程中的具体作用机制亟待阐明,本研究拟通过构建肠缺血后处理及肠缺血再灌注模型研究PI3K/Akt通路在此过程中的具体机制。
1 材料与方法 1.1 材料与试剂SPF级雄性C57BL/6J小鼠,9-12周,体重25-29 g,购于湖北省实验动物中心。丙二醛(MDA),超氧化物歧化酶(SOD)试剂盒均购于Sigma公司,兔抗鼠PI3K、Akt和磷酸化Akt (p-Akt)单克隆抗体购于Cell Signal公司。
1.2 模型制备及实验方法 1.2.1 模型制备30只小鼠C57随机数字表法分为3组(n=10):假手术组(S组)、缺血再灌注组(IR组)和缺血后处理+缺血再灌注组(IPO组)。参照文献复制肠缺血再灌注模型[4],腹腔注射2%戊巴比妥钠麻醉,固定后腹部正中脱毛,常规消毒铺巾后取正中切口进腹,分离肠系膜上动脉(superior mesenteric artery, SMA)。S组分离SMA后不作处理,IR组和IPO组用微动脉夹夹闭SMA根部,确定血管搏动消失、肠壁苍白,SMA血流阻断后关腹。夹闭SMA 45 min后经原切口进腹,IR组松开动脉夹恢复血供。IPO组给予3个再灌注30 s、缺血30 s的循环后恢复血供,所有小鼠在再灌注2 h时采集血标本后处死,留取肺组织。血液室温静置10-20 min,1 000 g离心20 min,取上清冻存;肺组织分为三部分分别冻存、固定和称重。
1.2.2 肺组织病理组织学观察病理学检测取右肺下叶组织,4%多聚甲醛固定,常规脱水渗透石蜡包埋后切片,切片厚度为5 μm。HE染色后200倍光镜下观察肺组织病理学变化。采用Smith评分法根据肺组织水肿、肺泡及肺间质炎症、肺泡及肺间质出血、肺不张及透明膜形成四个方面变化进行判定,每项按0-4分进行半定量分析,无损伤为0分,病变范围 < 25%为1分,病变范围在25%-50%的为2分,病变范围在50%-75%的为3分,病变满视野为4分,总评分为每项之和,每个标本取2个不同切片10个视野的总评分后取均值。
1.2.3 肺组织湿干重比(W/D)取右肺中叶,吸水纸快速吸干组织表面水分及血液,用天平测得肺湿重,置于80 ℃烤箱72 h后,再称量肺干重,计算湿干重比(W/D)。
1.2.4 血清SOD、MDA测定SOD活性检测试剂盒(Sigma公司) WST法步骤操作440 nm处的OD值,从而测得SOD活性;脂类过氧化作用(MDA)检测试剂盒(Sigma公司)硫代巴比妥酸法操作测波长530 nm OD值,得到MDA的含量。
1.2.5 Western Blot法检测蛋白表达水平取肺组织称重,按比加入裂解液匀浆,低温离心取上清,采用BCA法测蛋白浓度。加上样缓冲液并煮沸10 min,进行10%SDS-PAGE凝胶电泳,应用电转仪将电泳分离后的蛋白转移至PDVF膜,5%脱脂奶粉室温封闭1 h,然后用兔抗鼠PI3K、Akt和磷酸化Akt (p-Akt)单克隆抗体(稀释度1:1 000,Cell Signal公司,美国)分别4 ℃孵育过夜。次日用羊抗兔二抗(稀释度1:10 000,LI-COR公司,美国)室温孵育1 h,ODYSSEY双色红外激光成像系统扫描。以目的蛋白条带灰度值与β-Actin条带灰度值的比值反映目的蛋白的表达。
1.3 统计学分析所有数据采用GraphPad Prism 5.0统计学软件进行分析,计量资料用x±s表示,计数资料多组间比较先采用单因素方差分析(One-way ANNOVA),两组间比较再采用q检验。P<0.05为差异有统计学意义。
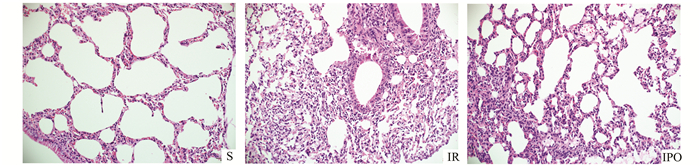
2 结果 2.1 肺组织病理学观察S组肺泡及肺间质基本正常;IR组正常肺泡结构破坏,肺泡及肺间质出血,并可见水肿液;IPO组肺泡结构部分破坏,肺泡及间质有少量水肿液。Smith肺组织病理学评分显示IR组损伤程度较之于S组显著增加,IPO处理后肺组织损伤程度显著减轻,但显著高于S组(P<0.05)(见图 1及表 1)。
|
图 1 肺组织病理学变化(HE×200) |
| 表 1 肺组织损伤程度、湿干重比结果(n=10, x±s) |
IR组肺组织湿干重比S组显著增高(P<0.05),IPO处理后肺组织的湿干重较之于IR组显著降低(P<0.05),但较之于S组仍显著增高(P<0.05)(见表 1)。
2.3 血清SOD活性、MDA含量IR组小鼠血清SOD活性较之于S组显著降低(P<0.05),IPO处理后SOD活性高于IR组,而低于S组(P<0.05)。IR组小鼠MDA含量较之于S组显著增高(P<0.05);IPO处理后MDA含量较之于IR组显著降低,但高于S组(P<0.05)(见表 2)。
| 表 2 血清SOD、MDA水平比较(n=10, x±s) |
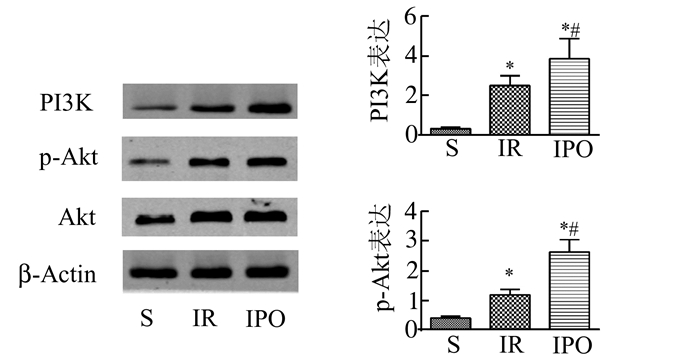
IR组PI3K、p-Akt蛋白表达含量较之于S组显著增高(P<0.05);与IR及S组相比,IPO组PI3K、p-Akt蛋白表达均显著增高(P<0.05),而三组间Akt含量无统计学差异(P>0.05)(见图 3和表 4)。
|
图 2 肺组织中PI3K、p-Akt蛋白表达(Western blot) 与对照组相比, *P<0.05;与IR组相比, #P<0.05 |
肠缺血再灌注(intestinal ischemia-reperfusion, IIR)损伤可因急性失血性休克、严重多发性创伤、肠梗阻、肠套叠、脓毒血症、器官移植手术等诸多因素引起[6]。IIR导致的黏膜屏障的破坏使细菌和内毒素发生易位从消化道进入血液,最终可能造成SIRS及多器官功能障碍综合征(multiple organ dysfunction syndrome, MODS)。循环血液中的炎症介质(包括活性氧簇、细胞因子和细菌性内毒素)的出现与IIR所致的远隔脏器损伤密切关联。IIR引起的肺损伤是一种多因素参与的复杂的病理过程,其主要发生于再灌注期间,随着再灌注时间延长,肺毛细血管通透性进行性增加。本研究亦证实遭受肠缺血再灌注处理的小鼠肺泡结构破坏,肺泡及肺间质出血,肺间质及肺泡水肿以及大量的中性粒细胞浸润,肺毛细血管内皮充血,内皮细胞肿胀、脱落、空泡变性等,肺组织水肿程度显著。
体内氧化系统和抗氧化系统的失衡是缺血再灌注损伤的一个重要原因,缺血缺氧激活各个氧化系统产生大量活性氧簇(ROS),超过内源性抗氧化系统清除能力,使SOD活性显著降低;同时,大量的ROS攻击线粒体、细胞膜等生物膜磷脂中的多不饱和脂肪酸引起脂质过氧化形成脂质过氧化物MDA[7]。本研究通过对野生C57BL/6J小鼠钳闭SMA 45 min开放2 h建立肠缺血再灌注模型,结果表明血清中的MDA含量显著增高,SOD活性下降,提示体内氧化系统和抗氧化系统失衡产生大量的ROS,出现氧化应激,从而导致急性肺脏损伤。
PI3K/Akt是体内参与细胞生长、增殖、分化的重要通路,正常细胞中PI3K以无活性的P85-P110复合物形式存在于胞质中。在发生缺血缺氧时,PI3K受到刺激而激活并由p110催化生成第二信使PIP3,PIP3与Akt结合后转位于细胞膜并改变构象获得催化活性催化自身Ser473和Thr308磷酸化,激活/抑制Bad、Caspase9、mTOR等下游因子,从而介导多种细胞增殖、迁移等,减少因缺血再灌注引起的细胞凋亡,从而起到保护作用[8]。本研究发现IR组PI3K、p-Akt蛋白的表达显著高于S组,而肺组织损伤加重,提示损伤后即有通道激活但是激活程度不足以对抗此期间缺血再灌注释放的ROS、炎性因子等引起的损伤。
IPO是临床可操作性强、效果明确的保护性措施,可显著减轻组织缺血再灌注损伤[9]。缺血后处理时释放的大量内源性活性物质及其炎性介质在受体水平发挥调节作用,如自由基、一氧化氮、白细胞介素、缓激肽、钙等。研究表明缺血后处理能通过减少氧化应激及线粒体内钙聚集,减少炎症因子释放、改善内皮细胞功能等途径而发挥保护作用[10],但是IPO可以减少氧化应激的具体分子机制尚未清楚。本研究中IPO组小鼠在夹闭SMA 45 min后给予3个循环开放/夹闭的操作处理,小鼠肺组织湿干重比、肺组织损伤程度较IR组均有显著降低,SOD活性显著增高,PI3K、p-Akt蛋白表达水平较之于IR组进一步增高,表明IPO的保护作用分子机制可能通过开放/夹闭的循环操作处理上调PI3K、Akt的表达,通过激活PI3K/Akt信号通路从而发挥减轻肠缺血再灌注导致的肺脏损伤。
综上所述,缺血后处理可减轻肠缺血再灌注引起的肺损伤,其机制可能与激活PI3K/Akt信号通路有关。
| [1] | Zhang F, Li ZL, Xu XM, et al. Protective effects of icariin-mediated SIRT1/FOXO3 signaling pathway on intestinal ischemia/reperfusion-induced acute lung injury[J]. Molecular Medicine Reports, 2015, 11(1): 269-276. |
| [2] | Sun Q, Meng QT, Jiang Y, et al. Protective effect of ginsenoside Rb1 against intestinal ischemia-reperfusion induced acute renal injury in mice[J]. PLoS One, 2013, 8(12): e80859. DOI: 10.1371/journal.pone.0080859. |
| [3] | Liu C, Shen Z, Liu Y, et al. Sevoflurane protects against intestinal ischemia-reperfusion injury partly by phosphatidylinositol 3 kinases/Akt pathway in rats[J]. Surgery, 2015, 157(5): 924-933. DOI: 10.1016/j.surg.2014.12.013. |
| [4] | Wen SH, Ling YH, Li Y, et al. Ischemic postconditioning during reperfusion attenuates oxidative stress and intestinal mucosal apoptosis induced by intestinal ischemia/reperfusion via aldose reductase[J]. Surgery, 2013, 153(4): 555-564. DOI: 10.1016/j.surg.2012.09.017. |
| [5] | Smith KM, Mrozek JD, Simonton SC, et al. Prolonged partial liquid ventilation using conventional and high-frequency ventilatory techniques: gas exchange and lung pathology in an animal model of respiratory distress syndrome[J]. Critical Care Medicine, 1997, 25(11): 1888-1897. DOI: 10.1097/00003246-199711000-00030. |
| [6] | Teke Z, Sacar M, Yenisey C, et al. Activated protein C attenuates intestinal reperfusion-induced acute lung injury: an experimental study in a rat model[J]. Am J Surg, 2008, 195(6): 861-873. DOI: 10.1016/j.amjsurg.2007.06.025. |
| [7] | 孟庆涛, 孙倩, 江莹, 等. 缺血后处理对小鼠肠缺血再灌注致肾损伤时Nrf2蛋白表达的影响[J]. 中华麻醉学杂志, 2012, 32(4): 504-507. |
| [8] | Chen S, Chen Y, Peng Y, et al. Role of PI3K/Akt signaling in the protective effect of magnesium sulfate against ischemia-perfusion injury of small intestine in rats[J]. Chinese Medical Journal, 2010, 123(11): 1447-1452. |
| [9] | Weng X, Wang L, Chen Z, et al. Ischemic postconditioning inhibits apoptosis in an in vitro proximal tubular cell model[J]. Molecular Medicine Reports, 2015, 12(1): 99-104. |
| [10] | Zhu M, Feng J, Lucchinetti E, et al. Ischemic postconditioning protects remodeled myocardium via the PI3K-PKB/Akt reperfusion injury salvage kinase pathway[J]. Cardiovasc Res, 2006, 72(1): 152-162. DOI: 10.1016/j.cardiores.2006.06.027. |
 2016, Vol. 37
2016, Vol. 37

