2. 武汉大学中南医院 肿瘤放化疗科 湖北 武汉 430071
2. Dept. of Radiation and Medical Oncology,Zhongnan Hospital of Wuhan University, Wuhan 430071 , China
以顺铂(DDP)为基础的化疗可以使卵巢癌患者生存获益; 但是,由于卵巢癌的顺铂耐药,一半晚期患者死于化学治疗无法控制的远处转移。目前,临床尚无逆转顺铂耐药药物; 因此,逆转卵巢癌顺铂耐药药物的研发迫在眉睫。
卵巢癌耐药原因复杂。基本可概括为三方面:一是卵巢癌细胞内顺铂浓度的减少; 二是卵巢癌细胞DNA损伤修复能力的提高; 三是肿瘤细胞内凋亡途径的改变。最近的研究显示NF-κB信号激活在卵巢癌细胞顺铂耐药机制中发挥重要作用。研究[1-3]已经证实NF-κB与卵巢癌的发生、发展及治疗耐药关系密切,NF-κB抑制剂是理想的抗癌药物增敏剂[4]。NF-κB可以增加多西他赛耐药卵巢癌细胞株SKOV3高表达凋亡抑制蛋白(CFLAR、XIAP、 BCL2和BCL2L1),促使细胞逃避凋亡[5]。Mabuchi报道[6]:相对于顺铂敏感细胞株A2780,顺铂耐药株Caov-3的磷酸化IκBα和NF-κB活性均显著增高; 且顺铂处理后,两株细胞的磷酸化IκBα和NF-κB活性都降低,但是A2780组降低更显著; IκBα磷酸化抑制剂BAY 11-7085可以增强顺铂对Caov-3毒性。
祖国传统医药为筛选NF-κB活性抑制剂提供了良好的数据库。暗罗属(Polyalthia) 是番荔枝科Annonaceae一个较大的属,全世界约120种,分布于东半球的热带及亚热带地区。我国有17种,分布于广东、云南、西藏和台湾等省。陵水暗罗P.nemoralis A.DC.是该属的一种,主要分布在海南和广东省。民间用于治疗疟疾、肝炎、淋巴节炎、肺炎和梅毒等[7]。1980年我国天然药物化学家韩公羽教授就对陵水暗罗有效成分进行了研究[8]; 韩教授从陵水暗罗中提取和鉴定了一种天然含锌化合物:暗罗素(Zincpolyanemine,ZPT)。暗罗素中含有锌离子,锌离子是一种与肿瘤关系非常密切的金属离子。我们前期报道显示锌离子可以抑制多种人肿瘤细胞的NF-κB活性。本研究将探讨暗罗素对顺铂耐药人卵巢癌细胞的逆转效应和初步机制
1 材料与方法 1.1 试验材料 1.1.1 细胞株人卵巢癌细胞株A2780和耐药株A2780/DDP获赠于华中科技大学同济医学院附属协和医院妇产科王泽华教授,由武汉大学肿瘤研究所保存。
1.1.2 试剂与仪器陵水暗罗提取物暗罗素购自于Sigmal公司;MTS试剂盒购置于promega公司(CellTiter 96®AQueous Non-Radiotive Cell Proliferatim Assay,普洛麦格北京生物技术有限公司);小鼠抗人p65抗体、抗Bcl-2抗体和小鼠抗人GAPDH抗体均购于美国Santa Cruz公司,兔抗小鼠IgG购自于武汉博士德公司。NF-κB-luc报告质粒为美国奥克拉荷马大学Ding Weiqun教授惠赠,荧光报告基因检测试剂盒Dual-Luciferase Reporter Assay System购于Promeaga公司(普洛麦格北京生物技术有限公司)。荧光检测仪Turner BioSystems ModulusTM ⅡMultimode Microplate Reader购于美国Turner BioSystems公司,现存于武汉大学肿瘤研究所实验室。
1.2 方法 1.2.1 细胞培养A2780和耐药株A2780/DDP细胞培养于含10%胎牛血清的RPMI培养液中,置于37 ℃、5%CO2培养箱内培养,待对数生长期备用。
1.2.2 MTS法检测ZPT对A2780和耐药株A2780/DDP细胞增殖影响接种约3 000-5 000个/孔A2780和耐药株A2780/DDP细胞于96孔板中,待细胞生长至70%汇合度且处对数生长期时,按照实验分组给予相应浓度药物处理细胞。检测ZPT对卵巢癌细胞增殖抑制效应时浓度分组分别为(0,0.1,0.2,0.4,0.8,1.0,2.0,4.0,8.0 μmol/L)。测定ZPT对A2780/DDP细胞顺铂逆转效应时分组如下:DMSO对照组,5 μmol/L DDP组,0.5 mol/L ZPT组,0.5 μmol/L ZPT+5 μmol/L DDP组。分别测定药物处理后48 h时各孔的吸光度(A 值)。具体操作和计算参照MTS试剂盒说明书(http://www.promega.com/tbs/tb169/tb169.pdf)。实验每次设3个平行样本,实验重复3次。
1.2.3 荧光素酶法检测A2780和耐药株A2780/DDP细胞NF-κB转录活性质粒NF-κB-Luc转染处于对数生长期的A2780和耐药株A2780/DDP细胞,将成功转染后的细胞转移至12孔板。检测两株细胞自身NF-κB转录活性时分组为对照组(A2780组)和观察组(A2780/DDP细胞)。检测ZPT对耐药株A2780/DDP细胞NF-κB转录活性时分组为分对照组(DMSO组)和实验组(0.5 μmol/L ZPT组)。6 h后收集各组细胞细胞,裂解细胞,收集细胞裂解液,12 000 g室温下离心30 s后收集上清,根据Dual-Luciferase Reporter Assay System试剂盒说明,采用荧光强度检测仪(Turner BioSystems ModulusTM ⅡMultimode Microplate Reader,武汉大学肿瘤研究所)检测各组各样本的荧光强度。此实验每次设3个平行样本,实验重复3次。
1.2.4 WesternBlot法检测ZPT对A2780/DDP细胞p65和Bcl-2蛋白表达水平的影响实验分对照组(DMSO组)和实验组(0.5 μmol/L ZPT组),处理A2780/DDP细胞48 h后收集细胞,Western细胞裂解液裂解细胞,提取总蛋白,Bradford蛋白浓度测定试剂盒检测各组蛋白总浓度,常规电泳、转印、封闭、一抗孵育、洗脱、二抗孵育和洗脱,DAB辣根过氧化物酶显色试剂盒显色,X线片曝光压片。目的蛋白相对表达量=目的蛋白灰度值/GAPDH灰度值。
1.2.5 统计学方法各组间的细胞增殖抑制率、p65和Bcl-2蛋白表达差异和荧光素酶活性差异均采用单因素方差分析,以P<0.05为差异有统计学意义。
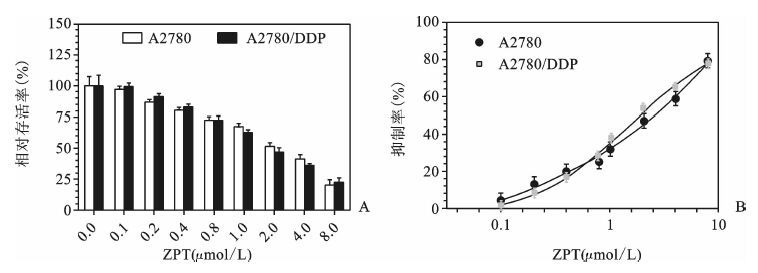
2 结果 2.1 ZPT对人卵巢癌细胞株A2780和A2780/DDP增殖抑制效应不同剂量的ZPT处理A2780和A2780/DDP 48 h,MTS法检测ZPT对两株细胞的增殖抑制效应。结果见图 1A和B,ZPT对A2780和A2780/DDP的增殖抑制效应呈剂量依赖性,且ZPT对两株细胞的抑制效应无明显差异。模拟增殖抑制曲线结果见图 1B,计算出A2780和A2780/DDP的半数抑制浓度(IC50)值分别为1.498 μmol/L和1.516 μmol/L。
|
图 1 ZPT对人卵巢癌细胞株A2780和A2780/DDP增殖抑制效应 |
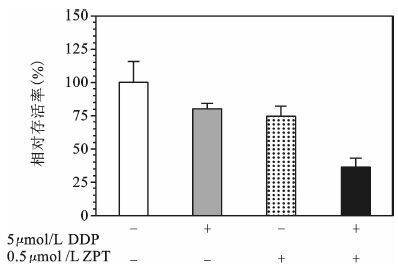
0.5 μmol/L ZPT预处理A2780/DDP细胞12 h,再联合5 μmol/L顺铂处理24 h,MTS法检测细胞增殖抑制率。结果如图 2,空白对照组、5 μmol/L顺铂组、0.5 μmol/L ZPT组和DDP+ZPT组的细胞增殖指数分别100%、80.80%、74.38%和35.63%,联合组相对于DDP组和ZPT组差别均有统计学意义。
|
图 2 ZPT联合顺铂对A2780/DDP增殖抑制效应 |
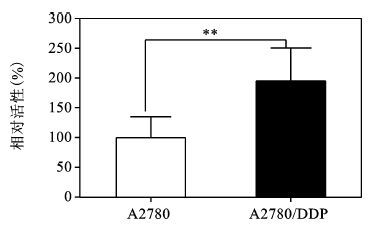
转染p-NF-κB-Luc入A2780、A2780/DDP,24 h后接种细胞接种至24孔板,12 h后收集细胞裂解液,荧光素酶法检测NF-κB活性。结果(如图 3) 提示:A2780/DDP组NF-κB活性是A2780组的1.92倍;两组差别均有统计学意义(P<0.01) 。
|
图 3 顺铂敏感和耐药卵巢癌细胞株NF-κB活性 |
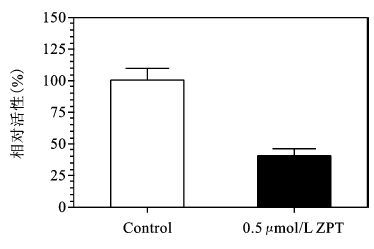
转染p-NF-κB-Luc入A2780/DDP,24 h后接种细胞接种至24孔板,12 h后采用0.5 μmol/L ZPT处理细胞6 h,收集细胞裂解液,荧光素酶法检测NF-κB活性。结果如图 4,0.5 μmol/L ZPT处理A2780/DDP细胞6 h后,A2780/DDP的NF-κB活性从100%降低至39.69%,两者差异有统计学意义。
|
图 4 ZPT对A2780/DDP细胞NF-κB活性的影响 |
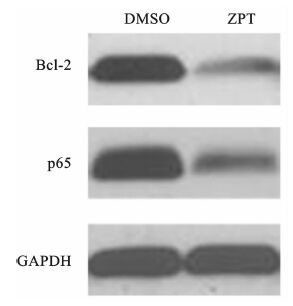
0.5 μmol/L ZPT处理细胞A2780/DDP细胞48 h,Western Blot法检测蛋白表达水平。结果如图 5所示,相对于对照组,0.5 μmol/L ZPT处理组的p65和Bcl-2蛋白表达水平显著下降。表明ZPT可下调A2780/DDP细胞的p65和Bcl-2蛋白表达。
|
图 5 ZPT对A2780/DDP细胞p65和Bcl-2蛋白表达的影响 |
以顺铂为基础的化疗是卵巢癌治疗的重要手段,顺铂化疗耐药严重影响其预后,目前临床还缺乏有效逆转方法。本研究发现中药陵水暗罗提取物ZPT可以显著增加顺铂对卵巢癌耐药细胞株A2780/DDP的增殖抑制效应,进一步的研究发现A2780/DDP耐药株的NF-κB转录活性显著增高,ZPT可以抑制A2780/DDP耐药株的NF-κB的活性,抑制p65蛋白的表达,下调抗凋亡蛋白Bcl-2的表达。我们的研究提示,ZPT下调NF-κB/Bcl-2途径活性可能是其逆转卵巢癌顺铂耐药的机制。
ZPT中含有锌离子,锌离子是一种与肿瘤关系非常密切的金属离子。报道[9-11]显示,锌离子与前列腺癌、肝癌、乳腺癌、膀胱癌等多种肿瘤的关系密切。血清锌离子浓度与前列腺癌发病呈负相关,前列腺癌患者的血清锌离子浓度和肿瘤细胞内锌离子浓度均低于正常人和组织[12]。荟萃分析[13]提示含锌饮食与结直肠癌发率呈负相关; 含锌饮食可以阻止食管炎症向食道肿瘤的转化[14]。锌离子载体转运锌离子进入肿瘤细胞可抑制肿瘤细胞的NF-κB活性,上调肿瘤细胞凋亡蛋白的表达,下调凋亡抑制蛋白的表达,抑制肿瘤细胞的增殖[15-17]。锌离子化合物Zinc protoporphyrin可以抑制卵巢癌细胞A2780的增殖[16]。本研究也证实ZPT可以抑制A2780和耐药株A2780/DDP的增殖活性,同时可以增加顺铂对A2780/DDP的细胞增殖抑制效应。
最近的研究显示NF-κB信号激活在卵巢癌细胞顺铂耐药机制中发挥重要作用。研究[1-3]已经证实NF-κB与卵巢癌的发生、发展及治疗耐药关系密切,NF-κB抑制剂是理想的抗癌药物增敏剂[4]。NF-κB可以增加多西他赛耐药卵巢癌细胞株SKOV3高表达凋亡抑制蛋白(CFLAR、XIAP、BCL2和BCL2L1),促使细胞逃避凋亡[5]。Mabuchi报道[6]:相对于顺铂敏感细胞株A2780,顺铂耐药株Caov-3的磷酸化IκBα和NF-κB活性均显著增高; 且顺铂处理后,两株细胞的磷酸化IκBα和NF-κB活性都降低,但是A2780组降低更显著; IκBα磷酸化抑制剂BAY 11-7085可以增强顺铂对Caov-3毒性。研究还显示,红桔素[18]、沙利霉素[19]和岩藻黄素[20]可抑制顺铂耐药卵巢癌细胞NF-κB活性,提高顺铂耐药卵巢癌细胞株对顺铂的敏感性,增加肿瘤细胞的凋亡,逆转顺铂耐药细胞株的耐药性。本研究也发现卵巢癌顺铂耐药株NF-κB活性均显著增高,ZPT可以抑制其增高的NF-κB活性,增加其对顺铂的敏感性。
总之,本研究初步发现中药陵水暗罗提取物ZPT可以增加人卵巢癌耐药细胞株A2780/DDP对顺铂的敏感性,其可能机制是抑制耐药株增高的NF-κB转录活性,抑制p65蛋白的表达,下调凋亡抑制蛋白Bcl-2的表达。未来我们将开展进一步的研究来验证其在体内的对人卵巢癌顺铂耐药株的逆转效应。
| [1] | Drummond AE, Fuller PJ. Activin and inhibin, estrogens and NFkappaB, play roles in ovarian tumourigenesis is there crosstalk[J]. Molecular and Cellular Endocrinology, 2012, 359(1-2): 85-91. DOI: 10.1016/j.mce.2011.07.033. |
| [2] | Gaikwad SM, Thakur B, Sakpal A, et al. Differential activation of NF-kappaB signaling is associated with platinum and taxane resistance in MyD88 deficient epithelial ovarian cancer cells[J]. Int J Biochem Cell Biol, 2015, 61: 90-102. DOI: 10.1016/j.biocel.2015.02.001. |
| [3] | Zou W, Ma X, Hua W, et al. Caveolin-1 mediates chemoresistance in cisplatin-resistant ovarian cancer cells by targeting apoptosis through the Notch-1/Akt/NF-kappaB pathway[J]. Oncology Reports, 2015, 34(6): 3256-3263. |
| [4] | Nakanishi C, Toi M. Nuclear factor-kappaB inhibitors as sensitizers to anticancer drugs[J]. Nature Reviews Cancer, 2005, 5(4): 297-309. DOI: 10.1038/nrc1588. |
| [5] | Yang YI, Ahn JH, Lee KT, et al. RSF1 is a positive regulator of NF-kappaB-induced gene expression required for ovarian cancer chemoresistance[J]. Cancer Research, 2014, 74(8): 2258-2269. DOI: 10.1158/0008-5472.CAN-13-2459. |
| [6] | Mabuchi S, Ohmichi M, Nishio Y, et al. Inhibition of NFkappaB increases the efficacy of cisplatin in in vitro and in vivo ovarian cancer models[J]. J Biol Chem, 2004, 279(22): 23477-23485. DOI: 10.1074/jbc.M313709200. |
| [7] |
姚建忠, 梁华清, 廖时萱. 陵水暗罗活性成分研究[J].
药学学报, 1994, 29(11): 845-850.
Yao JZ, Liang HQ, Liao SX. The study of active components of Polyalthia nemoralis[J]. Acta Pharmaceutica Sinica, 1994, 29(11): 845-850. |
| [8] |
韩公羽, 徐炳祥, 王肖鹏, 等. 陵水暗罗有效成分的研究——天然金属化合物暗罗素的分离及结构[J].
科学通报, 1980, 25(6): 285-286.
Han GY, XU BX, Wang XB, et al. The study of active ingredients of Polyalthia nemoralis- isolation and structure of natural zinc compound of Zincpolyanemine[J]. Chinese Science Bulletin, 1980, 25(6): 285-286. |
| [9] | Costello LC, Franklin RB. The status of zinc in the development of hepatocellular cancer: an important, but neglected, clinically established relationship[J]. Cancer Biology & Therapy, 2014, 15(4): 353-360. |
| [10] | Hoang BX, Han B, Shaw DG, et al. Zinc as a possible preventive and therapeutic agent in pancreatic, prostate, and breast cancer[J]. Eur J Cancer Prev, 2016, 25(5): 457-461. DOI: 10.1097/CEJ.0000000000000194. |
| [11] | Singh BP, Dwivedi S, Dhakad U, et al. Status and Interrelationship of Zinc, Copper, Iron, Calcium and Selenium in Prostate Cancer[J]. Indian J Clin Biochem, 2016, 31(1): 50-56. DOI: 10.1007/s12291-015-0497-x. |
| [12] | Park SY, Wilkens LR, Morris JS, et al. Serum zinc and prostate cancer risk in a nested case-control study: The multiethnic cohort[J]. The Prostate, 2013, 73(3): 261-266. DOI: 10.1002/pros.v73.3. |
| [13] | Qiao L, Feng Y. Intakes of heme iron and zinc and colorectal cancer incidence: a meta-analysis of prospective studies[J]. Cancer Causes & Control, 2013, 24(6): 1175-1183. |
| [14] | Taccioli C, Chen H, Jiang Y, et al. Dietary zinc deficiency fuels esophageal cancer development by inducing a distinct inflammatory signature[J]. Oncogene, 2012, 31(42): 4550-4558. DOI: 10.1038/onc.2011.592. |
| [15] | Yu H, Zhou Y, Lind SE, et al. Clioquinol targets zinc to lysosomes in human cancer cells[J]. The Biochemical Journal, 2009, 417(1): 133-139. DOI: 10.1042/BJ20081421. |
| [16] | Wang S, Avery JE, Hannafon BN, et al. Zinc protoporphyrin suppresses cancer cell viability through a heme oxygenase-1-independent mechanism: the involvement of the Wnt/beta-catenin signaling pathway[J]. Biochemical pharmacology, 2013, 85(11): 1611-1618. DOI: 10.1016/j.bcp.2013.03.011. |
| [17] | Ku JH, Seo SY, Kwak C, et al. The role of survivin and Bcl-2 in zinc-induced apoptosis in prostate cancer cells[J]. Urologic Oncology, 2012, 30(5): 562-568. DOI: 10.1016/j.urolonc.2010.06.001. |
| [18] | Arafa el-SA, Zhu Q, Barakat BM, et al. Tangeretin sensitizes cisplatin-resistant human ovarian cancer cells through downregulation of phosphoinositide 3-kinase/Akt signaling pathway[J]. Cancer Res, 2009, 69(23): 8910-8917. DOI: 10.1158/0008-5472.CAN-09-1543. |
| [19] | Parajuli B, Lee HG, Kwon SH, et al. Salinomycin inhibits Akt/NF-kappaB and induces apoptosis in cisplatin resistant ovarian cancer cells[J]. Cancer Epidemiology, 2013, 37(4): 512-517. DOI: 10.1016/j.canep.2013.02.008. |
| [20] | Liu CL, Lim YP, Hu ML. Fucoxanthin enhances cisplatin-induced cytotoxicity via NFkappaB-mediated pathway and downregulates DNA repair gene expression in human hepatoma HepG2 cells[J]. Marine Drugs, 2013, 11(1): 50-66. DOI: 10.3390/md11010050. |
 2017, Vol. 38
2017, Vol. 38

