2. 中南大学湘雅三医院/卫生部移植医学工程技术研究中心 湖南 长沙 410013
2. The 3rd Xiangya Hospital of Central South University & Research Center of National Health Ministry on Transplantation Medicine Engineering and Technology, Changsha 410013, China
肝移植是治疗终末期肝病的最佳选择[1],而供肝短缺是肝移植事业发展面临的主要矛盾,目前脑死亡供体(donor after brain death, DBD)已成为供肝来源的有效途径,然而,与亲属活体移植相比,脑死亡供肝肝移植疗效尚需进一步研究[2]。有研究证实脑死亡后供肝组织出现缺血缺氧而导致肝细胞凋亡[3],是肝移植效果急需探讨的重要原因。实验室前期研究通过建立家兔脑死亡模型[4],利用蛋白质组学方法筛选出肝脏存在的差异蛋白质线粒体乙醛脱氢酶2(aldehyde dehydrogenase 2, ALDH2),并证明其在脑死亡组表达明显降低[5]。本实验通过免疫组织化学法检测显示ALDH2主要表达于内皮细胞和肝细胞,进一步在细胞水平上建立缺氧模型并干扰ALDH2的表达来探究脑死亡供肝中ALDH2表达与细胞凋亡的关系,为临床脑死亡供肝质量评估提供新指标。
1 材料与方法 1.1 实验材料紫外分光光度计(上海现科仪器有限公司),电泳仪(北京六一仪器厂),高速离心机(英格兰JENWAY公司),低速离心机(德国Eppendorf公司),超低温冰箱ELT-13V-85V29(美国Thermo公司),丙烯酰胺(瑞典Amersham Biosciences公司),BCA蛋白定量检测试剂盒等Western blot试剂(碧云天生物技术公司),HRP标记的羊抗兔二抗(武汉博士德公司),p-ALDH2抗体(英国Abcam),Caspase 3抗体(小鼠来源,碧云天进口分装)。
1.2 实验方法 1.2.1 免疫组织化学检测p-ALDH2表达取脑死亡组和假手术组肝脏组织经10%甲醛溶液固定,石蜡包埋切片后,常规脱蜡和水化。用3%的H2O2-甲醇溶液室温孵育30 min以灭活内源性过氧化物酶,分别加入ALDH2抗体4 ℃孵育过夜,PBS洗涤3次后,再加入辣根过氧化物酶(HRP)偶联的二抗,37 ℃孵育1 h,PBS缓冲液漂洗后,DAB显色,苏木精复染细胞核,梯度脱水后用二甲苯透明,中性树胶封片。以PBS代替一抗作为阴性对照。每组内每张切片于200倍视野下进行拍照。选取相同的棕黄色作为判断所有照片阳性的统一标准,对每张照片进行分析,得出每张照片阳性的累积光密度值。
1.2.2 人脐静脉内皮细胞培养及分组人脐静脉内皮细胞株(购自ATCC),用含10%胎牛血清的和DMEM高糖培养基5% CO2、37 ℃培养箱培养,待细胞传代数瓶后进行分组处理。①正常细胞组:继续5% CO2、37 ℃培养8 h;②缺氧组:细胞经8 h 95% N2+5%CO2培养8 h;③大豆苷+缺氧组:在处理前24 h加入大豆苷(60 μmol)[6],24 h后细胞经8 h 95% N2+5%CO2培养8 h;④Alda-1+缺氧组:在处理前1 h加入Alda-1(20 μmol/L)[7],24 h后细胞经8 h 95% N2+5%CO2培养8 h。
1.2.3 免疫印迹法(Western blot)检测p-ALDH2, Cleaved-caspase 3表达细胞缺氧模型建立结束后提取各组细胞总蛋白,按BCA试剂盒测定蛋白浓度,取等量蛋白样品用15%SDS-PAGE凝胶进行电泳,电泳完毕后转至PVDF膜上,300 mA,3 h。含5%脱脂牛奶的TBST溶液中37 ℃封闭2 h;分别加入p-ALDH2抗体(1:2 000稀释)、caspase-3抗体(1:500稀释),4 ℃过夜;TBST充分洗涤后分别加入对应山羊抗鼠二抗(1:2 000稀释)或山羊抗兔二抗(1:3 000稀释)室温作用2 h,TBST再次充分洗涤;用ECL液与膜反应后,X线片压片曝光。电脑扫描记录结果的X线片,Image J图像分析软件读取胶片上蛋白条带的灰度值。
1.2.4 统计学处理利用SPSS 21.0统计软件进行数据统计分析。以上数据均利用SPSS 21.0统计软件进行ANOVA统计分析。检验水准α=0.05。
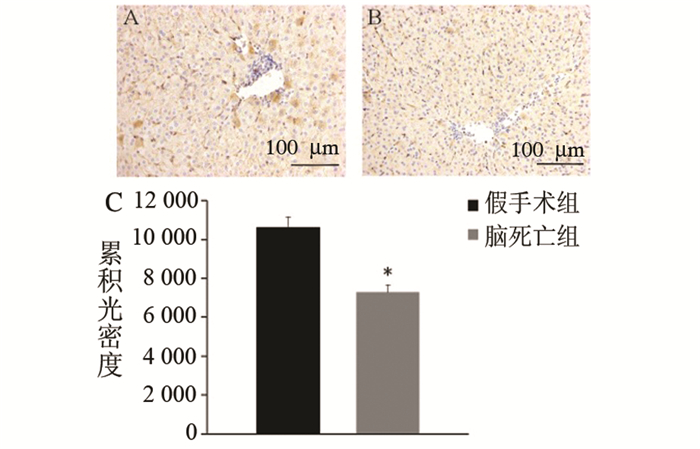
2 结果 2.1 ALDH2在家兔脑死亡模型肝脏组织中的表达情况免疫组织化学实验显示,p-ALDH2表达部位主要在血管内皮细胞和肝细胞。与假手术组相比,p-ALDH2的表达在脑死亡组较低,差异有统计学意义(P < 0.05)(图 1)。
|
图 1 ALDH2在肝脏中表达情况 A.假手术组,B.脑死亡组×200;C.累积光密度值对比,与假手术组相比,*P<0.05(n=5) |
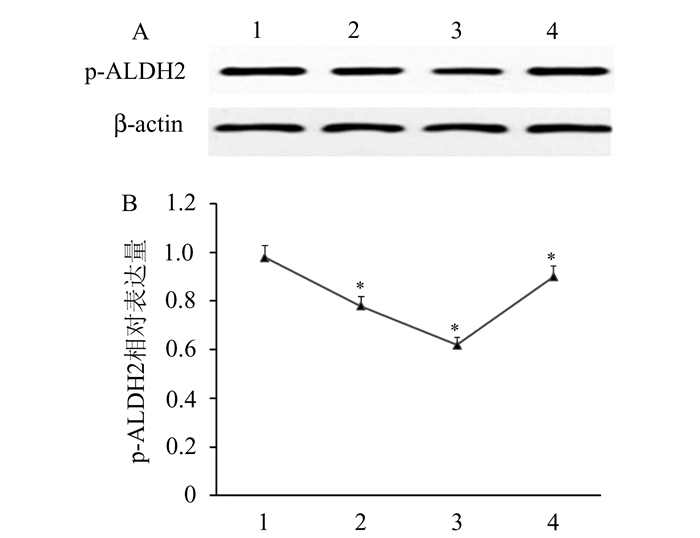
通过加入ALDH2特异性激动剂Alda-1或特异性抑制剂大豆苷后培养于不同实验条件下并收集标本。Western blot结果显示,缺氧组p-ALDH2表达水平较正常组低;在大豆苷+缺氧组中p-ALDH2表达水平进一步降低;在Alda-1+缺氧组中,与正常组相比,p-ALDH2的表达水平较低,而与缺氧组相比,p-ALDH2的表达水平较高,差异均具有统计学意义(P < 0.05)(图 2)。
|
图 2 p-ALDH2在人脐静内皮细胞中表达情况 A和B中1为正常组,2为缺氧组,3为大豆苷+缺氧组, 4为Alda-1+缺氧组;*其它3组相比,P<0.05 (n=3) |
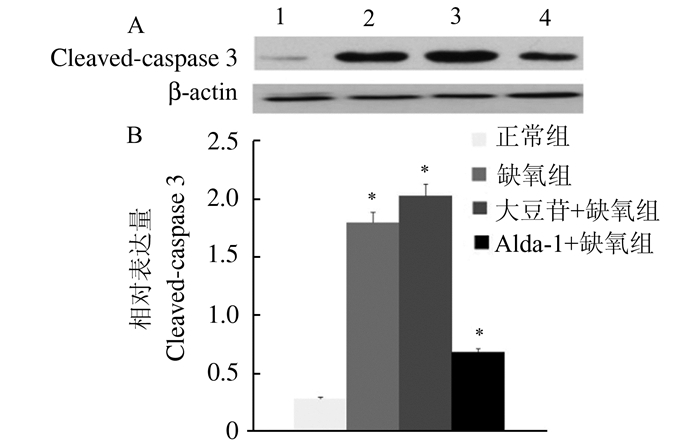
Western blot结果显示,缺氧组Cleaved-caspase 3表达水平较正常组高;在大豆苷+缺氧组中Cleaved-caspase 3表达水平进一步升高;在Alda-1+缺氧组中,与正常组相比,Cleaved-caspase 3的表达水平较高,而与缺氧组相比,p-ALDH2的表达水平明显降低,差异均具有统计学意义(P < 0.05)(图 3)。
|
图 3 Cleaved-caspase 3在人脐静脉内皮细胞中表达情况 1为正常组,2为缺氧组,3为大豆苷+缺氧组,4为Alda-1+缺氧组;其它3组相比,*P<0.05 (n=3) |
脑死亡供体(donor after brain death, DBD)已成为缓解移植器官来源短缺的有效途径,且脑死亡器官捐献肝移植手术不断增多,为提高移植疗效,如何评估供肝的质量是当今的研究热点[8]。实验室前期研究通过缓慢颅内加压建立稳定的家兔脑死亡模型,并采用蛋白组学方法筛选脑死亡组和假手术组中存在的差异蛋白质。结果发现,脑死亡组与假手术组共存在10种差异蛋白,进一步分析发现,其中一种差异蛋白线粒体乙醛脱氢酶2(ALDH2)与机体物质代谢密切相关,其在脑死亡组中表达明显降低。ALDH2是体内重要的抗氧化应激的保护因子之一,它参与各种内、外源性脂肪族及芳香族醛类物质代谢或解毒过程,对氧化应激起到防护作用,其活性形式主要是磷酸化ALDH2(p-ALDH2)[5]。文献报道,过表达ALDH2可以保护细胞对抗体外化学毒性物质,还能通过抗氧化应激作用对抗细胞凋亡[9]。细胞凋亡是细胞在一定生理或病理条件下,程序性主动死亡的过程。凋亡受多种基因严格控制,如Bcl-2家族、caspase家族等,凋亡过程的紊乱可能与许多疾病的发生有直接或间接的关系[10]。由此,我们推测,ALDH2表达降低可使肝细胞凋亡增加而致脑死亡供肝损伤。
本研究通过免疫组织化学法检测脑死亡组与假手术组家兔肝脏中p-ALDH2的表达,结果显示p-ALDH2在血管内皮细胞和肝细胞表达最多,且脑死亡组中p-ALDH2的表达降低。为进一步研究ALDH2与细胞凋亡的关系,我们建立人脐静脉内皮细胞缺氧模型模拟脑死亡状态,并通过加入ALDH2特异性抑制剂大豆苷或特异性激动剂Alda-1使ALDH2表达降低或升高。Western blot结果显示,缺氧组p-ALDH2表达水平较正常组低而Cleaved-caspase 3表达水平较正常组高;在大豆苷+缺氧组中p-ALDH2表达水平进一步降低,Cleaved-caspase3表达水平升高;同时,在Alda-1+缺氧组中,与正常组相比,p-ALDH2的表达水平较低,Cleaved-caspase3表达水平较高,而与缺氧组相比,p-AL-DH2的表达水平较高,Cleaved-caspase3表达水平较低,差异均具有统计学意义(P<0.05)。细胞凋亡水平随着Cleaved-caspase3的表达升高而升高。
综合以上实验结果提示脑死亡供肝ALDH2表达降低可增加细胞凋亡,引起肝脏损伤,但ALDH2和细胞凋亡之间的具体机制仍需进一步研究,若能证实ALDH2和脑死亡供肝细胞凋亡的具体机制,则ALDH2可成为评估脑死亡供肝质量的新指标。
| [1] | Olson JC, Wendon JA, Kramer DJ, et al. Intensive care of the patient with cirrhosis[J]. Hepatology, 2011, 54: 1864-1872. DOI: 10.1002/hep.24622. |
| [2] | Monbaliu D, Pirenne J, Talbot D. Liver transplanta-tion using Donation after Cardiac Death donors[J]. J Hepatol, 2012, 56(2): 474-485. DOI: 10.1016/j.jhep.2011.07.004. |
| [3] | 钟自彪, 张萌, 熊艳, 等. 家兔脑死亡供肝细胞凋亡水平的定量研究[J]. 中国普外基础与临床杂志, 2016, 23(1): 22-27. |
| [4] | 钟自彪, 王彦峰, 李玲, 等. 缓慢间断颅内加压法家兔脑死亡模型的建立及病理生理变化[J]. 中华肝胆外科杂志, 2013, 19(8): 622-624. |
| [5] | 钟自彪, 叶啟发, 王彦峰, 等. 脑死亡状态下家兔肝脏质量评估新指标---线粒体醛脱氢酶[J]. 中华肝胆外科杂志, 2013, 19(7): 534-538. |
| [6] | Zhang P, Xu D, Wang S, et al. Inhibition of aldehyde dehydrogenase 2 activity enhances antimycin-induced rat cardiomyocytes apoptosis through activation of MAPK signaling pathway[J]. Biomed Pharmacother, 2011, 65: 590-593. DOI: 10.1016/j.biopha.2009.12.001. |
| [7] | Chen CH, Budas GR, Churchill EN, et al. Activation of aldehyde dehydrogenase-2 reduces ischemic damage to the heartv[J]. Science, 2008, 321: 1493-1495. DOI: 10.1126/science.1158554. |
| [8] | Klein AS, Messersmith EE, Ratner LE, et al. Organ donation and utilization in the United States, 1999-2008[J]. Am J Transplant, 2010, 10: 973-986. DOI: 10.1111/ajt.2010.10.issue-4p2. |
| [9] | Rui G, Li Z, Jun R, et al. Overexpression of ALDH2 attenuates chronic alcohol exposure-induced apoptosis, change in Akt and Pim signaling in liver[J]. Clinical and Experimental Pharmacology and Physiology, 2009, 36: 463-468. DOI: 10.1111/cep.2009.36.issue-5-6. |
| [10] | Kam PC, Ferch NI. Apoptosis: mechanisms and clini-cal implications[J]. Anaesthesia, 2000, 55(11): 1081-1093. DOI: 10.1046/j.1365-2044.2000.01554.x. |
 2016, Vol. 37
2016, Vol. 37

