2. 口腔基础医学省部共建国家重点实验室培育基地和口腔生物医学教育部重点实验室 武汉大学口腔医学院 湖北 武汉 430079
2. The State Key Laboratory Breeding Base of Basic Science of Stomatology (Hubei_MOST) & Key Laboratory of Oral Biomedicine Ministry of Education, School of Stomatology, Wuhan University, Wuhan 430079, China
同源结构域相互作用蛋白激酶2(homeodomain-interacting protein kinase 2,HIPK2)属于丝/苏氨酸蛋白激酶家族(HIPKs),是一种参与调节细胞周期、衰老及凋亡的转录因子[1],主要表达于细胞核中。研究发现,HIPK2在甲状腺癌[2]、膀胱癌[3]及结直肠癌[4]中表达下调,且与肿瘤转移及侵袭呈负相关,说明HIPK2可能具有抑癌作用。然而,Cheng等发现HIPK2在宫颈癌中表达增多[5],其表达量与宫颈癌的发展呈正相关;抑制HIPK2的表达可引起细胞凋亡增加,增殖减少,证明HIPK2在宫颈癌中可能发挥了癌基因的功能。以上研究提示HIPK2在肿瘤中的作用尚无定论,它在口腔鳞状细胞癌(oral squamous cell carcinoma,OSCC)中的表达情况及其对预后的影响尚不清楚。本文通过研究HIPK2在OSCC组织及细胞中的表达,探讨其在OSCC中的作用,为OSCC的预后评估提供参考。
1 材料与方法 1.1 样本及临床资料收集组织芯片样本来源于武汉大学口腔医院2002年1月至2009年2月经手术切除并确诊的OSCC石蜡标本99例(其中20例伴颈淋巴结转移)。
1.2 组织芯片的制作在每例标本HE切片上标记癌旁正常上皮、肿瘤中心和肿瘤前沿三个部位(伴淋巴结转移者还包括淋巴结转移灶)并在供体蜡块的对应部位作标记,设计好阵列图,送往上海芯超生物有限公司制成组织芯片。
1.3 免疫组化染色组织切片60 ℃烘烤1 h,使用AutostainerLink 48(Dako)进行脱蜡、梯度乙醇溶液水化及抗原修复,HIPK2抗体(兔抗,Sigma)室温孵育1 h,再使用AutostainerLink进行过氧化物阻断、二抗孵育及DAB染色。
1.4 细胞培养OSCC细胞系(包括Cal27、SCC9及SCC25)常规培养于含10%FBS(Hyclone)的DMEM或DME/F12培养基中,正常上皮细胞系(HIOEC)常规培养于KBM(Lonza)培养基中,37 ℃、5%CO2恒温培养。
1.5 Real-time PCR提取细胞总RNA(Omega总RNA提取试剂盒),以总RNA为模板进行逆转录合成cDNA(Takara逆转录试剂盒),再进行real-time PCR反应(Roche,FastStart Essential DNA Green Master)。以β-actin为内参,使用2-ΔΔCt法对目的基因进行分析。引物序列如下:
β-actin Forward 5′-ACCAACTGGGACGACATGGAGAAA-3′;
Reverse 5′-TAGCACAGCCTGGATAGCAA CGTA-3′;
HIPK2 Forward 5′-CCCCGTGTACGAAGGTATGG-3′;
Reverse 5′-GGGATGTTCTTGCTCTGGCT-3′。
1.6 细胞免疫荧光贴壁培养的细胞用4%多聚甲醛固定15 min,1%Triton破膜15 min,4%BSA室温封闭30 min,滴加HIPK2抗体(兔抗,Abcam)4 ℃孵育过夜;用PBS浸洗3次,5 min/次,用标记有Cy3的二抗37 ℃避光孵育1 h,PBS浸洗3次,5 min/次。滴加DAPI复染核5 min,蒸馏水浸洗3次,5 min/次,共聚焦显微镜下观察。使用Image-Pro Plus软件分析细胞免疫荧光结果,以细胞的平均荧光强度(IOD)代表蛋白表达密度。
1.7 统计学分析免疫组化染色结果使用Aperio ImageScope v11.2.0进行分析。染色阳性结果计算公式:(强阳性细胞数×3+阳性细胞数×2+弱阳性细胞数×1)/染色面积。每一个阵点随机选取4个视野,取平均值。数据以均数±标准差表示,使用GraphPad Prism 5进行统计分析。计数资料采用Fisher检验,组间的两两比较采用t检验,多组间的比较采用ANOVA检验,并使用log-rank检验进行生存分析。P<0.05为差异具有统计学意义。
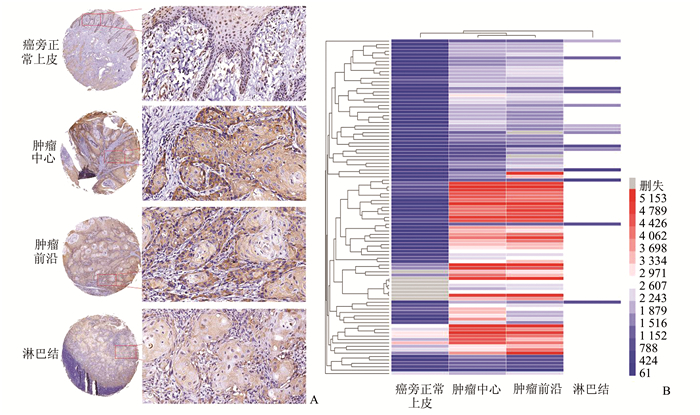
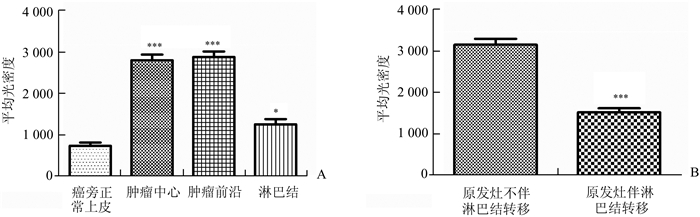
2 结果 2.1 HIPK2在OSCC组织中表达升高免疫组化染色结果显示,99例OSCC组织的癌旁正常上皮、肿瘤中心、肿瘤前沿及转移淋巴结均表现为HIPK2染色阳性(图 1)。ImageScope软件分析显示,癌旁正常上皮的平均光密度为748.75±755.90,肿瘤中心、肿瘤前沿及转移淋巴结的平均光密度分别为2 843.32±1 328.16、2 920.28±1 318.18及1 274.15±454.87,分别是癌旁正常上皮的3.80倍、3.90倍及1.70倍,差异具有统计学意义(P<0.05)(图 2A)。其中,肿瘤原发灶不伴淋巴结转移的平均光密度(3 174.96±1 305.54)是伴淋巴结转移(1 533.35±1 446.63)的2.07倍,差异具有统计学意义(P=0.000 6)(图 2B)。
|
图 1 HIPK2在OSCC组织芯片中的代表性病例(×500) A:免疫组化结果显示HIPK2在癌旁正常上皮中的阳性染色比肿瘤中心、肿瘤前沿及淋巴结转移灶浅;B:99例OSCC组织芯片免疫组化染色结果的聚类关系 |
|
图 2 HIPK2在肿瘤不同部位及是否伴淋巴结转移表达的差异 A:癌旁正常上皮、肿瘤中心、肿瘤前沿及淋巴结的平均光密度值比较,肿瘤中心、肿瘤前沿及淋巴结的平均光密度比癌旁正常上皮显著升高(P<0.05);B:肿瘤中心伴淋巴结转移及不伴淋巴结转移的平均光密度值比较,有转移比无转移低(P<0.000 1) |
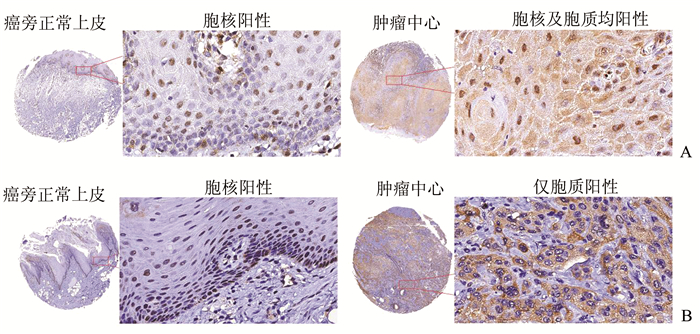
免疫组化染色结果显示,HIPK2在OSCC组织中表现出胞核阳性、胞核及胞质均阳性及仅胞质阳性3种表达模式。癌旁正常上皮主要表现为胞核阳性,肿瘤中心主要表现为胞核及胞质均阳性或仅胞质阳性(图 3)。HIPK2在OSCC肿瘤中心以仅胞质阳性表达模式为主(61/99),占61.62%。
|
图 3 HIPK2在OSCC组织中的不同表达模式 A:病例1中癌旁正常上皮为胞核阳性,肿瘤中心为胞核及胞质均阳性;B:病例2中癌旁正常上皮为胞核阳性,肿瘤中心为仅胞质阳性 |
通过分析99位OSCC患者的临床病理资料与HIPK2表达的关系,我们发现HIPK2的表达模式与患者临床分期及病理分级显著相关(P<0.01),而与性别及年龄无显著相关性(P>0.05)(表 1)。其中,临床分期Ⅰ+Ⅱ期病例中仅胞质阳性的例数显著少于Ⅲ+Ⅳ期病例(P=0.004 1);病理分级Ⅰ+Ⅱ级病例中仅胞质阳性的例数显著少于Ⅲ级病例(P=0.000 7)。
| 表 1 HIPK2的表达与临床病理因素间的关系[Fisher精确检验, n(%)] |
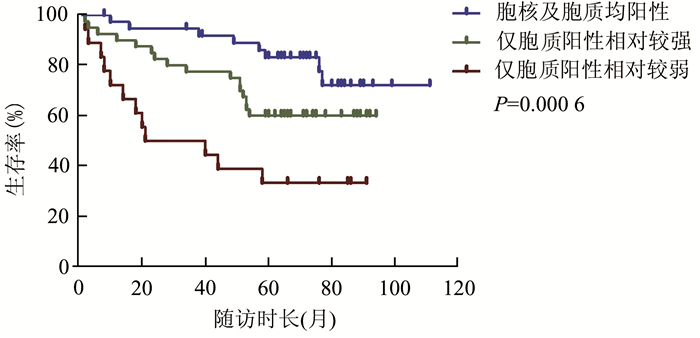
99位OSCC患者死亡36例,生存60例,失访3例,总体生存率为60.61%,随访时间为60-111个月。通过log-rank检验对肿瘤中心不同表达模式的患者进行生存分析,结果显示胞核及胞质均阳性、仅胞质阳性相对较强、仅胞质阳性相对较弱者的总体生存率依次降低(P=0.000 6),仅胞质阳性相对较弱者的总体生存率最低(图 4)。
|
图 4 肿瘤中HIPK2的表达模式与预后的关系 胞核及胞质均阳性、仅胞质阳性相对较强、仅胞质阳性相对较弱者的总体生存率依次降低(P=0.000 6),仅胞质阳性相对较弱者的总体生存率最低 |
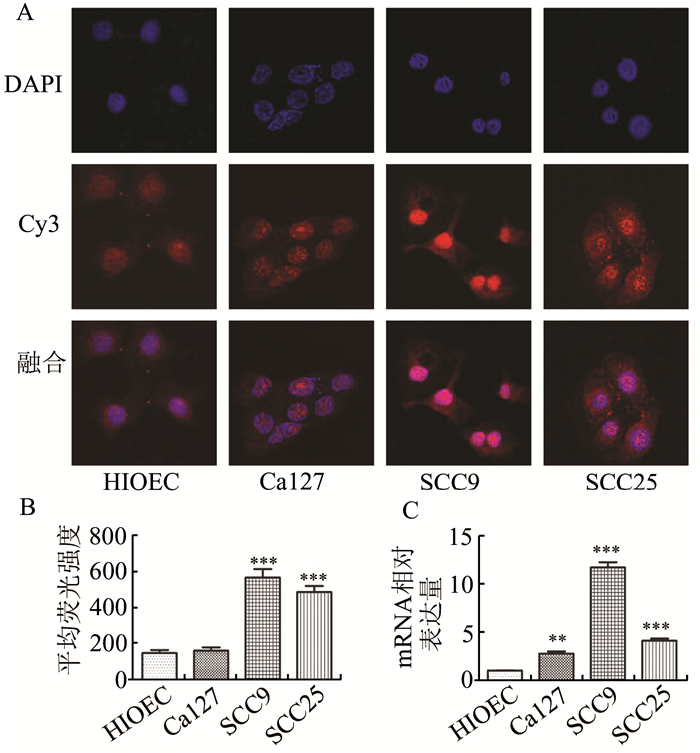
Real-time PCR结果显示,与HIOEC相比,HIPK2在Cal27、SCC9及SCC25细胞中mRNA的表达分别升高了1.71倍、10.40倍及3.00倍,差异具有统计学意义(P<0.01)(图 5C)。细胞免疫荧光结果显示,HIPK2在HIOEC、Cal27、SCC9及SCC25细胞中的IOD分别为151.03±39.12、165.31±37.69、571.17±105.08及490.02±76.24,HIPK2在SCC9及SCC25细胞中蛋白的表达显著升高(P<0.001)(图 5A,图 5B)。其中,HIPK2在HIOEC及Cal27细胞中主要表达于胞核,仅少量表达于胞质中;在SCC9及SCC25细胞中胞核及胞质均有表达。
|
图 5 HIPK2在OSCC细胞系中的表达 A:细胞免疫荧光实验显示HIPK2在4种细胞系(HIOEC、Cal27、SCC9及SCC25)中蛋白的表达(×1 000);B:HIPK2在SCC9及SCC25细胞中蛋白的表达显著高于HIOEC(P<0.001);C:Real-time PCR检测HIPK2在4种细胞系中mRNA的表达,在Cal27、SCC9及SCC25细胞中mRNA的表达显著高于HIOEC(P<0.01) |
HIPK2是HIPKs家族的主要成员,可被紫外线、电离辐射及化疗药物等DNA损伤刺激激活[1]。研究显示,激活的HIPK2可以通过p53依赖或非p53依赖的方式激活细胞凋亡[1],还可以参与p53[6]及Wnt信号通路[7]影响细胞增殖,发挥抑癌功能。研究报道HIPK2在甲状腺癌[2]、膀胱癌[3]及结直肠癌[4]中表达减少,并抑制细胞凋亡。其表达下调还与肿瘤转移及侵袭呈负相关,说明HIPK2可能抑制了肿瘤的发展。然而,也有研究发现HIPK2在多种肿瘤中表达上调并发挥了促癌作用,提示HIPK2在肿瘤中的作用尚存争议,值得探讨。
本研究结果显示,HIPK2在OSCC肿瘤中表达显著升高,说明它在OSCC中可能起到了促癌作用。据文献报道,HIPK2在上皮鳞状细胞癌、基底细胞癌[8]及宫颈癌[5]中表达也明显上调,其在宫颈癌中的表达量还与宫颈癌的发展呈正相关,证明HIPK2在其他肿瘤中也可能具有癌基因的功能。研究表明,在正常状态下HIPK2主要表达于细胞核核斑内,容易被蛋白酶降解而保持较低水平。在基础活性氧水平下,HIPK2通过类泛素化修饰并结合组蛋白去乙酰化酶3(HDAC3),限制细胞的增殖及分化[9];然而,在中度水平的活性氧刺激下,HIPK2的类泛素化修饰被乙酰化代替,HIPK2从核斑转位至核浆及胞质,帮助癌细胞逃避死亡[10],促使肿瘤生存;在超过耐受阈值的活性氧刺激下,HIPK2的乙酰化被阻断,HIPK2可逃避蛋白酶降解保持较高水平,并可冲破细胞自身的保护机制[11],造成细胞凋亡[9]。以上研究说明在一定程度肿瘤环境刺激下,HIPK2具有促癌功能,其表达量及表达模式可以反映肿瘤的进展情况,可能是评估肿瘤进展的新靶点。
本研究还发现HIPK2具有胞核表达、胞核及胞质均表达及仅胞质表达3种表达模式,在OSCC肿瘤中主要表现为胞核及胞质均阳性或仅胞质阳性,并以仅胞质阳性为主。HIPK2的这种表达模式还与患者的预后相关,仅胞质阳性相对较弱者预后最差。此研究结果证实了HIPK2的胞质再定位与肿瘤预后密切相关。研究表明,影响HIPK2胞质再定位的因素主要有两个,一是基因突变,例如,Lys798突变可使HIPK2弥散表达于整个细胞质中[12];Arg826及Tyr361F突变可显著减少HIPK2在细胞核内的表达[12, 13]。二是蛋白翻译后修饰,如HIPK2乙酰化后表达于细胞核核浆及细胞质中[9, 10];HIPK2磷酸化后表达于细胞质中[14]。此外,酪氨酸自主磷酸化[15, 16]及热激[17]也可以影响HIPK2的胞质再定位。HIPK2向核浆甚至胞质中的转位相应地改变了其功能[10],不但可以引起多种氧化还原调节基因的转录抑制[9],还可以影响蛋白-蛋白间的相互作用及信号传递[12],但影响肿瘤预后的具体机制尚不明确,有待进一步深入研究。
总之,本研究发现HIPK2在OSCC中表达升高,且以仅胞质阳性表达为主。HIPK2的表达及胞质再定位与OSCC的预后密切相关,但其具体机制尚不清楚,有待进一步探索。
| [1] | D'Orazi G, Rinaldo C, Soddu S. Updates on Hipk2: A Resourceful oncosuppressor for clearing cancer[J]. J Exp Clin Cancer Res, 2012, 31: 63. DOI: 10.1186/1756-9966-31-63. |
| [2] | Lavra L, Rinaldo C, Ulivieri A, et al. The loss of the P53 activator Hipk2 is responsible for galectin-3 overexpression in well differentiated thyroid carcinomas[J]. PLoS One, 2011, 6(6): e20665. DOI: 10.1371/journal.pone.0020665. |
| [3] | Tan M, Gong H, Zeng Y, et al. Downregulation of homeodomain-interacting protein kinase-2 contributes to bladder cancer metastasis by regulating Wnt signaling[J]. J Cell Biochem, 2014, 115(10): 1 762-1 767. DOI: 10.1002/jcb.24842. |
| [4] | Zhou L, Feng Y, Jin Y, et al. Verbascoside promotes apoptosis by regulating Hipk2-P53 signaling in human colorectal cancer[J]. BMC Cancer, 2014, 14: 747. DOI: 10.1186/1471-2407-14-747. |
| [5] | Cheng Y, Al-Beiti M, Wang J, et al. Correlation between homeodomain-interacting protein kinase 2 and apoptosis in cervical cancer[J]. Mol Med Rep, 2012, 5(5): 1 251-1 255. |
| [6] | Kuwano Y, Nishida K, Akaike Y, et al. Homeodomain-interacting protein kinase-2: a critical regulator of the DNA damage response and the epigenome[J]. Int J Mol Sci, 2016, 17(10): pii: E1638. DOI: 10.3390/ijms17101638. |
| [7] | Feng Y, Zhou L, Sun X, et al. Homeodomain-interacting protein kinase 2 (Hipk2): a promising target for anti-cancer therapies[J]. Oncotarget, 2017, 8(12): 20 452-20 461. |
| [8] | Kwon MJ, Min SK, Seo J, et al. Hipk2 Expression in progression of cutaneous epithelial neoplasm[J]. Int J Dermatol, 2015, 54(3): 347-354. DOI: 10.1111/ijd.2015.54.issue-3. |
| [9] | Wook Choi D, Yong Choi C. Hipk2 Modification Code for Cell Death and Survival[J]. Mol Cell Oncol, 2014, 1(2): e955999. DOI: 10.1080/23723548.2014.955999. |
| [10] | de la Vega L, Grishina I, Moreno R, et al. A redox-regulated sumo/acetylation switch of Hipk2 controls the survival threshold to oxidative stress[J]. Mol Cell, 2012, 46(4): 472-483. DOI: 10.1016/j.molcel.2012.03.003. |
| [11] | Chiocca S, Seiser C. Lifting the threshold between life and death: Sumo and Hdac fine-tune Hipk2 to sense redox status[J]. Mol Cell, 2012, 46(4): 382-383. DOI: 10.1016/j.molcel.2012.05.010. |
| [12] | de la Vega L, Frobius K, Moreno R, et al. Control of nuclear Hipk2 localization and function by a sumo interaction motif[J]. Biochim Biophys Acta, 2011, 1 813(2): 283-297. |
| [13] | van der Laden J, Soppa U, Becker W. Effect of tyrosine autophosphorylation on catalytic activity and subcellular localisation of homeodomain-interacting protein kinases (Hipk)[J]. Cell Commun Signal, 2015, 13: 3. DOI: 10.1186/s12964-014-0082-6. |
| [14] | Polonio-Vallon T, Kirkpatrick J, Krijgsveld J, et al. Src kinase modulates the apoptotic P53 pathway by altering Hipk2 localization[J]. Cell Cycle, 2014, 13(1): 115-125. DOI: 10.4161/cc.26857. |
| [15] | Saul VV, de la Vega L, Milanovic M, et al. Hipk2 kinase activity depends on cis-autophosphorylation of its activation loop[J]. J Mol Cell Biol, 2013, 5(1): 27-38. DOI: 10.1093/jmcb/mjs053. |
| [16] | Siepi F, Gatti V, Camerini S, et al. Hipk2 catalytic activity and subcellular localization are regulated by activation-loop Y354 autophosphorylation[J]. Biochim Biophys Acta, 2013, 1 833(6): 1 443-1 453. |
| [17] | Upadhyay M, Bhadauriya P, Ganesh S. Heat shock modulates the subcellular localization, stability, and activity of Hipk2[J]. Biochem Biophys Res Commun, 2016, 472(4): 580-584. DOI: 10.1016/j.bbrc.2016.03.035. |
 2018, Vol. 39
2018, Vol. 39


