溶酶体相关4次跨膜蛋白质β(lysosome-associated protein transmembrane 4 beta,LAPTM4B)基因,广泛地分布于人体的多种组织中[1],研究表明组织内异常表达的LAPTM4B与乳腺癌及胃癌的预后具有相关性[2, 3]。在前期研究中,本实验组发现LAPTM4B在前列腺癌组织中表达具有特异性,显著上调的LAPTM4B与多种前列腺癌患者的临床病理指标相关[4]。已有研究表明在肝癌等其他肿瘤中LAPTM4B表达水平增加可促进细胞从G1期进入S期,抑制细胞凋亡,促进肿瘤细胞增殖、迁移和侵袭[5]。到目前为止LAPTM4B在前列腺癌的发生发展中的生物功能报道尚少。鉴于此,本实验在体外水平通过沉默LAPTM4B基因表达,研究LAPTM4B对前列腺癌细胞增殖和转移的影响。
1 材料与方法 1.1 前列腺细胞培养人正常前列腺上皮细胞(RWPE-1)置于K-SFM培养基(Gibco公司)中;LNCaP细胞, DU145细胞和PC-3细胞置于含有10%胎牛血清(Invitrogen公司)的RPMI 1640培养基(加拿大Life Technologies公司)中。以上细胞在37 ℃、5% CO2孵箱内培养。
1.2 RNA干扰(RNAi)实验设计并合成LAPTM4B短发卡RNA(shRNA)序列,LAPTM4B shRNA的目标序列为ATGCTGTGGTACTGTTGA-TTT。将pSilencer-shRNA质粒与pSilencerTM载体构建。细胞分为未转染组,空载体转染组和LAPTM4B shRNA转染组。用lipofectamine 2000介导转染前列腺癌细胞进行RNAi实验。在细胞转染48 h后,进行细胞克隆实验及细胞侵袭迁移实验。
1.3 实时荧光定量聚合酶链反应(qRT-PCR)使用Trizol法对不同组前列腺癌细胞中的总RNA进行提取。取2 μl RNA溶液对总RNA浓度及完整性进行检测。按反转录试剂盒(Thermo scientific)说明将各组提取的总RNA再取等量的RNA逆转录成cDNA。使用实时定量荧光PCR仪(美国ABI公司)按照试剂盒说明书以cDNA为模板, 使用LAPTM4B特定引物(上海生工生物有限公司合成),进行PCR扩增。依据各组LAPTM4B循环阈值Ct采用2-△△Ct结果作为测定LAPTM4B的mRNA相对表达量。
1.4 软琼脂细胞克隆形成实验制备浓度为1.2%和0.7%两种低熔点琼脂糖液,高压灭菌后用于制备双琼脂层。1.2%琼脂糖液和20%胎牛血清的RPMI 1640培养液按1:1体积混合,取3 ml平铺培养皿。调整各种前列腺癌细胞浓度至1×106/L。0.7%琼脂糖液和20%胎牛血清的RPMI 1640培养液按1:1体积混合后加入细胞悬液铺于已铺好高浓度琼脂糖液的培养皿中。每孔接种前列腺癌细胞1 000个。培养2周后显微镜下计数克隆数。
1.5 前列腺癌细胞侵袭和迁移实验调整各组无血清前列腺癌细胞悬液浓度至2×105/L,迁徙实验中将Transwell小室上层中放100 μl前列腺癌细胞悬液,下层中放含10%胎牛血清的完全培养基700 μl;侵袭实验中采用Matrigel胶包被的Transwell小室。常规培养48 h,使用0.5%结晶紫染色。拍照显微镜观察结果,随机挑选6个视野计算穿膜的细胞数,每处重复3次。
1.6 统计学方法采用SPSS 17.0统计软件分析。计量资料已均数±标准差(x±s)。多组间均数比较均采用单因素反差分析(One-Way ANOVA),以P<0.05为差异有统计学意义。
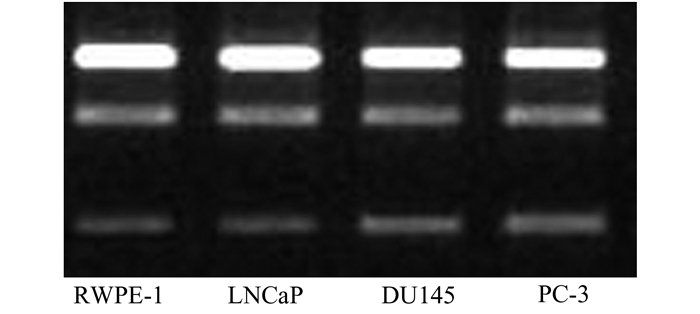
2 结果 2.1 前列腺细胞总RNA质量鉴定将RWPE-1、LNCaP、DU145和PC-3细胞中提取的RNA经0.8%琼脂糖凝胶电泳。结果显示清晰的28S和18S区带且两区带灰度比约为2:1,表明提取的RNA具有较好的完整性和均一性(图 1)。经核酸定量仪测OD260/OD280值在1.7-2.0之间,表示提取的RNA纯度较好。
|
图 1 前列腺细胞总RNA琼脂糖凝胶电泳 |
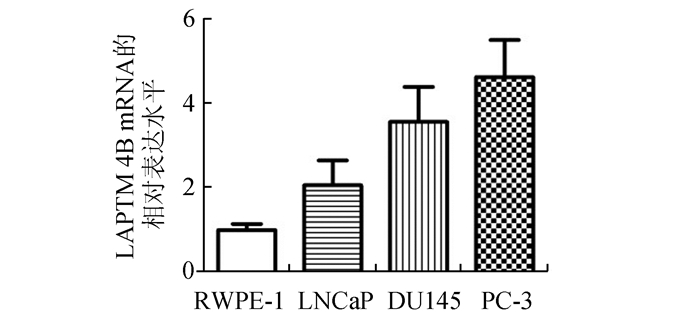
我们使用qRT-PCR技术检测前列腺RWPE-1、LNCaP、DU145和PC-3细胞中LAPTM4B mRNA的表达水平,结果显示LNCaP、DU145和PC-3细胞中LAPTM4B mRNA水平较RWPE-1明显增高,且差异具有统计学意义(P=0.001 2),其中LAPTM4B在PC3细胞中相对表达水平最高(图 2)。鉴于以上结果,选择LNCaP和PC-3细胞作为后续RNAi实验的细胞系。
|
图 2 前列腺细胞LAPTM4B mRNA相对表达水平 |
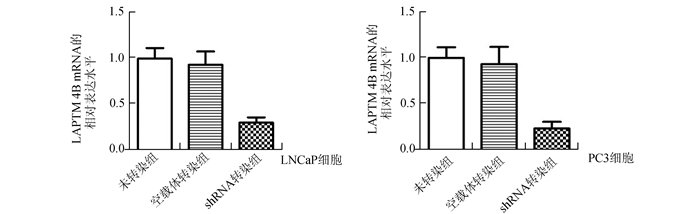
分别提取LNCaP和PC-3细胞中未转染组,空载体转染组和LAPTM4B shRNA转染组中总RNA,利用qRT-PCR技术检测各组细胞中LAPTM4B mRNA的相对表达水平。结果显示LNCaP和PC-3细胞中LAPTM4B的表达在未转染组和空载体转染组比较没有变化,无统计学意义(P>0.05);而LAPTM4B shRNA转染组较未转染组和空载体转染组中LAPTM4B的表达水平明显下调, 差异有统计学意义(P=0.038 3,P=0.045)如图 3中A和B。
|
图 3 质粒转染后LNCaP和PC-3细胞LAPTM4B mRNA表达相对水平 |
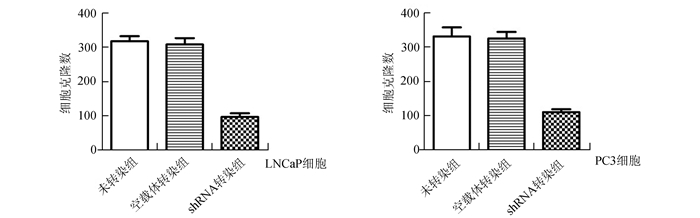
通过体外克隆形成实验检验LAPTM4B对LNCaP和PC-3细胞增殖能力的影响。如图 4中A和B显示LNCaP和PC-3细胞中LAPTM4B shRNA转染组细胞的体外克隆形成能力明显低于未转染组和空载体转染组, 差异有统计学意义(P<0.000 1); LNCaP和PC-3细胞中未转染组和空载体转染组细胞克隆之间无显著差别,无统计学意义(P>0.05)。
|
图 4 质粒转染后各组LNCaP和PC-3细胞克隆形成数示意图 |
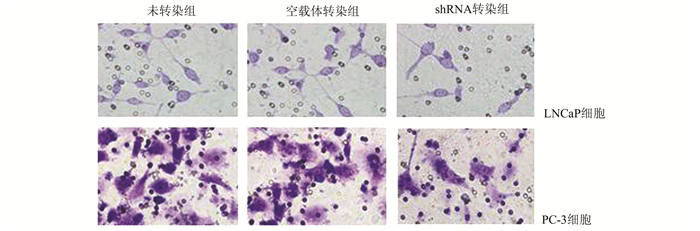
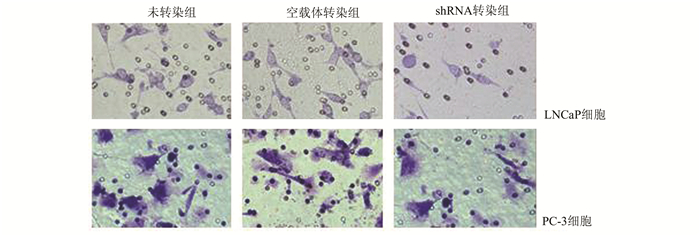
通过不铺和铺人工基底膜Matrigel两种Transwell趋化小室模型来分别观察下调LAPTM4B后LNCaP和PC-3细胞迁移和侵袭能力的变化。结果如图 5和6所示, LAPTM4B shRNA转染组PC-3和LNCaP细胞到达对侧的迁移细胞数明显低于未转染组和空载体转染组,差异有统计学意义(P<0.05);到达对侧的迁移PC-3和LNCaP细胞数在未转染组和空载体转染组之间无统计学意义(P>0.05)。
|
图 5 Transwell细胞迁移实验比较各组细胞的迁移能力 |
|
图 6 Transwell细胞侵袭实验比较各组细胞的侵袭能力 |
在本实验组的前期研究中发现LAPTM4B在前列腺癌组织中表达上调,并与前列腺癌患者的血PSA、Gleason评分、临床分期和精囊侵犯密切相关。为进一步明确LAPTM4B在前列腺癌中的表达情况,本实验对比了前列腺癌细胞系LNCaP、DU145和PC-3与人正常前列腺上皮细胞RWPE-1中LAPTM4B的表达水平。结果显示三种前列腺癌系中LAPTM4B mRNA水平较RWPE-1明显增高,其中LAPTM4B在PC3细胞中相对表达水平最高。以上结果再次证明了LAPTM4B在前列腺癌中高表达。
异常表达的LAPTM4B在前列腺癌中的调控作用尚不明确。有文献报道,转染LAPTM4B的小鼠NIH3T3细胞具有在NIH小鼠体内形成纤维肉瘤的特性[6],LAPTM4B基因过表达可导致肝脏正常上皮细胞L02发生恶性转化[7]。由此我们可以推断,LAPTM4B可能是调控细胞增殖、分化及恶性转化的重要因素,并在恶性转化过程中发挥重要的作用。为进一步明确LAPTM4B在前列腺癌中的生物功能,我们在下调LAPTM4B基因表达的条件下,研究LAPTM4B对前列腺癌细胞增殖、迁徙和侵袭能力的影响。人工构建shRNA LAPTM4B质粒,筛选出成功转染shRNA的前列腺癌细胞株。对比转染前后不同组前列腺癌细胞的克隆形成数,结果显示下调LAPTM4B后,前列腺癌细胞增殖能力明显下降。对比转染前后不同组前列腺癌细胞在Transwell趋化小室中到达对侧的迁移细胞数,结果显示下调LAPTM4B后,前列腺癌细胞肿瘤迁移和侵袭能力明显下降。
以上结果表明LAPTM4B基因与前列腺癌肿瘤发生发展及生物学行为密切相关,但是其生物学结构及功能尚未得到全面的揭示,详细的分子机制还需要进一步的研究。有报道发现上调LAPTM4B在子宫颈癌细胞HeLa中的表达可显著激活PI3K/AKT信号通路[8]。我们将在进一步研究中探讨在前列腺癌中LAPTM4B发挥促进肿瘤细胞增殖和转移作用的信号通路。
综上所述,LAPTM4B在前列腺癌肿瘤中的高表达,下调的LAPTM4B在前列腺癌细胞中的表达可以抑制肿瘤细胞的增殖与转移能力。LAPTM4B是一个与细胞增殖、分化乃至恶性转化调控相关的原癌基因[6, 7],在肿瘤的发生发展过程中发挥重要作用。
| [1] | Meng Y, Wang L, Chen D, et al. LAPTM4B: an oncogene in various solid tumors and its functions[J]. Oncogene, 2016, 35(50): 6359-6365. DOI: 10.1038/onc.2016.189. |
| [2] | Li XY, Kong XN, Chen X, et al. LAPTM4B allele *2 is associated with breast cancer susceptibility and prognosis[J]. PLoS One, 2012, 7(9): e44916. DOI: 10.1371/journal.pone.0044916. |
| [3] | Liu LY, Xu XF, Jing LL, et al. Lysosomal-associated protein transmembrane 4 beta-35 overexpression is a novel Independent prognostic marker for gastric carcinoma[J]. PLoS One, 2015, 10(2): e0118026. DOI: 10.1371/journal.pone.0118026. |
| [4] |
郭佳, 刘修恒, 王敏, 等. 溶酶体相关4次跨膜蛋白质β基因在前列腺癌组织的表达及临床意义[J].
中华实验外科杂志, 2015, 32(12): 2973-2975.
Guo J, Liu XH, Wang M, et al. Overexpressed lysosome-associated protein transmembrane 4 beta is associated with prostate cancer[J]. Chinese Journal of Experimental Surgery, 2015, 32(12): 2973-2975. DOI: 10.3760/cma.j.issn.1001-9030.2015.12.018. |
| [5] | Li MJ, Zhou RL, Shan Y, et al. Targeting a novel cancer-driving protein (LAPTM4B-35) by a small molecule (ETS) to inhibit cancer growth and metastasis[J]. Oncotarget, 2016, 7(36): 58531-58542. |
| [6] |
何静, 邵根泽, 周柔丽. 肝癌中高表达的新基因LAPTM4B对细胞增殖及成瘤性的影响[J].
北京大学学报:医学版, 2003, 35(4): 348-352.
He J, Shao G, Zhou R. Effects of the novel gene, LAPTM4B, highly expression in hepatocellular carcinoma on cell proliferation and tumorigenesis of NIH3T3 cells[J]. Journal of Peking University: Health Sciences, 2003, 35(4): 348-352. |
| [7] | Li L, Shan Y, Yang H, et al. Upregulation of LAPTM4B-35 promotes malignant transformation and tumorigenesis in L02 human liver cell line[J]. Anat Rec, 2011, 294(7): 1135-1142. DOI: 10.1002/ar.v294.7. |
| [8] | Manning BD, Cantley LC. AKT/PKB signaling: navigating downstream[J]. Cell, 2007, 129(7): 1261-1274. DOI: 10.1016/j.cell.2007.06.009. |
 2018, Vol. 39
2018, Vol. 39


