肠缺血再灌注(intestinal ischemia-reperfusion, IIR)是极其严重和复杂的临床问题,可导致肠道细菌屏障破坏,细菌移位,从而引发全身炎症反应(systemic inflammatory response syndrome, SIRS)和多器官功能障碍综合征(multiple organ dysfunction syndrome, MODS)[1],累及肾脏、肺脏、肝脏和心脏。由于再灌注期导致的低血压和氧化应激反应,肾脏成为肠缺血再灌注损伤的一个重要靶器官[2]。然而,肠缺血再灌注致肾脏损伤的分子机制尚未阐明。
作为人参主要成分的人参皂苷Rb1,在多脏器缺血再灌注损伤的机制研究中发挥了保护作用。其抗肿瘤、抗凋亡和抗氧化应激作用已得到广泛证实。但是,人参皂苷Rb1对肠缺血再灌注所致肾脏损伤的防治作用及其机制尚待阐明。本实验主要研究细胞凋亡在肠缺血再灌注所致肾脏损伤保护作用中的机制。
1 材料与方法 1.1 实验动物及分组野生型成年雄性C57 BL/6J小鼠,9-12周,实验前禁食12 h,自由饮水。所有小鼠随机分为5组(每组10只):①假手术组(Sham组),仅分离而不夹闭肠系膜上动脉;②模型组(IIR组):夹闭肠系膜上动脉缺血45 min,后开放再灌注2 h;③生理盐水组(NS组):再灌注前给予10 ml/kg的生理盐水;④低剂量组(Rb1-30组):再灌注前给予30 mg/kg的人参皂苷Rb1(生理盐水溶解成3 mg/ml,按10 ml/kg给药;浓度99.5%,购于中医药学研究中心);⑤高剂量组(Rb1-60组):再灌注前给予60 mg/kg的人参皂苷Rb1(生理盐水溶解成6 mg/ml,按10 ml/kg给药)。
1.2 小鼠肠缺血再灌注模型制备采用野生型成年雄性C57小鼠,腹腔注射戊巴比妥钠(50 mg/kg)麻醉后复制IIR模型[3],腹部正中脱毛,消毒铺巾,正中切口进腹,分离肠系膜上动脉,微动脉夹夹闭肠系膜上动脉根部,观察2 min,确定血管搏动消失,肠壁苍白,肠系膜上动脉血流被阻断后,缝合伤口。45 min后经原切口进腹,松开动脉夹恢复血供。整个手术过程中,于腹腔内滴加温热37 ℃生理盐水维持体内内环境平衡。假手术组同样开腹,除不钳夹血管外其余操作相同。再灌注2 h后采取肾脏标本。
1.3 观察及检测指标 1.3.1 肾组织病理学评估左肾固定包埋后,用苏木精-伊红染色。在光学显微镜(BX50;Olympus Optica,日本)下观察各组肾组织。利用McWhinnie[4]等方法对肾小管坏死进行半定量病理学评分。每个肾脏标本累计100个交叉处的剖面肾小管损伤总分,最高为300分。
1.3.2 肾脏组织超氧化物歧化酶(SOD)和丙二醛(MDA)检测取50 mg肾脏组织,加入0.9 ml生理盐水制成10%的组织匀浆。采用硫代巴比妥酸法测定MDA含量,邻苯三酚法测定SOD活性,具体操作步骤参照试剂盒(购于南京建成生物技术公司)说明书。
1.3.3 肾脏TUNEL细胞检测将肾脏组织石蜡包埋切片,运用TUNEL细胞凋亡检测试剂盒(购于武汉博士德公司)检测,TUNEL阳性上皮细胞计数分析。
1.3.4 肾脏组织Caspase-3蛋白免疫组化分析将肾脏组织石蜡包埋切片,运用免疫组化SP法检测Caspase-3含量。细胞质中黄色部分视为阳性。运用Image-Pro® Plus version 6.0进行半定量分析。
1.3.5 肾脏组织Caspase-3蛋白Western Blot分析组织样品用蛋白提取试剂盒(购于Santa Cruz公司)提取胞质蛋白,BCA法测蛋白浓度。BandScan分析胶片灰度值。
1.4 统计学处理采用SPSS 13.0统计软件分析数据,计量资料以均数±标准差表示,组间比较采用单因素方差(ANOVA)分析,组间比较采用t检验,P<0.05为差异有统计学意义。
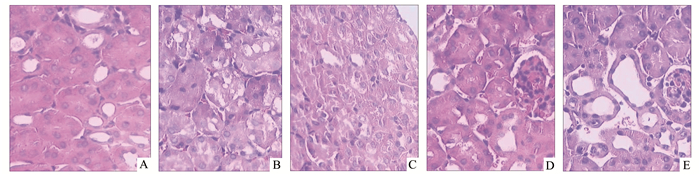
2 结果 2.1 肾脏组织病理学评估在图 1中,IIR组的肾小管出现病理损伤,包括水肿、坏死和空泡化。NS组改善并不明显。而给予30 mg/kg和60 mg/kg Rb1处理可明显减轻肾小管水肿、坏死和空泡化损伤。
|
图 1 肾脏组织病理学损伤(HE×400) A: Sham组; B: IIR组; C:NS组; D:Rb1-30组; E:Rb1-60组 |
与Sham组(16.70±4.06)比较,IIR组(198.60±9.71)和NS组(196.80±9.20)病理损伤评分显著增高(P<0.01);与IIR组比较,Rb1-30组(135.10±8.71)和Rb1-60组(94.60±9.24)病理学评分明显降低(P<0.05)。
2.2 肾脏组织SOD和MDA含量变化在IIR组,再灌注后可明显降低SOD活性并提高MDA的含量(P<0.01)。较之于IIR组,给予30 mg/kg和60 mg/kg Rb1则可提高SOD活性并降低MDA的含量(P<0.01),且呈剂量依赖性(表 1)。
| 表 1 肾脏组织SOD和MDA含量(x±s, n=10) |
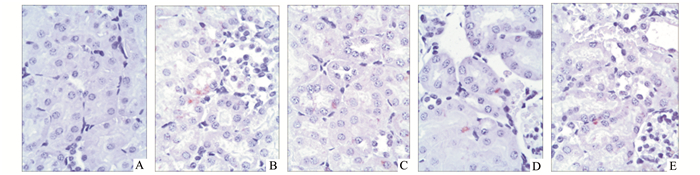
与Sham组(0.90±0.27)比较,IIR组(16.00±0.73)和NS组(16.70±0.90)肾脏TUNEL阳性细胞率(%)显著增高(P<0.01);与IIR组比较,Rb1-30组(12.90±0.38)和Rb1-60组(10.30±0.45)肾脏TUNEL阳性细胞率明显降低(P<0.05)。见图 2。
|
图 2 肾脏组织TUNEL细胞检测(×400) A: Sham组; B: IIR组; C: NS组; D: Rb1-30组; E: Rb1-60组 |
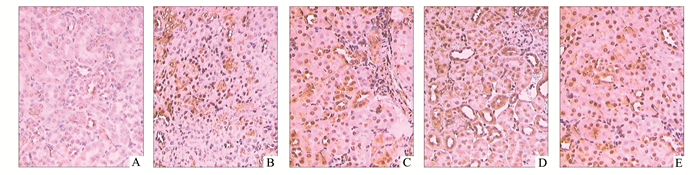
Sham组Caspase-3蛋白在胞质中极少表达,而IIR组细胞质中Caspase-3蛋白显著表达。与IIR组比较,给予30 mg/kg和60 mg/kg Rb1则可降低Caspase-3蛋白表达(P<0.01),且呈剂量依赖性(图 3, 表 2)。
|
图 3 肾脏组织Caspase-3蛋白表达免疫组化(SP×200) A: Sham组; B: IIR组; C: NS组; D: Rb1-30组; E: Rb1-60组 |
| 表 2 肾脏组织Caspase-3蛋白表达变化(x±s, ,n=8) |
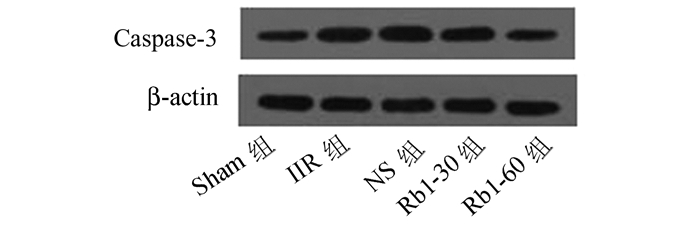
Sham组中Caspase-3蛋白表达极弱,而IIR组Caspase-3蛋白显著表达(P<0.01)。与IIR组比较,给予30 mg/kg和60 mg/kg Rb1则可降低Caspase-3蛋白表达(P<0.01),且呈剂量依赖性(图 4;表 2)。
|
图 4 肾脏组织Caspase-3蛋白表达(Western Blot) |
肠缺血再灌注损伤(IIR)仍然是一个十分严峻的临床问题,严重的创伤、感染和休克均能导致肠缺血再灌注的发生,其死亡率高达60%-80%[5]。肠缺血再灌注损伤破坏了肠黏膜屏障功能,引起肠道细菌移位和内毒素血症,严重者可引起全身炎症反应综合征(SIRS)和多器官功能障碍综合征(MODS)。所以肠缺血再灌注及其远隔脏器损伤的发生机制及其防治成为亟待解决的热点问题。
氧化应激介质是缺血再灌注损伤的关键环节,如活性氧簇(ROS),可诱导脂质过氧化和蛋白质氧化反应[6]。肠缺血再灌注导致体内氧自由基主要由黄嘌呤氧化酶及中性粒细胞、巨噬细胞呼吸爆发产生。SOD是一种氧化还原酶,可以催化氧化应激反应,缺血再灌注使得大量氧自由基聚集会导致过量的SOD消耗,SOD活性下降[7]。同时缺血再灌注所引发的脂质过氧化反应和前列腺素生物合成反应都可产生MDA。组织和血液中MDA的含量可以直接推测氧自由基导致的细胞损伤程度[8]。本研究发现,小肠缺血45 min,再灌注120 min导致肾小管上皮细胞出现大量水肿、坏死和空泡化现象,病理损伤严重,病理学评分显著增高。再灌注明显降低肾脏组织中SOD活性,同时升高MDA含量。表明肠缺血再灌注引发了肾脏损伤,其损伤与肠缺血再灌注导致全身氧化应激反应、肾脏氧自由基大量蓄积密切相关。
肠道的局部炎症反应和缺血缺氧可激活细胞凋亡基因的表达,肠道再灌注后全身氧自由基大量产生,肾小管上皮细胞内大量氧自由基堆积,可使细胞膜脂质过氧化、DNA破坏等损伤,诱导细胞凋亡,同时钙超载激活一系列钙依赖性酶促反应, 促进了细胞凋亡的发生[9]。Caspase家族在介导细胞凋亡的过程中起着非常重要的作用,其中Caspase-3为细胞凋亡的关键蛋白水解酶,它在凋亡信号传导的许多途径中发挥核心作用,亦是所有凋亡途径的最后效应因子[10]。Caspase-3正常以酶原的形式存在于胞质中,在凋亡的早期阶段,它被激活,活化的Caspase-3能够激活脱氧核糖核酸酶, 裂解DNA成碎片,最终导致细胞凋亡[11]。本研究中肾脏TUNEL凋亡细胞检测发现肠缺血再灌注导致肾小管上皮细胞凋亡大量增加,同时免疫组化结果及Western Blot分析发现Caspase-3蛋白在IIR组表达较Sham组显著增高(P<0.01)。表明肠缺血再灌注诱发了肾小管上皮细胞凋亡,其主要与氧化应激有关,并最终导致肾脏组织损伤。
近年来大量研究表明,人参皂苷Rb1在抗氧化、清除氧自由基、抗炎症反应、抗肿瘤和提高学习记忆等方面有较强活性[12]。本研究证实给予Rb1(30 mg/kg和60 mg/kg)则可减轻肾脏病理学损伤,降低病理学评分和肾脏组织MDA含量。与此同时肾脏SOD活性增加,其增加可保护细胞免受过氧化物的损伤。与IIR组比较,在人参皂苷Rb1治疗组肾脏TUNEL凋亡阳性细胞率增加,Caspase-3蛋白表达显著降低(P<0.01)。本实验亦揭示了人参皂苷Rb1减轻肾脏损伤的保护和凋亡的抑制作用呈剂量相关性。
综上所述,本研究证实人参皂苷Rb1对肠缺血再灌注所致肾小管上皮细胞凋亡具有保护作用,其机制可能与减少细胞内ROS过氧化损伤产物和保护线粒体功能有关。其确切的作用靶点和信号转导途径仍有待于进一步深入研究。
| [1] | Tassopoulos A, Chalkias A, Papalois A, et al. The effect of antioxidant supplementation on bacterial translocation after intestinal ischemia and reperfusion[J]. Redox Rep, 2017, 22(1): 1-9. DOI: 10.1080/13510002.2016.1229893. |
| [2] | Alexandropoulos D, Bazigos GV, Doulamis IP, et al. Protective effects of N-acetylcystein and atorvastatin against renal and hepatic injury in a rat model of intestinal ischemia-reperfusion[J]. Biomed Pharmacother, 2017, 89: 673-680. DOI: 10.1016/j.biopha.2017.02.086. |
| [3] | Teke Z, Sacar M, Yenisey C, et al. Activated protein C attenuates intestinal reperfusion-induced acute lung injury: an experimental study in a rat model[J]. Am J Surg, 2008, 195(6): 861-873. DOI: 10.1016/j.amjsurg.2007.06.025. |
| [4] | McWhinnie DL, Thompson JF, Taylor HM, et al. Morphometric analysis of cellular infiltration assessed by monoclonal antibody labeling in sequential human renal allograft biopsies[J]. Transplantation, 1986, 42(4): 352-358. DOI: 10.1097/00007890-198610000-00004. |
| [5] | Grootjans J, Lenaerts K, Buurman WA, et al. Life and death at the mucosal-luminal interface: New perspectives on human intestinal ischemia-reperfusion[J]. World J Gastroenterol, 2016, 22(9): 2760-2770. DOI: 10.3748/wjg.v22.i9.2760. |
| [6] | Bhattacharyya A, Chattopadhyay R, Mitra S, et al. Oxidative stress: an essential factor in the pathogenesis of gastrointestinal mucosal diseases[J]. Physiol Rev, 2014, 94(2): 329-354. DOI: 10.1152/physrev.00040.2012. |
| [7] | Kanzaki H, Wada S, Narimiya T, et al. Pathways that regulate ROS scavenging enzymes, and their role in defense against tissue destruction in periodontitis[J]. Front Physiol, 2017, 8: 351. DOI: 10.3389/fphys.2017.00351. |
| [8] | Chen Z, Wang D, Liu X, et al. Oxidative DNA damage is involved in cigarette smoke-induced lung injury in rats[J]. Environ Health Prev Med, 2015, 20(5): 318-324. DOI: 10.1007/s12199-015-0469-z. |
| [9] | Marques GM, Rasslan R, Belon AR, et al. Pentoxifylline associated to hypertonic saline solution attenuates inflammatory process and apoptosis after intestinal ischemia/reperfusion in rats[J]. Acta Cir Bras, 2014, 29(11): 735-741. DOI: 10.1590/S0102-86502014001800007. |
| [10] | Lo HC, Yang RB, Lee CH. Guanylyl cyclase-G modulates jejunal apoptosis and inflammation in mice with intestinal ischemia and reperfusion[J]. PLoS One, 2014, 9(7): e101314. DOI: 10.1371/journal.pone.0101314. |
| [11] | Yang Q, Zheng FP, Zhan YS, et al. Tumor necrosis factor-alpha mediates JNK activation response to intestinal ischemia-reperfusion injury[J]. World J Gastroenterol, 2013, 19(30): 4925-4934. DOI: 10.3748/wjg.v19.i30.4925. |
| [12] | Yang X, Xiong X, Wang H, et al. Protective effects of panax notoginseng saponins on cardiovascular diseases: a comprehensive overview of experimental studies[J]. Evid Based Complement Alternat Med, 2014, 2014: 204840. |
 2018, Vol. 39
2018, Vol. 39


