依托咪酯是一种短效、非巴比妥类的镇静催眠药,其麻醉效能强,起效快,尤其适用于血流动力学不稳定的患者。它对呼吸仅有轻微的抑制作用,因此依托咪酯是麻醉诱导的理想药物[1]。然而含有丙二醇的依托咪酯仍然存在许多的不良反应,虽然乳剂依托咪酯取代水剂依托咪酯后静脉炎、溶血、注射痛等不良反应已基本消失,但其引起肌阵挛的副反应至今仍未解决,发生率高达50%-80%[2]。有研究发现预注全麻药物如阿片类药物、苯二氮卓类和罗库溴铵可不同程度地减轻依托咪酯引起的肌阵挛[3]。曲马多是阿片受体的弱激动药,可选择性地激动μ受体, 并抑制五羟色胺(5-HT)和去甲肾上腺素(NE)的重摄取。该药具有镇痛作用较强、持续时间较长、依赖性潜力较低的特点[4]。同时曲马多也用于治疗或预防术后颤抖并取得良好效果[5]。治疗剂量的曲马多不抑制呼吸,对呼吸频率、潮气量、动脉血CO2分压均无影响,其副作用较少,故曲马多明显优于芬太尼。预注曲马多是否能减轻肌阵挛尚未见文献报道。由于曲马多较好的抗寒颤作用且副作用相比其他药物而言较小,因此,本研究通过预注低剂量和较高剂量的曲马多观察其对肌阵挛的影响,初步探讨曲马多是否有减轻依托咪酯全麻诱导中引起肌阵挛的作用。
1 临床资料 1.1 一般资料本研究经患者知情同意及本院道德和伦理委员会批准后进行。择期全麻下手术患者90例,男42例,女48例,ASAⅠ或Ⅱ级,年龄30-64岁,体重51-74 kg。排除标准:近期服用镇静及阿片类药物,神经系统疾病,体重低于标准体重80%或高于标准体重120%。随机均分为T1组(1 mg/kg曲马多),T2组(2 mg/kg曲马多)和T0组(同等剂量的生理盐水),每组人数均为30例。
1.2 麻醉方法本研究为前瞻性、双盲、随机对照研究。患者术前均不用药,入室后,建立静脉通路,持续输注复方乳酸钠,速率为10 ml/(kg·h)。常规监测心电图、无创血压、脉搏血氧饱和度。T1组:预注1 mg/kg曲马多;T2组:预注2 mg/kg曲马多;T0组:生理盐水对照组。该负责推注实验药物的麻醉医师不参与此次研究。5 min后静注0.3 mg/kg依托咪酯并观察有无肌阵挛发生,同时记录肌阵挛的严重程度。间隔1 min后三组均静注0.6 mg/kg罗库溴铵,5 μg/kg芬太尼行气管插管。实验期间同时记录无创动脉血压(BP)和心率(HR)。
1.3 观察指标由一名不知受试患者分组情况的麻醉医师负责观察并记录实验指标。在给予预注药液后,观察并询问患者有无呼吸困难,并记录用药前(BASE)、用药后(PI)、插管前(BIT)及插管后1 min(IT1)、5 min(IT5)的心率(HR)和无创动脉血压(BP)。0级为无肌阵挛发生;1级为轻度肌阵挛(肢体某一部分微小的运动, 如一个手指或肩膀的运动);2级为中度肌阵挛(两块不同的肌肉或肌肉群的轻微运动,如脸或腿);3级为重度(两块或者更多的肌肉的强烈的挛缩,如肢体的快速外展)[6]。
1.4 统计学分析所有数据用均数±标准差表示。采用SPSS 22.0统计软件进行数据分析。计量资料采用单因素方差分析,计数资料采用卡方检验。P<0.05为差异有统计学意义。
2 结果 2.1 一般资料、肌阵挛的发生率和严重程度三组患者性别、年龄、身高、体重以及既往疾病等一般情况比较,差异无统计学意义(表 1)。T0组有28例出现肌阵挛(93%,n=30),其中轻度2例,中度8例,重度18例; 而T1组有24例出现肌阵挛(80%,n=30%),T2组21例(70%,n=30)。T1和T2组肌阵挛的发生率明显低于对照组T0,且差异有统计学意义(表 2,P<0.01)。
| 表 1 患者一般资料 |
| 表 2 肌阵挛发生情况的比较[n(%)] |
对照组T0没有不良反应的发生,T1组眩晕2例,T2组恶心6例、眩晕8例、呼吸困难6例。由此T2组不良反应的发生率明显高于T0组和T1组(表 3,P<0.05),而T1组和T0组差异无统计学意义。
| 表 3 不良反应的比较 |
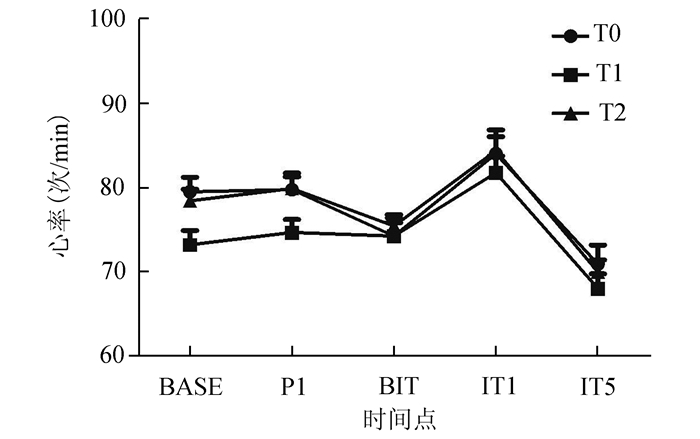
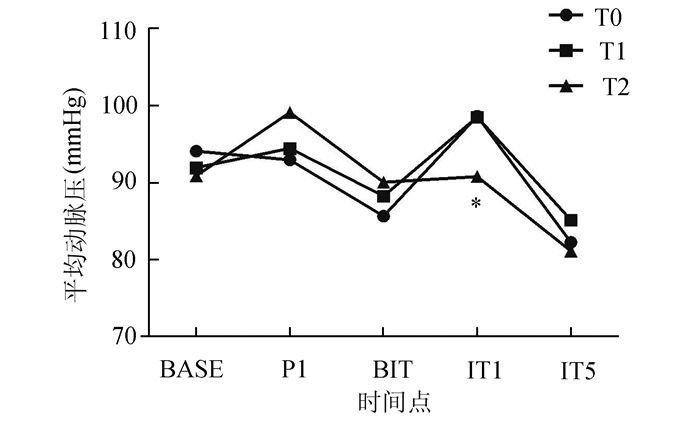
三个组间心率的变化较为一致,无明显变化(图 1)。三个组间平均动脉压的变化也较为一致,除了T2组在插管后1 min时的平均动脉压明显降低,且都低于T0组和T1组(P<0.05,图 2)。
|
图 1 心率的组间比较 |
|
图 2 平均动脉压的组间比较 *IT1时,T1和T2相比,P<0.05, T0和T2相比,P<0.05 |
依托咪酯是咪唑类衍生的静脉麻醉药, 其注射引起的肌阵挛可导致眼压升高从而增加玻璃体脱垂的危险。本研究旨在找到适合剂量的曲马多,并应用其预处理达到减少肌阵挛发生,减轻其严重程度,且不伴有明显副反应的效果。依托咪酯引起肌阵挛的机制目前尚不清楚,可能是由于依托咪酯作用于大脑中的γ-氨基丁酸A型受体, 从而抑制中枢神经网状激活系统[7],表现为皮质下不被抑制,即在皮质下活动抑制前皮质活动已经被抑制。
研究表明,预注芬太尼、阿芬太尼以及舒芬太尼等阿片类药物对依托咪酯诱导时的肌阵挛均有一定的预防作用[8]。但较大剂量的阿片类药物适用于时间较长的外科手术,对于短小手术以及门诊手术,可能会引起呼吸抑制、苏醒延迟、术后恶心呕吐等并发症。预注苯二氮卓类、阿片类以及罗库溴铵等药物可不同程度地抑制依托咪酯诱导时所致的肌阵挛[9-11]。Fassoulaki等[12]报道以100 μg的芬太尼预处理可使依托咪酯肌阵挛的发生率降低,同时呼吸抑制的发生几率增大。Stockham等[3]报道以0.3 μg/kg的舒芬太尼预处理也可降低依托咪酯引起肌阵挛的发生率,但和对照组相比病人表现出明显的高镇静率和低通气率。而治疗剂量的曲马多不抑制呼吸,对呼吸频率、潮气量、动脉血CO2分压均无影响,故相比较减小其副作用而言,曲马多明显优于芬太尼。在此次研究中,剂量为1 mg/kg和2 mg/kg的曲马多均能减少由依托咪酯引起的肌阵挛的发生率和严重程度。其中,中到重度的肌阵挛发生率分别为T0组86.6%,T1组46.7%,T2组43.3%(T1 vs T0,P<0.01;T2 vs T1,P<0.01),而T1组和T2组差异无统计学意义。相反,T2组不良反应的发生率明显高于T1组(P<0.05)。因此,基于以上结论我们认为,低剂量的曲马多(1 mg/kg)可以明显减少肌阵挛的发生率和严重程度,且无明显副反应。
曲马多抑制肌阵挛的作用可能是通过阿片机制和非阿片机制结合的协同作用方式实现的,即作用于μ-阿片类受体以及去甲肾上腺素和血清张力素系统,它可以通过作用于μ阿片受体以及弱亲和力的δ受体和κ受体来调节中缝核的活动[2, 6, 13],同时也抑制去甲肾上腺素和五羟色胺的重摄取。曲马多无明显的呼吸抑制和镇静作用的药效学特点使得它比其他阿片类受体激动剂更安全。
本研究中,三组间的血流动力学的变化大体一致,除了T2组在插管后1 min时的平均动脉压明显降低,且都低于T0组和T1组,可能是由于较高剂量的曲马多降低了插管时血浆中儿茶酚胺升高的浓度。
总之,这是首次临床研究表明曲马多抑制由0.3 mg/kg依托咪酯引起的肌阵挛,且无明显的镇静、呼吸抑制、呕吐等副作用。曲马多能有效降低患者肌阵挛的发生率和严重程度,且预注剂量为1 mg/kg的曲马多更能提供稳定的血流动力学。这为临床麻醉静脉诱导提供了参考,是较理想的静脉麻醉选择。
| [1] | Wu GN, Xu HJ, Liu FF, et al. Low-dose ketamine pretreatment reduces the incidence and severity of myoclonus induced by etomidate: a randomized, double-blinded, controlled clinical trial[J]. Medicine (Baltimore), 2016, 95(6): e2701. |
| [2] | Doenicke AW, Roizen MF, Hoernecke R, et al. Solvent for etomidate may cause pain and adverse effects[J]. Br J Anaesth, 1999, 83(3): 464-466. |
| [3] | Huter L, Schreiber T, Gugel M, et al. Low-dose intravenous midazolam reduces etomidate-induced myoclonus: a prospective, randomized study in patients undergoing elective cardioversion[J]. Anesth Analg, 2007, 105(5): 1 298-1 302. |
| [4] | Abreu M, Aguado D, Benito J, et al. Tramadol-induced hyperalgesia and its prevention by ketamine in rats: A randomised experimental study[J]. Eur J Anaesthesiol, 2015, 32(10): 735-741. |
| [5] |
曹建平, 徐建国. 曲马多和哌替啶用于全麻后寒战的预防[J].
中华麻醉学杂志, 2003, 23(3): 60-61.
Cao JP, Xu JG. Tramadol and Pethidine for the prevention of shivering after general anesthesia[J]. Chin J Anesthesiol, 2003, 23(3): 60-61. |
| [6] | Doenicke AW, Roizen MF, Kugler J, et al. Reducing myoclonus after etomidate[J]. Anesthesiology, 1999, 90(1): 113-119. |
| [7] | Nooraei N, Solhpour A, Mohajerani SA. Priming with atracurium efficiently suppresses etomidate-induced myoclonus[J]. Acta Anaesthesiologica Taiwanica, 2013, 51(4): 145-148. DOI: 10.1016/j.aat.2013.12.005. |
| [8] | Ri HS, Shin SW, Kim TK, et al. The proper effect site concentration of remifentanil for prevention of myoclonus after etomidate injection[J]. Korean J Anesthesiol, 2011, 61(2): 127-132. DOI: 10.4097/kjae.2011.61.2.127. |
| [9] | El-okdi NS, Lumbrezer D, Karanovic D, et al. Serotonin syndrome after the use of tramadol and ziprasidone in a patient with a deep brain stimulator for Parkinson disease[J]. Am J Ther, 2014, 21(4): e97-e99. |
| [10] | He L, Ding Y, Chen H, et al. Dezocine pretreatment prevents myoclonus induced by etomidate: a randomized, double-blinded controlled trial[J]. J Anesth, 2015, 29(1): 143-145. DOI: 10.1007/s00540-014-1854-2. |
| [11] | Lv Z, Fang J, Zhu J, et al. Intravenous dezocine pretreatment reduces the incidence and intensity of myoclonus induced by etomidate[J]. J Anesth, 2014, 28(6): 944-947. DOI: 10.1007/s00540-014-1842-6. |
| [12] | Fassoulaki A, Pateras C, Kaniaris P. Fentanyl in the prevention of etomidate-induced myoclonus[J]. Cah Anesthesiol, 1987, 35(3): 201-202. |
| [13] | Miyano K, Minami K, Yokoyama T, et al. Tramadol and its metabolite m1 selectively suppress transient receptor potential ankyrin 1 activity, but not transient receptor potential vanilloid 1 activity[J]. Anesth Analg, 2015, 120(4): 790-798. |
 2018, Vol. 39
2018, Vol. 39


