2. 湖南省急救医学研究所 急危重症代谢组学湖南省重点实验室;
3. 湖南省人民医院急诊科
2. Hunan Provincial Institute of Emergency Medicine, Hunan Provincial Key Laboratory of Emergency and Critical Care Metabonomics, Changsha, China;
3. Emergency Department, Hunan Provincial People's Hospital, Changsha, China
心脏骤停(CA)是临床上最为常见的急危重症之一,近年来随着心肺复苏术(CPR)的普及和高级生命支持的进步,CA患者自主循环恢复(ROSC)率有所提高,但患者出院存活率及长期生存率并未见明显改善[1]。有研究表明,复苏后心肌功能障碍是患者早期高死亡率的主要原因之一,约占23%[2]。因此,CA患者ROSC后心肌保护有重大意义。2015年美国心脏协会(AHA)心肺复苏与心血管急救指南指出,所有在CA后ROSC的昏迷且血流动力学尚稳定的成年患者,都应采用治疗性亚低温,尤其能改善CA后缺血缺氧脑病的神经功能障碍[3]。另有研究表明,亚低温治疗对CA后心肌功能障碍亦具有保护作用[4]。代谢组学技术是研究生物体在基因修饰下或病理生理刺激下的动态代谢变化,其研究对象是小分子代谢物(<1000Da),这些变化在人类疾病、药理及毒理学、系统生物学等研究领域有广泛的应用[4]。本研究旨在通过利用超高效液相色谱-飞行时间质谱(UPLC-QTOF-MS)技术对ROSC后大鼠的心肌进行检测,探究亚低温干预后的代谢改变,发现潜在的生物标志物,以及亚低温改善CA致心肌组织损伤的机制。
资料和方法 一、研究对象实验动物及分组:雄性SD大鼠,体重220~300g,购于湖南斯莱克景达实验动物有限公司,许可证:SCXK(湘)2013-0004,动物实验通过伦理委员会批准(批件:2019-S60)。按随机数字表法将ROSC后大鼠分为常温组(n=10)、亚低温组(n=10)。
二、CA大鼠模型制作SD大鼠禁食不禁水12h,水合氯醛腹腔麻醉,固定于小动物手术台,股动脉置动脉留置针,连接至动脉压力传感器监测平均动脉压(MAP),股静脉置静脉留置针,用于复苏药物的注射,生物机能试验仪监测心电图(ECG)、心率(HR)变化,温度探测器监测直肠温度,气管插管后,ECG示心电静止、电机械分离,未扪及心脏搏动,MAP<20mmHg的标准采用窒息的方式诱导CA,CA 3min后立即行胸外心脏按压,同时接小动物呼吸机行机械通气,注射肾上腺素、碳酸氢钠直至ROSC,如5min后无ROSC则剔除,术后适当补液防止脱水。
三、亚低温治疗大鼠CPR成功20min内,将多个冰袋置于其周边快速诱导低温,维持直肠温度在33.0±0.5℃,3h后缓慢复温,以0.5℃/h的速率复温。
四、指标监测及标本采集连续监测两组大鼠的ECG、HR、MAP,记录CA前窒息持续时间、CPR至ROSC持续时间,ROSC后24h取左室及心尖部心肌行苏木精-伊红(HE)染色、代谢组学检测。
五、UPLC-QTOF-MS分析将100mg心肌自然解冻后置于离心管中,加入50%甲醛-水(1:1,v:v)混合溶液1000uL,旋涡20s后离心(12000rpm、4℃)10min,将上清液转移至新的EP管中,快速离心浓缩仪中挥干,加入50%乙腈200uL复溶,充分混匀,室温静置10min,再次离心(12000rpm、4℃)10min,吸取200uL上清液经PTEF过滤后进行代谢组学分析。
六、差异代谢物的筛选和统计学分析通过Metaboscape 4.0软件处理UPLC-QTOF-MS数据,将代谢物数据导入SIMCA-P 14.1软件,采用主成分分析(PCA)和正交偏最小二乘判别分析(OPLS-DA)各样本的总体分布及组间代谢轮廓的总体差异,以P<0.05,VIP值>1.5,差异倍数FC>1.2或<0.8作为筛选差异代谢物的条件,将内源性差异代谢物导入MetaboAnalyst 4.0进行代谢通路分析。
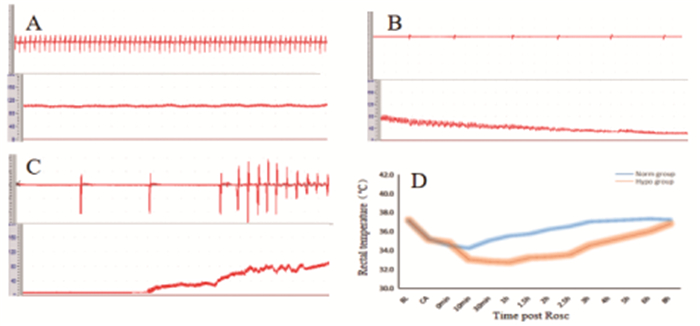
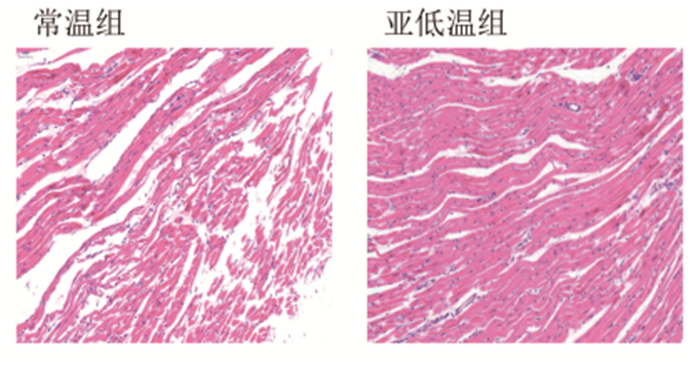
结果 一、亚低温对CA后大鼠心肌具有保护作用如表 1所示,两组大鼠的体重、直肠温度、MAP、HR在基线水平无统计学意义(P>0.05),实验大鼠窒息前(图 1A)、CA状态(图 1B)与ROSC(图 1C)后ECG、MAP波动变化如图 1,大鼠直肠温度变化曲线如图 1D,表明本研究CA模型制备成功且均质化,亚低温治疗方式亦是有效性的。在相同倍数光学显微镜下(20×),心肌HE染色显示:相对于亚低温组,常温组大鼠心肌结构紊乱,大部分心肌纤维断裂,心肌间质充血,可见血管扩张,细胞核染色不均匀(图 2),表明亚低温治疗在一定程度上可以改善心肌损伤程度。
| 表 1 两组大鼠基线水平生理参数 |
|
图 1 实验大鼠窒息与复苏过程中心电、血压、体温变化(A:窒息前基线水平;B:窒息诱发CA时;C:自主循环恢复时;D:直肠温度变化曲线) |
|
图 2 心肌组织HE染色(20×) |
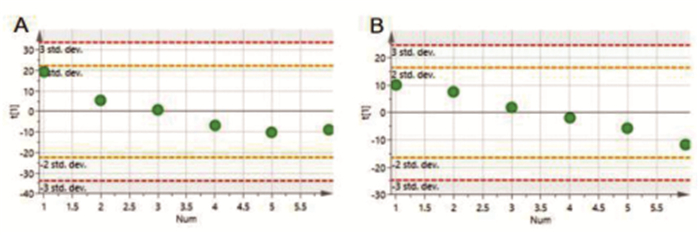
第一主成分散点图如图 3,结果显示正负离子模式下QC样品都在均数±2倍标准差范围内波动,提示系统稳定性和实验可控性均良好。
|
图 3 正离子(A)和负离子(B)模式下QC样品PCA散点图 |
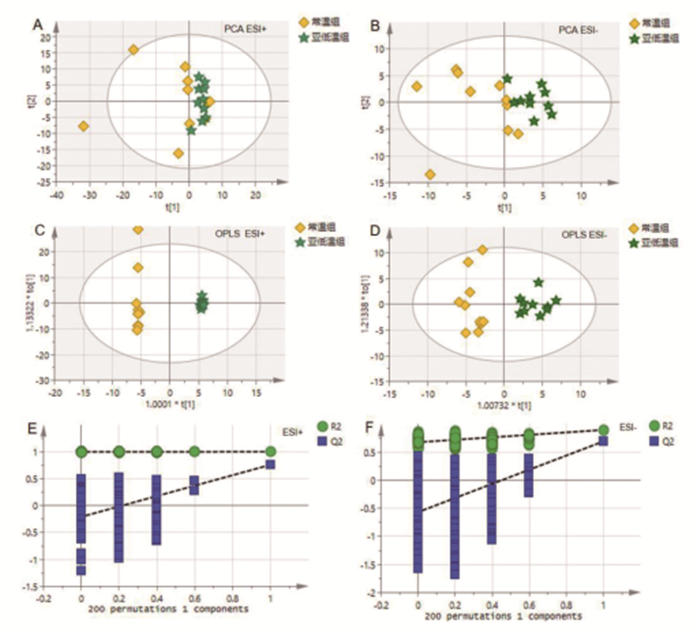
将数据导入SIMCA-P 14.1软件,对样本进行质量控制及归一化处理后,对正负离子模式下心肌组织的代谢组学数据进行PCA分析,结果如图 4A、B所示,正、负离子模式下,常温组和亚低温组代谢轮廓存在差异。进行OPLS-DA分析显示,正(图 4C)负(图 4D)离子模式下常温组和低温组之间代谢指纹显著不同,对OPLS-DA模型进行200次置换检验,提示OPLS-DA模型无“过拟合”现象,模型稳健性良好(图 4E、F)。
|
图 4 亚低温治疗后心肌组织代谢特征发生改变。正负离子模式下PCA得分图(A、B)、OPLS-DA得分图(C、D)和置换检验图(E、F) |
上述多元分析表明,常温组和亚低温组间代谢轮廓存在显著差异,将数据导入MetaboAnalyst 4.0软件,通过以P<0.05,VIP值>1.5,FC>1.2或<0.8的标准共筛选出差异代谢物20个,其中正离子模式下11个,负离子模式下9个,具体代谢物见表 2。
| 表 2 亚低温治疗后大鼠心肌组织中的差异代谢物 |
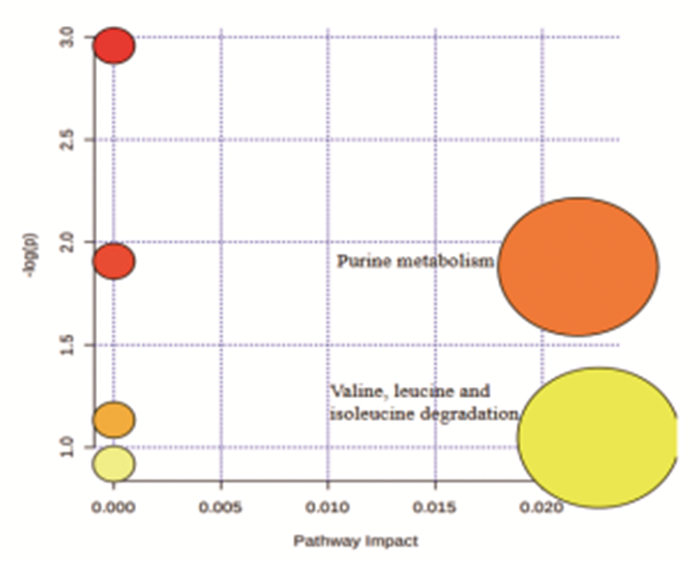
将心肌组织样本中内源性差异代谢物导入MetaboAnalyst 4.0进行代谢通路分析,结果如图 5所示,亚低温干预后心肌保护作用主要涉及嘌呤代谢、缬氨酸/亮氨酸/异亮氨酸代谢途径。
|
图 5 代谢通路图 |
近年来,CPR在复苏方法、药物、器械等方面有明显改善,但目前院外心脏骤停(OHCA)和院内心脏骤停(IHCA)患者存活率依然较低,复苏后心肌功能障碍是CA患者ROSC后未能长期存活的重要原因之一[5]。因此,减轻CA患者自主循环恢复后器官功能的损伤,有助于提高CA患者的生存率。亚低温治疗是目前证实可改善CA患者脑损伤的有效方法,研究表明,亚低温治疗对CA后心肌功能障碍可能存在保护作用[6~8]。本研究也证明,亚低温治疗可以改善CA后心肌损伤。然而,目前关于亚低温治疗温度、治疗方式、持续时间、复温时间及速率等存在诸多争议,治疗性亚低温也存在影响呼吸循环系统,加重凝血功能、内环境紊乱等异常变化[9]。因此,寻求新方法理解并阐明亚低温对心肌保护机制,最大程度减少其并发症意义重大。
代谢组学是新兴发展起来的研究系统生物学的一门技术,作为高通量的研究手段,可以整体分析机体动态代谢变化特征,阐明疾病的病理生理机制。本研究运用的UPLC-TOF-MS技术具有高通量、高分离度、高灵敏度等优势,尤其是在分析复杂样品中更为高效快速,且直接观察心肌代谢,较既往的血浆更具有说服力,有助于全面分析亚低温干预后的心肌代谢特征[10]。本研究筛选出20种内源性差异代谢物,嘌呤代谢、缬氨酸/亮氨酸/异亮氨酸代谢通路在亚低温干预后发生了明显改变。
本研究结果显示,甲基丙二酸(MMA)在常温组和亚低温组中是存在差异的,MMA是甲基丙二酰辅酶A的产物,参与细胞膜脂肪酸组成的代谢途径[11],甲基丙二酰辅酶A在线粒体基质中转化为琥珀酰辅酶A并进入三羧酸循环,并使脂肪酸和蛋白质产生能量[11],而MMA是氧化应激和线粒体功能障碍的生物标志物,且与心肌舒缩功能相关[12],说明亚低温可能通过改善CA后心肌中的能量代谢,减少氧化应激反应后的心肌破坏性病理进程。本研究中也观察到次黄嘌呤在亚低温干预后表达下调,次黄嘌呤在缺血条件下积累,其作为底物通过黄嘌呤氧化酶途径促进自由基的产生,并通过广泛的脂质过氧化作用导致局部和全身性氧化应激[13],而预处理可以阻断黄嘌呤或黄嘌呤氧化酶途径[14],亚低温治疗可能通过降低次黄嘌呤,从而减少自由基在心肌组织中的产生与蓄积。另外,γ亚麻酸、血栓素B2在两组中有显著差异,γ亚麻酸是前列腺素的前体物质,一方面可以抑制血小板聚集,另一方面可以抑制血栓素A2合成酶活性,减少血栓素A2、B2的生成,抑制脂质过氧化,减轻凝血系统的异常激活及血栓形成的风险[15]。
综上所述,本研究从形态学及代谢层面证实,亚低温一定程度上可以减轻CA后的心肌损伤,差异代谢物及相关通路分析表明亚低温可能通过减少氧自由基的生成、减轻氧化应激反应及凝血系统障碍等方面发挥保护作用。
| [1] |
Wissenberg M, Lippert FK, Folke F, et al. Association of national initiatives to improve cardiac arrest management with rates of bystander intervention and patient survival after out-of-hospital cardiac arrest[J]. JAMA, 2013, 310(13): 1377-1384. DOI:10.1001/jama.2013.278483 |
| [2] |
Laver S, Farrow C, Turner D, et al. Mode of death after admission to an intensive care unit following cardiac arrest[J]. Intensive Care Med, 2004, 30(11): 2126-2128. |
| [3] |
王增武, 董颖. 2015年《AHA心肺复苏与心血管急救指南》解读[J]. 中国循环杂志, 2015, 30(Z2): 8-22. DOI:10.3969/j.issn.1000-3614.2015.Z2.004 |
| [4] |
Krastanov A. Metabolomics-the state of art[J]. Biotechnology and Biotechnological Equipment, 2014, 24(1): 1537-1543. |
| [5] |
朱英, 黄淮, 颜景华, 等. 心肺复苏后多器官功能障碍综合征危险因素和预后分析[J]. 中国医师杂志, 2006, 8(8): 1048-1050. DOI:10.3760/cma.j.issn.1008-1372.2006.08.016 |
| [6] |
Bernard SA, Gray TW, Buist MD, et al. Treatment of comatose survivors of out-of-hospital cardiac arrest with induced hypothermia[J]. N Engl J Med, 2002, 346(8): 557-563. DOI:10.1056/NEJMoa003289 |
| [7] |
Peberdy MA, Callaway CW, Neumar RW, et al. Part 9:post-cardiac arrest care:2010 American Hcart Association Guidelines for cardiopulmonary resuscitation and emergency cardiovascular care[J]. Circulation, 2010, 122(18 Suppl 3): S768-786. |
| [8] |
Li YP, Fan ZX, Qin J, et al. Effect of pre-arrest and post-arrest mild hypothermia on myocardial function of ventricular fibrillation after restoration of spontaneous circulation in rabbits[J]. Chin Crit Care Med, 2015, 27(3): 185-189. |
| [9] |
Soleimanpour H, Rahmani F, Safari S, et al. Hypothermia after cardiac arrest as a novel approach to increase survival in cardiopulmonary cerebral resuscitation:a review[J]. Iran Red Crescent Med J, 2014, 16(7): e17497. |
| [10] |
Yoon D, Choi BR, Ma S, et al. Metabolomics for Age Discrimination of Ginseng Using a Multiplex Approach to HR-MAS NMR Spectroscopy, UPLC-QTOF/MS, and GC x GC-TOF/MS[J]. Molecules, 2019, 24(13): 2381. DOI:10.3390/molecules24132381 |
| [11] |
Green R, Allen LH, Bjorke-Monsen AL, et al. Vitamin B12 deficiency[J]. Nat Rev Dis Primers, 2017, 3: 17040. DOI:10.1038/nrdp.2017.40 |
| [12] |
Polytarchou K, Dimitroglou Y, Varvarousis D, et al. Methylmalonic Acid and Vitamin B12 in Patients with Heart Failure[J]. Hellenic J Cardiol, 2019, 15: S1109-9666(19)30286-6. |
| [13] |
Kaminski KA, Bonda TA, Korecki J, et al. Oxidative stress and neutrophil activation-the two keystones of ischemia/reperfusion injury[J]. Int J Cardiol, 2002, 86(1): 41-59. |
| [14] |
Peralta C, Bulbena O, Xaus C, et al. Ischemic preconditioning:a defense mechanism against the reactive oxygen species generated after hepatic ischemia reperfusion[J]. Transplantation, 2002, 73(8): 1203-1211. DOI:10.1097/00007890-200204270-00004 |
| [15] |
Nilsen D, Aarsetoey H, Ponitz V, et al. The prognostic utility of dihomo-gamma-linolenic acid (DGLA) in patients with acute coronary heart disease[J]. Int J Cardiol, 2017, 249: 12-17. DOI:10.1016/j.ijcard.2017.09.202 |
 2020, Vol. 4
2020, Vol. 4

