2. 湖南省人民医院(湖南师范大学附属第一医院)湖南省急救医学研究所 急危重症代谢组学湖南省重点实验室
2. Hunan Provincial Institute of Emergency Medicine, Hunan Provincial People's Hospital(the First Affiliated Hospital of Hunan Normal University), Hunan Provincial Key Laboratory of Emergency and Critical Care Metabonomics, Changsha, China
心脏骤停所致的突然死亡是现代医学面临的一个重要挑战,是最为严重的急危重症,包括院内心脏骤停(in-hospital cardiac arrest,IHCA)和院外心脏骤停(out-of-hospital cardiac arrest,OHCA)[1]。全球IHCA的年发病率的中位数为1.5‰,存活率为18.4%[2],有研究显示我国IHCA的年发病率为4.4‰[3]。全球OHCA的年发病率为63.8~113.6/100000,其存活率仅为1.2~12.8%,亚洲的存活率最低,仅为1.6~2.8%。及早有效的心肺复苏和电除颤与心脏骤停的存活情况显著正相关[1]。溺亡、缺氧、心肺疾病、药物过量、恶性肿瘤、休克、交通创伤是院外心脏骤停的主要原因。除了原发疾病,心脏骤停后的病人多伴有不同程度的脑缺氧损伤、全身的缺血再灌注损伤和心肌功能障碍[4]。代谢组学是通过考察生物体系在一特定生理时期内收到刺激或扰动前后所有小分子代谢物的组成及其含量变化,从而表征生物体系的整体代谢特征。其研究对象是分子量小于1000道尔顿的小分子物质,如糖、有机酸、脂质、维生素氨基酸、芳香烃之类的化合物[5]。本研究通过缺氧制作新西兰家兔的心脏骤停模型,从代谢组学层面探索心脏骤停家兔的血清代谢组学的变化,阐明心脏骤停的发病机理和了解心脏骤停代谢特征,为制定心脏骤停的有效干预策略提供理论依据和参考。
对象与方法 一、研究对象实验动物及分组:2.5kg体重的新西兰家兔,购于湖南斯莱克景达实验动物有限公司,许可证号:SCXK(湘)2013-0004。按随机数字表法将家兔分为假手术组(n=24)、心肺复苏常温治疗组织(n=24)。动物试验符合伦理学标准。
二、研究方法 (一) 心脏骤停家兔模型的制作[6]新西兰家兔禁食不禁水12h后,戊巴比妥麻醉,固定于兔台,耳缘动脉置动脉留置针,用于血压监测,生物机能实验仪检测心电、血压,温度探测器监测肛温和耳蜗温度,气管插管后,以心电显示无脉心电活动或无电活动,血压小于10mmHg的标准采用窒息的方式诱导室颤致心脏骤停,7min后给予动物呼吸机机械通气,注射肾上腺素并行胸外按压术至自主循环恢复。
(二) 标本采集连续监测家兔体温、血压,记录ROSC时间,肾上腺素用量,机械通气时间,并在心脏骤停前,自主循环恢复后30min,以及心脏骤停后24h从耳缘动脉抽血2ml进行代谢组学样本检测,同时抽取1ml完成血气分析。
(三) GC/MS分析将血浆自然解冻,取50μL加入内标(L-2-氯-苯丙氨酸0.3g/L,甲醇配置)、蛋白沉淀剂甲醇-乙腈(2:1),冰水浴超声提取,4℃离心10min,取上清液装入玻璃衍生瓶中挥干,加入甲氧胺盐酸吡啶溶液(15g/L),涡旋震荡,肟化,加入双(三甲基硅烷基)三氟乙酰胺〔BSTFA,含1%三甲基氯硅烷(TMCS)〕衍生试剂和正乙烷,涡旋震荡,70℃反应60min。室温放置30min,用7890A-5975C型GC-MS联用仪进行代谢组学分析。
(四) 代谢物鉴定通过ChromaTOF软件处理GC-MS数据,分析得315个代谢物。将代谢物数据矩阵导入SIMCA-P+14.0软件,采用主成分分析(PCA)和偏最小二乘判别分析(PLS-DA)各样本的总体分布以及各组间代谢轮廓的总体差异;采用t检验筛选组间差异代谢物。P < 0.05表示差异有统计学意义。
结果 一、心脏骤停致血气分析指标的变化收集心脏骤停组和假手术组的家兔在心脏骤停前、自主循环恢复后,心脏骤停后24h动脉血液标本,进行血气分析发现,相对于对照组,CA组家兔在自主循环恢复时乳酸含量显著增高,表现为酸中毒,然而氧分压有所增加,二氧化碳分压下降,心脏骤停后24h,CA组家兔的乳酸含量有所降低,但还是高于对照组,与自主循环恢复时间点不同的是,CA组家兔的氧分压出现了显著的下调。
| 表 1 心脏骤停家兔血清指标的变化 |
我们对心脏骤停家兔和假手术组家兔的血清样本进行GC-MS检测,共检测并识别出小分子代谢物共351个,通过以差异倍数>2,P < 0.05的标准共筛选出差异代谢物41个,其中上调表达的代谢物28个,下调表达的代谢物13个,具体代谢物见表 2,3。
| 表 2 心脏骤停家兔血清样本中表达上调的代谢物(差异倍数>2,P < 0.05) |
| 表 3 脏骤停家兔血清样本中表达下调的代谢物(差异倍数>2,P < 0.05) |
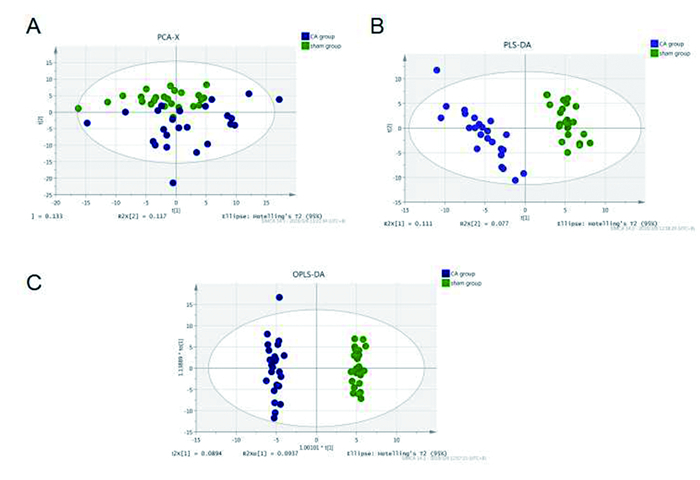
对假手术组和心脏骤停组家兔血清代谢物数据进行PCA分析发现,PCA图中假手术组样本主要位于左右的下象限,而心脏骤停组血清样本主要位于左右的上象限,说明心脏骤停组家兔血清代谢状态发生明显改变。对假手术组和心脏骤停组家兔血清代谢物数据进行PLS-DA分析发现,两组呈现明显差异,且PLS-DA模式分析结果明显优于PCA模式分析。通过OPLS-DA进一步证实假手术组和心脏骤停组家兔血清代谢轮廓存在显著差异。
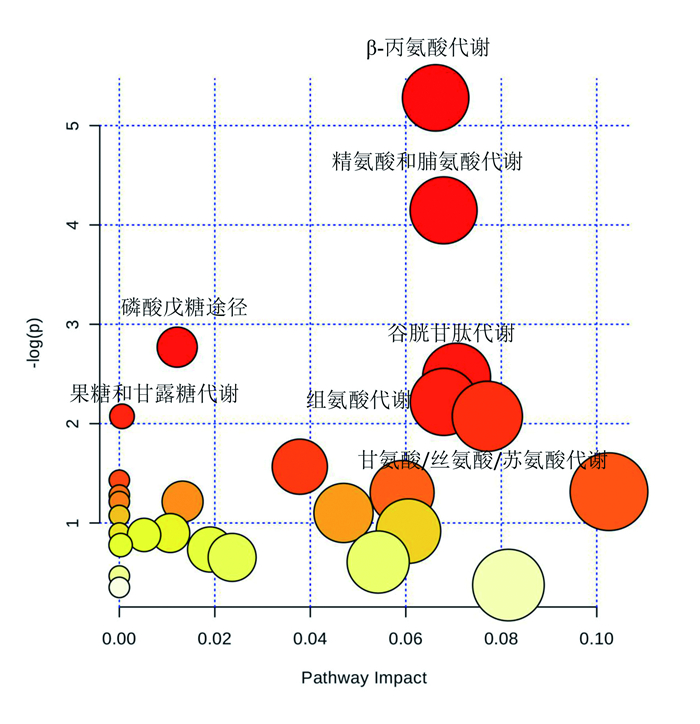
四、心脏骤停家兔的氨基酸和糖代谢发生明显紊乱通过对心脏骤停家兔的血清差异代谢物进行代谢通路分析发现,28条代谢通路在心脏骤停组和假手术组间存在差异(表 4),其中脂质代谢通路包括前原发性胆汁酸生物合成,氨基酸代谢通路包括β-丙氨酸代谢、精氨酸和丙氨酸代谢、甘氨酸、丝氨酸和苏氨酸代谢、组氨酸代谢、丙氨酸、硫代谢、天冬氨酸和谷氨酸代谢、亮氨酸和异亮氨酸生物合成、赖氨酸生物合成、色氨酸代谢、氮代谢、丙氨酸、半胱氨酸和蛋氨酸代谢、亮氨酸和异亮氨酸降解,糖类代谢包括谷胱甘肽代谢、果糖和甘露糖代谢、磷酸盐途径、咖啡因代谢、糖酵解、丁糖代谢、半乳糖代谢、淀粉和蔗糖代谢,维生素b6代谢,以及核苷酸代谢途径包括吡啶代谢、氨基乙酰-RNA生物合成、氨基酸和核苷酸代谢、嘌呤代谢。各代谢通路的权重见图 2。
| 表 4 假手术组与心脏骤停组差异代谢通路分析(Top 8) |
|
图 1 心脏骤停家兔血清代谢轮廓的改变。A,心脏骤停家兔和假手术组家兔血清代谢组学轮廓特征差异的PCA分析;B,心脏骤停家兔和假手术组家兔血清代谢组学轮廓特征差异的PLS-DA分析;C,心脏骤停家兔和假手术组家兔血清代谢组学轮廓特征差异的OPLS-DA分析 |
|
图 2 心脏骤停家兔差异性代谢通路分析 |
窒息可稳定性的诱导心脏骤停,致缺血再灌注损伤。机体的缺血损伤不仅限制了氧气和营养物质的供应,而且还阻止了机体代谢产生废物的排除。因此,心脏骤停所致的机体全身缺血缺氧损伤可引起可逆性或不可逆性的能量代谢紊乱、离子稳态、电生理、氨基酸、糖、脂质代谢异常[7]。同时心肺复苏又致再灌注损伤,再灌注过程中机体大量的ROS等有害物质对机体持续造成损伤。窒息诱导的心脏骤停过程中,机体的代谢特征一般发生率显著的改变。代谢组学是指对生物体液或组织中存在的低分子量代谢产物(metabolome)进行识别和定量,从而研究生命系统在基因修饰或生理病理刺激下的动态代谢变化。作为高通量的研究手段,结合生物信息学的分析技术,代谢组学用于疾病病情评估、早期诊断、预后及疗效评估生物标志物的筛选越来越受到重视[8, 9]。本研究通过窒息法成功制作的心脏骤停的家兔模型,检测其血清代谢组学发现心脏骤停家兔的糖、脂质、氨基酸和核酸等代谢发生了明显改变,筛选出41中差异代谢物,β-丙氨酸代谢、精氨酸和脯氨酸代谢、磷酸戊糖途径、谷胱甘肽代谢、组氨酸代谢、果糖和甘露糖代谢、甘氨酸/丝氨酸/苏氨酸代谢、色氨酸代谢等代谢通路在心脏骤停的过程中发生明显的改变。
在窒息诱导的心脏骤停家兔模型中,本研究在窒息前、ROSC恢复30min和心脏骤停后24h检测了血气分析,发现乳酸含量在心脏骤停复苏成功后30min后显著升高,可能是窒息造成的无氧糖酵解相关,而在CA后24h虽有回落,但乳酸水平还是明显高于假手术组,并且心脏骤停后出现明显的酸中毒,此结果与Junhwan Kim等研究报道一致[10]。不同的是,PO2在ROSC恢复30min略为增加,而心脏骤停后24h PO2显著下降,可能是ROSC后心脏骤停家兔刚完成机械通气,此时机体并不处于缺氧的状况,而心脏骤停致家兔心肌细胞损伤,故在心脏骤停后出现24h PO2显著下降。
心脏骤停血清代谢轮廓产生了明显改变,差异代谢物涉及糖、脂类、氨基酸和核酸代谢物。丙氨酸代谢参与糖代谢和尿酸循环,研究的结果提示在心脏骤停血清代谢通路中血清丙氨酸代谢通路、磷酸盐和糖酵解存在差异,提示各个代谢通路之间存在显著关联,是相互影响相互制约的关系。内源精氨酸主要来源于肾近曲小管中瓜氨酸的转化, 瓜氨酸则是由肠道内的谷氨酸和谷氨酰胺合成[11],本研究中谷氨酸代谢存在显著紊乱。谷氨酰胺代谢与ROS生成相关,谷胱甘肽代谢作为ROS清除途径其在心脏骤停的家兔中也是异常的。磷酸戊糖途径包括氧化部分和非氧化部分己糖激酶的催化下葡萄糖生成6磷酸葡萄糖。葡萄糖在6-磷酸葡萄糖脱氢酶,6-磷酸葡糖酸内酯酶(6-Phosphogluconolactonase)和6-磷酸葡萄糖酸脱氢酶协助下生成5-磷酸核酮糖。5-磷酸核酮糖可通过一系列基团转移反应,将核糖转变成6-磷酸果糖和3-磷酸甘油醛而进入糖酵解途径。磷酸戊糖途径与核苷酸的生物合成、糖酵解密切相关,此通路在本研究中均发生了明显的改变。
综上所述,心脏骤停家兔血清代谢特征发生了明显改变,涉及糖、脂类、氨基酸、维生素和核酸代谢物的表达异常,β-丙氨酸代谢、精氨酸和脯氨酸代谢、磷酸戊糖途径、谷胱甘肽代谢、组氨酸代谢、果糖和甘露糖代谢、甘氨酸/丝氨酸/苏氨酸代谢、色氨酸代谢等代谢通路在心脏骤停的过程中发生明显的改变。
| [1] |
Nolan, Jerry. Cardiac Arrest and Cardiopulmonary Resuscitation[J]. Seminars in Neurology, 2017, 37(01): 005-012. |
| [2] |
Berdowski J, Berg RA, Tijssen JG, et al. Global incidences of out-of-hospital cardiac arrest and survival rates:systematic review of 67 prospective studies[J]. Resuscitation, 2010, 11: 1479-1487. |
| [3] |
Shao F, Li CS, Liang LR, et al. Incidence and outcome of adult in-hospital cardiac arrest in Beijing, China[J]. Resuscitation, 2016, 102: 51-56. DOI:10.1016/j.resuscitation.2016.02.002 |
| [4] |
Madder RD, Reynolds JC. Multidisciplinary Management of the Post-Cardiac Arrest Patient[J]. Cardiology Clinics, 2018, 36(1): 85-101. DOI:10.1016/j.ccl.2017.08.005 |
| [5] |
Lindon JC, Nicholson JK, Holmes E, et al. Metabonomics:Metabolic processes studied by NMR spectroscopy of biofluids[J]. Concepts in Magnetic Resonance Part A, 2015, 12(5): 289-320. |
| [6] |
邹联洪, 祝益民, 刘晓亮, 等. 亚低温对心脏骤停家兔脑损伤保护作用的代谢组学研究[J]. 实用休克杂志, 2018, 2(6): 347-366. |
| [7] |
Sekhon MS, Ainslie PN, Griesdale DE. Clinical pathophysiology of hypoxic ischemic brain injury after cardiac arrest:a "two-hit" model[J]. Critical Care, 2017, 21(1): 90. DOI:10.1186/s13054-017-1670-9 |
| [8] |
Bracewellmilnes T, Saso S, Abdalla H, et al. Metabolomics as a tool to identify biomarkers to predict and improve outcomes in reproductive medicine:a systematic review[J]. Human Reproduction Update, 2017, 23(6): 723-736. DOI:10.1093/humupd/dmx023 |
| [9] |
Chalkias A, Fanos V, Noto A, et al. 1H NMR-metabolomics:Can they be a useful tool in our understanding of cardiac arrest?[J]. Resuscitation, 2014, 85(5): 595-601. DOI:10.1016/j.resuscitation.2014.01.025 |
| [10] |
Junhwan K, Tai Y, Ming Y, et al. Examination of Physiological Function and Biochemical Disorders in a Rat Model of Prolonged Asphyxia-Induced Cardiac Arrest followed by Cardio Pulmonary Bypass Resuscitation[J]. PLoS ONE, 2014, 9(11): e112012. DOI:10.1371/journal.pone.0112012 |
| [11] |
Morris SM Jr. Arginine Metabolism Revisited[J]. Journal of Nutrition, 2016, 146(12): 2579S-2586S. DOI:10.3945/jn.115.226621 |
 2019, Vol. 3
2019, Vol. 3

