院外心脏骤停(out-hospital cardiac arrest,OHCA)是一个重要的世界性公共健康问题,在我国每年发生院外心脏骤停的患者人数估计达到544 000人[1],而心脏骤停患者的存活率在美国也仅为15%[2],我们国家更低。脑组织是耗氧量极大的器官,心脏骤停所致的缺血缺氧以及复苏过程中的再灌注对其损伤极为严重[3]。亚低温治疗是唯一被公认为治疗心脏骤停致脑损伤的有效方式,但目前亚低温对心脏骤停后脑损伤保护作用的机制尚未达成共识,导致临床上对亚低温治疗的温度和时间的选择存在很大的争议。代谢组学是指对生物体液或组织中存在的低分子量代谢产物(metabolome)进行识别和定量,从而研究生命系统在基因修饰或生理病理刺激下的动态代谢变化[4]。作为高通量的研究手段,结合生物信息学的分析技术,代谢组学用于疾病病情评估、早期诊断、预后及疗效评估生物标志物的筛选越来越受到重视。本研究成功制作了缺氧所致的心脏骤停模型,心肺复苏成功后亚低温处理,基于GC-MS技术检测心脏骤停后不同时间的大鼠血浆的代谢组学,探讨心脏骤停致脑损伤和亚低温治疗对心脏骤停脑保护的可能分子机制。
资料和方法 一、研究对象实验动物及分组:2.5kg体重的新西兰家兔,购于湖南斯莱克景达实验动物有限公司,许可证号:SCXK(湘)2013-0004。按随机数字表法将家兔分为假手术组(n=6)、心肺复苏常温治疗组织(n=9)和亚低温治疗组(n=9)。动物试验符合伦理学标准。
二、研究方法(一)心脏骤停家兔模型的制作:新西兰家兔禁食不禁水12h后,戊巴比妥麻醉,固定于兔台,耳缘动脉置动脉留置针,用于血压监测,生物机能实验仪检测心电、血压,温度探测器监测肛温和耳蜗温度,气管插管后,以心电显示无脉心电活动或无电活动,血压小于10mmHg的标准采用窒息的方式诱导室颤致心脏骤停,7min后给予动物呼吸机机械通气,注射肾上腺素并行胸外按压术至自主循环恢复。
(二)亚低温治疗:将尿不湿加水湿润后冷冻12h,兔子心肺复苏成功后于兔台下置冰袋,兔台上置冷冻后的尿不湿快速降温,并维持体温32-35℃,3h后让其缓慢升温。
(三)神经缺陷量表评分:选3个观察员对兔子的意识水平、呼吸、神经反射、步态、感觉功能、行为等内容按神经缺陷量表进行评分。
(四)标本采集:连续监测家兔体温、血压,记录ROSC时间,肾上腺素用量,机械通气时间,并在心脏骤停前,心脏骤停后15min,30min,2h,6h,24h耳缘动脉抽血2mL。
(五)GC/MS分析:将血浆自然解冻,取50μL加入内标(L-2-氯-苯丙氨酸0.3g/L,甲醇配置)、蛋白沉淀剂甲醇-乙腈(2:1),冰水浴超声提取,4℃离心10min,取上清液装入玻璃衍生瓶中挥干,加入甲氧胺盐酸吡啶溶液(15g/L),涡旋震荡,肟化,加入双(三甲基硅烷基)三氟乙酰胺〔BSTFA,含1%三甲基氯硅烷(TMCS)〕衍生试剂和正乙烷,涡旋震荡,70℃反应60min。室温放置30min,用7890A-5975C型GC-MS联用仪进行代谢组学分析。
(六)代谢物鉴定:通过ChromaTOF软件处理GC-MS数据,分析得315个代谢物。将代谢物数据矩阵导入SIMCA-P+14.0软件,采用主成分分析(PCA)和偏最小二乘判别分析(PLS-DA)各样本的总体分布以及各组间代谢轮廓的总体差异;采用t检验筛选组间差异代谢物。P<0.05表示差异有统计学意义。
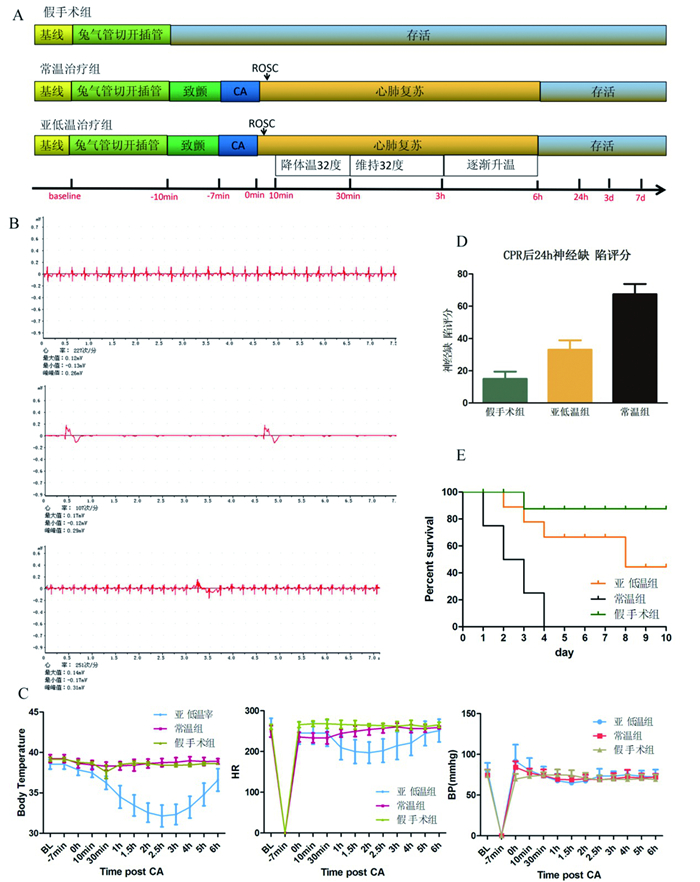
结果 一、亚低温改善心脏骤停家兔的脑损伤并增加存活率家兔行气管切开术并插管,窒息致心脏骤停7min后心肺复苏,成功构建了心脏骤停模型(图 1A, B),复苏成功后1h内降低体温至32-35℃(图 1C),心电监测发现心脏骤停家兔复苏后心率的变化趋势与体温一致(图 1C),血压在各组间不存在明显差异(图 1C)。家兔心肺复苏后24h的脑神经缺陷评分显示:常温治疗组的家兔脑组织损伤最为严重,亚低温治疗可以改善心脏骤停致家兔脑组织的损伤(图 1D),生存分析发现亚低温治疗可以提高心肺复苏成功的心脏骤停家兔的存活率(图 1E)。
|
图 1 研究流程(A), 通过窒息法成功制作了心脏骤停家兔模型(B), 自主循环恢复后15min到6h, 心率、体温、血压的变化(C)。24h后脑神经缺陷评分(D), 亚低温组、常温组、假手术组心脏骤停家兔生存分析(E)。 |
|
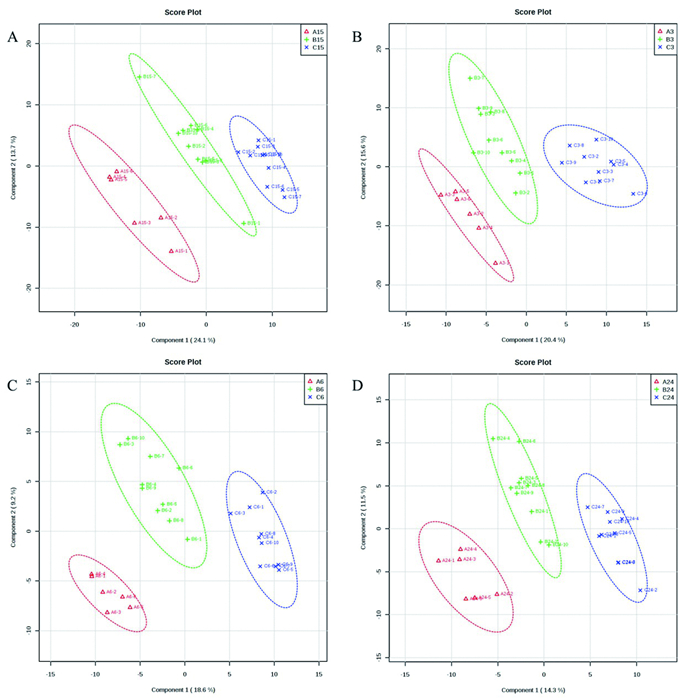
图 2 假手术组、常温治疗组、亚低温治疗组心肺复苏后15min (A), 3h (B), 6h (C), 24h (D)差异性代谢产物的PLS-DA分析。红色代表假手术组, 绿色代表亚低温治疗组, 蓝色代表亚低温治疗组。 |
GC/MS平台分析心脏骤停家兔经亚低温和常温治疗后不同时间点血浆代谢组学。按表达差异倍数大于1.5,P<0.05的标准,筛选出的假手术组、亚低温治疗组和常温治疗组的差异代谢产物数如表 1所示:在自主循环回复后的30min,3h,6h,24h,检测出的常温组和假手术组之间的差异性代谢产物分别有118, 57, 51, 54个,检测出的亚低温组和假手术组间差异性代谢产物分别有79, 58, 34, 33个,检测出的常温组和亚低温组之间的差异性代谢产物分别有91, 97, 87, 79个与常温治疗组相比,亚低温治疗组家兔的不同时间点血浆差异性代谢产物(前10)如表 2所示。
| 表 1 假手术组、常温治疗组、亚低温治疗组间的差异代谢产物数 |
| 表 2 常温组与亚低温组心肺复苏家兔模型血浆代谢产物变化(TOP10) |
对不同时间点假手术组、常温治疗组和亚低温治疗组的差异性代谢产物进行最小二乘判别分析(PLS-DA)发现,各时间点的假手术组、常温治疗组和亚低温治疗组的代谢均存在明显差异,但与常温治疗组相对,亚低温治疗组心脏骤停家兔模型的代谢轮廓与假手术组更为接近,从代谢组学层面提示亚低温治疗对心脏骤停家兔具有保护作用。
讨论美国每年发生院外心脏骤停的患者估计有325 000人[5],欧洲每年约有350000名院外心脏骤停患者[6],在中国,每年发生院外心脏骤停的患者人数估计达到544000人[1]。随着血管升压类药物的使用、心肺复苏术的实施和心脏除颤的应用,心脏骤停患者自主循环恢复(return of spontaneous circulation,ROSC)率在发达国家已达到了30%~40%[7]。尽管如此,仍有60%的心脏骤停患者无法恢复自主循环,并且仅有10%~15%的心脏骤停的患者能够成功出院[8],其中有超过1/3的心脏骤停的患者伴随有永久性的神经功能损害[9]。在自主循环恢复的心脏骤停患者中,缺血缺氧引起的脑组织损伤是导致其最终死亡的重要原因[2]。亚低温治疗是目前唯一被公认为治疗心脏骤停致脑损伤的有效方式[10, 11],本研究证实:亚低温治疗可有效改善心脏骤停致大脑的损伤,并且显著降低心脏骤停大鼠自主循环恢复后的死亡率。尽管如此,亚低温治疗干扰心脏骤停致脑损伤的机制是复杂的,且尚未完全阐明[12]。并且目前临床上对亚低温治疗心脏骤停患者的方式存在争论。为了如何避免或减少亚低温导致的并发症,最佳亚低温治疗的温度和时间是临床上关于亚低温治疗争论的焦点[13, 14]。阐明亚低温治疗心脏骤停脑损伤的机制有助于理解和明确最优亚低温治疗方式。
代谢组学可以监测来自组织或体液的数百种代谢产物,阐明疾病的病理生理机制,并确定了代谢变化的特征,可用于跟踪疾病发生进展的全过程[4]。尽管代谢组学技术仍处于发展阶段,但作为一种很有前途的工具,可用于确定生物通路和发现临床生物标志物,加强对心脏骤停预防和治疗的优化[15]。一项预测院外心脏骤停患者预后的代谢组学研究显示[16]:支链氨基酸和丙氨酸与心脏骤停的预后显著先关。在本研究中,与假手术组相比,血浆中丙氨酸水平上调,与此结果相符(数据未展示)。另一项心肺复苏的动物模型的代谢组学研究表明[17],血浆犬尿酸表达上调,色氨酸表达下调,且与心脏骤停心肺复苏的最终结局相关。本研究同样表明血浆犬尿酸和色氨酸的表达水平在假手术组、常温组、亚低温组的心脏骤停家兔的血浆中是存在差异的,提示心肺复苏后全尿酸通路是激活的。Dimitrios Varvarousis等[18]研究表明:在缺氧或室颤所致心脏骤停的动物模型,三羧酸循环,尿素循环发生紊乱,琥珀酸盐的高表达是心脏骤停预后不良的生物标志,在本研究中,与对照组相比,三羧酸循环代谢通路发了显著改变。代谢组学信息的主成分分析发现,假手术组、常温治疗组和亚低温治疗组心肺复苏后不同时间点的血浆样本是明显分离的,提示其代谢轮廓特征存在显著差异,而相对于常温治疗组,亚低温治疗组的心脏骤停家兔的代谢特征更接近于假手术组,从代谢组学的层面说明亚低温对心脏骤停是存在明确的治疗效果。
综上所述,本研究证实亚低温治疗可减轻心脏骤停的脑损伤,显著降低死亡率。与假手术组相比,常温组和亚低温组心脏骤停家兔的血浆代谢轮廓特征发生明显改变,相对于常温组,亚低温治疗处理的心脏骤停家兔心肺复苏成功后不同时间点的血浆代谢轮廓与假手术组更接近,从代谢组学的层面证实:亚低温对心脏骤停有明确的保护作用。
| [1] |
Hua W, Zhang LF, Wu YF, et al. Incidence of sudden cardiac death in China:analysis of 4 regional populations[J]. Journal of the American College of Cardiology, 2009, 54(12): 1110-1118. DOI:10.1016/j.jacc.2009.06.016 |
| [2] |
Nolan JP, Neumar RW, Adrie C, et al. Post-cardiac arrest syndrome:epidemiology, pathophysiology, treatment, and prognostication. A Scientific Statement from the International Liaison Committee on Resuscitation; the American Heart Association Emergency Cardiovascular Care Committee; the Counc[J]. Resuscitation, 2008, 79(3): 350-379. DOI:10.1016/j.resuscitation.2008.09.017 |
| [3] |
Madl C, Holzer M. Brain function after resuscitation from cardiac arrest[J]. Current Opinion in Critical Care, 2004, 10(3): 213-217. DOI:10.1097/01.ccx.0000127542.32890.fa |
| [4] |
Lindon JC, Holmes E, Bollard ME, et al. Metabonomics technologies and their applications in physiological monitoring, drug safety assessment and disease diagnosis[J]. Biomarkers, 2010, 9(1): 1-31. |
| [5] |
Nichol G, Thomas E, Callaway CW, et al. Regional variation in out-of-hospital cardiac arrest incidence and outcome[J]. Journal of the American Medical Association, 2008, 300(12): 1423-1431. DOI:10.1001/jama.300.12.1423 |
| [6] |
Atwood C, Eisenberg MS, Herlitz J, et al. Incidence of EMS-treated out-of-hospital cardiac arrest in Europe[J]. Resuscitation, 2005, 67(1): 75-80. DOI:10.1016/j.resuscitation.2005.03.021 |
| [7] |
Willard W.Sharp. Dynamin-Related Protein 1 as a therapeutic target in cardiac arrest[J]. J Mol Med (Berl), 2015, 93(3): 243-252. DOI:10.1007/s00109-015-1257-3 |
| [8] |
Go AS, Mozaffarian D, Roger VL, et al. Heart disease and stroke statistics-2014 update:a report from the American Heart Association[J]. Circulation, 2014, 129: e28-e292. DOI:10.1161/CIRCULATIONAHA.113.003961 |
| [9] |
Patrick Meybohm, Matthias Gruenewald, Kai D Zacharowski, et al. Mild hypothermia alone or in combination with anesthetic post-conditioning reduces expression of inflammatory cytokines in the cerebral cortex of pigs after cardiopulmonary resuscitation[J]. Critical Care, 2010, 14: R21. DOI:10.1186/cc8879 |
| [10] |
Arrich J, Holzer M, Havel C, et al. Hypothermia for neuroprotection in adults after cardiopulmonary resuscitation[J]. Cochrane Database Syst Rev, 2012, 9: CD004128. |
| [11] |
Choi HA, Badjatia N, Mayer SA. Hypothermia for acute brain injury——mechanisms and practical aspects. Nature reviews[J]. Neurology, 2012, 8: 214-222. |
| [12] |
Yenari MA, Han HS. Neuroprotective mechanisms of hypothermia in brain ischaemia[J]. Nat Rev Neurosci, 2012, 13: 267-278. DOI:10.1038/nrn3174 |
| [13] |
Peberdy MA, Callaway CW, Neumar RW, et al. 2010 American heart association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care[J]. Circulation, 2010, 122(3): S768-S786. |
| [14] |
Nolan JP, Soar J, Zidemanetal DA. European resuscitation council guidelines for resuscitation 2010 section 1.executive summary[J]. Resuscitation, 2010, 8(10): 1219-1276. |
| [15] |
Chalkias A, Fanos V, Noto A, et al. 1H NMR-metabolomics:Can they be a useful tool in our understanding of cardiac arrest?[J]. Resuscitation, 2014, 85(5): 595-601. DOI:10.1016/j.resuscitation.2014.01.025 |
| [16] |
Tsai CL, Tsai MS, Kuo CH, et al. Metabolomic Profiling for Outcome Prediction in Emergency Department Patients with Out-of-Hospital Cardiac Arrest[J]. Resuscitation, 2017, 123: e1-e2. |
| [17] |
Ristagno G, Fries M, Brunelli L, et al. Early kynurenine pathway activation following cardiac arrest in rats, pigs, and humans ☆[J]. Resuscitation, 2013, 84(11): 1604-1610. DOI:10.1016/j.resuscitation.2013.06.002 |
| [18] |
Varvarousis D, Xanthos T, Ferino G, et al. Metabolomics profiling reveals different patterns in an animal model of asphyxial and dysrhythmic cardiac arrest[J]. Scientific Reports, 2017, 7(1): 16575. DOI:10.1038/s41598-017-16857-6 |
 2018, Vol. 2
2018, Vol. 2

